获取国外Alprolix(静脉注射)药品价格,使用等信息,最快 24 小时回馈
Alprolix(静脉注射)
Alprolix(静脉注射)
FAK-tor NINE Fc FUE-准PROE-teen ree-KOM-bi-ant
常用品牌名称
在美国
- 阿普利克斯
可用的剂型:
- 溶液粉
Alprolix的用途
凝血因子IX Fc融合蛋白重组注射液作为按需治疗,可控制或预防B型血友病(先天性凝血因子IX缺乏症)患者的出血发作,预防手术中的出血或减少出血发作的频率。
IX因子是体内天然产生的蛋白质。 Alprolix®是一种人造蛋白质,可在体内复制天然存在的IX因子。它用于通过帮助血友病B的血液凝结来止血。
这种药物只能由您的医生或其他医疗保健专业人员或在其监督下服用。
使用Alprolix之前
在决定使用药物时,必须权衡服用药物的风险和所能带来的好处。这是您和您的医生会做出的决定。对于这种药物,应考虑以下几点:
过敏症
告诉您的医生您是否曾经对此药物或任何其他药物有任何异常或过敏反应。如果您还有其他类型的过敏症,例如食物,染料,防腐剂或动物,也请告知您的医疗保健专业人员。对于非处方产品,请仔细阅读标签或包装成分。
小儿科
迄今为止进行的适当研究尚未显示出会限制Alprolix®在儿童中使用的儿科特定问题。但是,小于12岁的孩子可能需要调整Alprolix®的剂量,具体取决于孩子的医生。
老年医学
尽管尚未在老年人群中进行关于年龄与Alprolix®作用的关系的适当研究,但迄今为止,尚无文献记载老年性问题。
哺乳
妇女没有足够的研究来确定在母乳喂养期间使用这种药物的婴儿风险。在母乳喂养期间服用这种药物之前,要权衡潜在收益与潜在风险。
与药物的相互作用
尽管某些药物根本不能一起使用,但在其他情况下,即使可能发生相互作用,也可以同时使用两种不同的药物。在这些情况下,您的医生可能希望更改剂量,或者可能需要其他预防措施。如果您正在服用其他处方药或非处方药(非处方药[OTC]),请告知您的医疗保健专业人员。
与食物/烟草/酒精的相互作用
在进食食物或进食某些类型的食物时或前后,不应使用某些药物,因为可能会发生相互作用。在某些药物上使用烟酒也可能引起相互作用。与您的医疗保健专业人员讨论将药物与食物,酒精或烟草一起使用的方法。
其他医疗问题
其他医疗问题的存在可能会影响该药的使用。确保您告诉医生是否还有其他医疗问题,尤其是:
- 血块或由血块引起的医疗问题史-请谨慎使用。这些情况可能会增加形成血块的风险。
- 患有IX因子抑制剂的患者-可能会增加发生过敏反应的风险。
正确使用Alprolix
医生或其他训练有素的健康专家将为您或您的孩子服用这种药。您也可能受过训练自己注射这种药物。这种药物是通过一根插入您一根静脉的针头给药的。
该药随附患者信息单张。仔细阅读并遵循说明非常重要。问您的医生是否有疑问。
使用Alprolix时的注意事项
在您或您的孩子服用这种药物时,请医生仔细检查您和孩子的病情,以确保其正常工作,这一点非常重要。需要进行血液测试以检查不良影响。
该药可能引起严重的过敏反应,包括过敏反应。这可能会危及生命,需要立即就医。如果您出现皮疹,皮肤瘙痒,吞咽困难,头晕,心跳加快,头晕或昏厥,躁动不安,呼吸困难,脸,手,舌头或喉咙肿胀或胸痛,请立即告诉您的医生或护士收到药后。
您的身体会产生针对这种药物的抗体(抑制剂),这可能会阻止其正常工作。您的医疗保健提供者可能需要不时测试您的血液中的这些抑制剂。
这种药可能会增加您出现凝血问题的机会。如果您在服用这种药物时突然或严重的头痛,视力或言语问题,胸痛,呼吸困难或麻木或无力,请立即告诉医生。
告诉您的医生这种药物是否不能按预期预防或止血。
使用这种药物可能会出现严重的肾脏问题。立即与您的医生联系,看看您的尿液中是否有血液,尿量减少,腰背或侧痛,脚或小腿肿胀或异常疲倦或虚弱。
Alprolix副作用
除了所需的作用外,药物还可能引起某些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
如果出现以下任何副作用,请立即与您的医生或护士联系:
罕见
- 从躺着或坐着的姿势突然起床时头晕,头昏或头昏眼花
- 快速,不规则,剧烈震动或心跳或脉搏加快
- 出汗
发病率未知
- 咳嗽
- 呼吸困难
- 荨麻疹,瘙痒或皮疹
- 胸部,腹股沟或腿部特别是小腿疼痛
- 眼睑或眼睛,面部,嘴唇或舌头周围浮肿或肿胀
- 严重,突然头痛
- 言语不清
- 突然失去协调
- 手臂或腿突然,严重的虚弱或麻木
- 胸闷或疼痛
- 视力改变
可能会发生一些通常不需要医疗的副作用。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
不常见
- 头痛
罕见
- 口腔灼痛,发痒,麻木,点刺或刺痛感
- 口味变化或丧失
- 注射部位疼痛
未列出的其他副作用也可能在某些患者中发生。如果您发现任何其他影响,请咨询您的医疗保健专业人员。
打电话给您的医生,征求有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。
注意:本文档包含有关凝血因子ix的副作用信息。此页面上列出的某些剂型可能不适用于Alprolix品牌。
对于消费者
适用于凝血因子:溶液用静脉粉
需要立即就医的副作用
凝血因子ix(Alprolix中包含的活性成分)及其所需的作用可能会引起一些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
服用凝血因子ix时,请立即与您的医生或护士联系,看是否有以下任何副作用:
发病率未知
- 焦虑
- 模糊的视野
- 灼烧,爬行,发痒,麻木,刺,“针刺”或刺痛感
- 胸痛
- 混乱
- 咳嗽
- 呼吸困难或劳累
- 吞咽困难
- 头晕或头晕
- 从躺着或坐着的姿势突然起床时头晕,晕眩或头晕
- 晕倒
- 快速的心跳
- 荨麻疹,瘙痒或皮疹
- 面部,眼睑,嘴唇,舌头,喉咙,手,腿,脚或性器官上的大型蜂巢状肿胀
- 恶心
- 胸部,腹股沟或腿部疼痛,尤其是腿部小腿疼痛
- 眼睑或眼睛,面部,嘴唇或舌头周围浮肿或肿胀
- 躁动
- 突然发作的严重头痛
- 突然失去协调
- 无明显原因突然呼吸急促
- 突然出现口齿不清
- 突然呼吸急促或呼吸困难
- 突然的视力改变
- 出汗
- 患处有压痛,疼痛,肿胀,发热,皮肤变色和明显的浅表静脉
- 胸闷
- 不寻常的嗜睡,迟钝,疲倦,虚弱或呆滞感
- 异常疲倦或虚弱
- 呕吐
不需要立即就医的副作用
可能会发生凝血因子ix的某些副作用,这些副作用通常不需要医疗。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。
请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
不常见
- 口味变化
- 味觉丧失
- 头痛
- 手臂或腿部疼痛
对于医疗保健专业人员
适用于凝血因子ix:静脉药盒,静脉注射粉剂
过敏症
未报告频率:超敏反应(包括支气管痉挛反应和/或低血压,过敏反应,开发高滴度抑制剂需要其他治疗) [参考]
血液学
常见(1%至10%):抑制因子IX [参考]
胃肠道
常见(1%至10%):恶心,呕吐[Ref]
皮肤科
常见(1%至10%):皮疹瘙痒,荨麻疹[参考]
本地
常见(1%至10%):注射部位不适,注射部位疼痛[Ref]
神经系统
常见(1%至10%):头痛,消化不良,嗜睡,头晕,摇晃,嗜睡[Ref]
呼吸道
常见(1%至10%):干咳,低氧,胸闷,呼吸困难[参考]
肾的
治疗出血发作后12天,C型肝炎抗体阳性的患者发生肾梗塞。梗塞与该药物先前给药的关系尚不确定。 [参考]
常见(1%至10%):肾梗死[参考]
眼科
常见(1%至10%):视物模糊[参考]
免疫学的
常见(1%至10%):流行性感冒,注射部位蜂窝组织炎,注射部位静脉炎[Ref]
精神科
常见(1%至10%):冷漠,沮丧[Ref]
其他
常见(1%至10%):血友病(缺乏疗效),乏力,发烧,发冷[参考]
心血管的
常见(1%至10%):冲洗[参考]
参考文献
1.“产品信息。BeneFIX(凝血因子IX)。”惠氏实验室,宾夕法尼亚州费城。
2.“产品信息。毒性(凝血因子IX)。” Cangene bioPharma,Inc.,马里兰州巴尔的摩。
某些副作用可能没有报道。您可以将其报告给FDA。
常规预防
- 推荐的起始治疗方案为每周一次50 IU / kg,或每10天一次100 IU / kg。
- 根据个人反应调整给药方案。
重组
- 重组过程中,请使用无菌技术(清洁且无菌)和平坦的工作表面。
- 使用前,让小瓶的ALPROLIX和预填充的稀释液注射器达到室温。
- 从小瓶上取下塑料盖,然后用酒精擦拭小瓶的橡胶塞。让橡胶塞干燥。
剥去盖子,从样品瓶适配器包装中完全取下衬板。不要从包装中取出样品瓶适配器,也不要触摸适配器包装的内部。
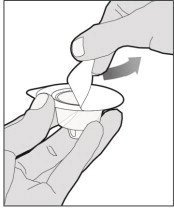
将样品瓶放在平坦的表面上,并用一只手保持样品瓶稳定。用另一只手将样品瓶适配器放在样品瓶上。将转接器长钉直接放在橡胶塞子的中心上方,然后向下垂直推适配器,直到长钉刺穿小瓶塞子的中心并完全插入。

提起包装盖,使其脱离样品瓶适配器,并丢弃该盖。
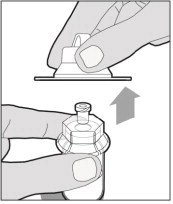
将柱塞杆固定在圆盘上。将柱塞杆的尖端放入注射器的末端。顺时针旋转,直到牢固连接。仅使用ALPROLIX包装中提供的稀释剂注射器。
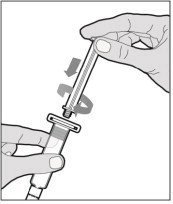
- 用一只手将稀释剂注射器紧紧握住盖子下方的隆起部分,使盖子朝上。如果盖子已卸下或未牢固安装,请勿使用。
- 用另一只手抓住盖子,并以90°的角度弯曲盖子,直至其折断。松开瓶盖后,您将看到注射器的玻璃尖端。请勿触摸注射器的玻璃尖端或瓶盖内部。
- 将样品瓶放在平坦的表面上,将注射器的尖端插入适配器的开口中。顺时针旋转注射器,直到将其牢固地连接到适配器上。
- 慢慢按下柱塞杆,将所有稀释剂注入样品瓶中。在此过程之后,柱塞杆可能会稍微上升。这很正常。
- 在注射器仍连接到适配器的情况下,轻轻旋转小瓶,直到产品完全溶解。最终溶液应澄清至微乳白色和无色。不要摇晃。如果重组的ALPROLIX包含可见的颗粒或浑浊,请勿使用。
- 确保柱塞杆完全按下。将小瓶颠倒。慢慢拉动柱塞杆,将溶液吸入注射器。注意不要将柱塞杆从注射器中完全拉出。
- 轻轻地从小瓶适配器上拧下注射器,并在仍然连接适配器的情况下处置小瓶。请勿触摸注射器尖端或盖子内部。
- 尽快使用重组后的ALPROLIX,但重建后不得迟于3个小时。避免阳光直射。复原后请勿冷藏。
要在上述步骤12之后合并两个或多个ALPROLIX小瓶,请遵循以下合并步骤:
- 逆时针旋转直到完全分离为止,从小瓶适配器上卸下稀释剂注射器。在准备将大型鲁尔锁注射器连接到下一个样品瓶(已连接样品瓶适配器)之前,请勿卸下稀释剂注射器或大型鲁尔锁注射器。
- 将小瓶适配器留在小瓶上,这是连接大型鲁尔锁注射器所需要的。
- 顺时针旋转直到其固定到位,连接一个单独的大型鲁尔锁注射器。
- 慢慢拉动柱塞杆,将溶液吸入注射器。
- 对每个小瓶重复此合并过程,以获得所需剂量。收集所需剂量后,请使用大型鲁尔锁注射器进行给药。
行政
仅用于静脉注射
- 给药前,目视检查重组后的ALPROLIX溶液是否有颗粒物质和变色。如果发现有颗粒物或变色,请勿使用。
- 请勿将重组的ALPROLIX与其他药物放在同一管道或容器中使用。
管理步骤:
- 顺时针旋转直到将其牢固固定到位,将注射器连接到输液器软管的连接器端。
- 压下柱塞,直到从注射器中清除所有空气,并且ALPROLIX到达输液器导管的末端。请勿将ALPROLIX穿过针头。
- 从输液器管路上取下针头保护罩。
- 进行静脉推注。给药速率应由患者的舒适度决定,且不要超过每分钟10毫升。
输注ALPROLIX后,取出并正确丢弃输液器。
Alprolix的适应症和用法
Alprolix,凝血因子IX(重组),Fc融合蛋白,是重组DNA衍生的凝血因子IX浓缩物,适用于血友病B(先天性因子IX缺乏症)的成人和儿童,用于:
- 按需治疗和控制出血发作,
- 围手术期出血
- 常规预防可减少出血发作的频率。
使用限制
Alprolix不能用于诱导B型血友病患者的免疫耐受[见警告和注意事项( 5.3 )]。
Alprolix剂量和给药
仅在重建后静脉内使用
剂量指导
- 在经验丰富的B型血友病治疗专业人员的监督下开始使用Alprolix进行治疗。
- 治疗的剂量和持续时间取决于IX因子缺乏症的严重程度,出血的部位和程度以及患者的临床状况。
- 患者的药代动力学(例如半衰期,体内恢复)和临床反应可能有所不同。 Alprolix的剂量和频率取决于个体的临床反应。 Alprolix的每个小瓶标签均以国际单位(IU)表示了IX因子的效价。 Alprolix药效是使用基于体外,活化的部分凝血活酶时间(aPTT)的一阶段凝血测定法进行分配的,该测定法已针对世界卫生组织(WHO)IX因子浓缩物国际标准进行了校准。
- 临床实验室中的IX因子活性测量可能会受到所用aPTT试剂类型或实验室标准的影响。[请参阅警告和注意事项( 5.4 )]
每千克体重1 IU Alprolix可将因子IX的循环水平提高1%[IU / dL]。使用以下公式,以IU / dL(或正常值的百分比)估算因子IX水平所需的剂量或预期的体内峰值增加:
| IU / dL(或正常百分比)= |
| [总剂量(IU)/体重(kg)] x恢复(IU / dL / IU / kg) |
| 要么 |
| 剂量(IU)= |
| 体重(kg)x所需的IX因子升高值(IU / dL或 |
| 正常值的百分比)x恢复的倒数(IU / kg / IU / dL) |
- 在12岁以下的小儿患者中可能需要调整剂量[参见在特定人群中使用( 8.4 )]。对于12岁以上的患者,通常不需要调整剂量。
按需治疗和控制出血发作
表1提供了按需治疗和控制出血发作的Alprolix剂量。
| 出血类型 | 循环因子IX水平 必需(IU / dL 或正常百分比) | 加药间隔(小时) |
|---|---|---|
| 中小 例如:无并发症的海藻糖,无神经血管损害的浅表肌肉(肌除外),浅表软组织,粘膜 | 30-60 | 如果有进一步的出血迹象,请每48小时重复一次 |
| 重大的 例如:I足类动物和深部肌肉伴有神经血管损伤或大量失血;咽,咽后,腹膜后,中枢神经系统 | 80-100 | 在6-10小时后考虑重复剂量,然后在头3天中每24小时重复一次。 由于Alprolix的半衰期较长,因此在第3天后剂量可以减少,给药频率可以延长至每48小时或更长时间,直到出血停止并达到治愈为止。 |
围手术期管理
表2提供了围手术期管理的Alprolix剂量。
| 手术类型 | 要求的循环因子IX水平(IU / dL或正常值的%) | 加药间隔(小时) |
|---|---|---|
| 次要 (包括简单的拔牙) | 50至80 | 一次输注就足够了。 24-48小时后根据需要重复,直到出血停止并治愈为止。 |
| 重大的 | 60至100(初始水平) | 在6-10小时后考虑重复剂量,然后在头3天中每24小时重复一次。 由于Alprolix的半衰期长,可以减少剂量,并且在术后第3天的服药频率可以延长至每48小时或更长时间,直到出血停止并达到治愈为止。 |
常规预防
- 推荐的起始治疗方案为每周一次50 IU / kg,或每10天一次100 IU / kg。
- 根据个人反应调整给药方案。
重组
- 重组过程中,请使用无菌技术(清洁且无菌)和平坦的工作表面。
- 使用前,让Alprolix小瓶和预填充的稀释剂注射器达到室温。
- 从小瓶上取下塑料盖,然后用酒精擦拭小瓶的橡胶塞。让橡胶塞干燥。
剥去盖子,从样品瓶适配器包装中完全取下衬板。不要从包装中取出样品瓶适配器,也不要触摸适配器包装的内部。

将样品瓶放在平坦的表面上,并用一只手保持样品瓶稳定。用另一只手将样品瓶适配器放在样品瓶上。将转接器长钉直接放在橡胶塞子的中心上方,然后向下垂直推适配器,直到长钉刺穿小瓶塞子的中心并完全插入。

提起包装盖,使其脱离样品瓶适配器,并丢弃该盖。

将柱塞杆固定在圆盘上。将柱塞杆的尖端放入注射器的末端。顺时针旋转,直到牢固连接。仅使用Alprolix包装中提供的稀释剂注射器。

- 用一只手将稀释剂注射器紧紧握住盖子下方的隆起部分,使盖子朝上。如果盖子已卸下或未牢固安装,请勿使用。
- 用另一只手抓住盖子,并以90°的角度弯曲盖子,直至其折断。松开瓶盖后,您将看到注射器的玻璃尖端。请勿触摸注射器的玻璃尖端或瓶盖内部。
- 将样品瓶放在平坦的表面上,将注射器的尖端插入适配器的开口中。顺时针旋转注射器,直到将其牢固地连接到适配器上。
- 慢慢按下柱塞杆,将所有稀释剂注入样品瓶中。在此过程之后,柱塞杆可能会稍微上升。这很正常。
- 在注射器仍连接到适配器的情况下,轻轻旋转小瓶,直到产品完全溶解。最终溶液应澄清至微乳白色和无色。不要摇晃。如果重组的Alprolix含有可见的颗粒或浑浊,请勿使用。
- 确保柱塞杆完全按下。将小瓶颠倒。慢慢拉动柱塞杆,将溶液吸入注射器。注意不要将柱塞杆从注射器中完全拉出。
- 轻轻地从小瓶适配器上拧下注射器,并在仍然连接适配器的情况下处置小瓶。请勿触摸注射器尖端或盖子内部。
- 尽快使用重组后的Alprolix,但重建后不得迟于3小时。避免阳光直射。复原后请勿冷藏。
要在上述步骤12之后合并两个或多个Alprolix小瓶,请遵循以下合并步骤:
- 逆时针旋转直到完全分离为止,从小瓶适配器上卸下稀释剂注射器。在准备将大型鲁尔锁注射器连接到下一个样品瓶(已连接样品瓶适配器)之前,请勿卸下稀释剂注射器或大型鲁尔锁注射器。
- 将小瓶适配器留在小瓶上,这是连接大型鲁尔锁注射器所需要的。
- 顺时针旋转直到其固定到位,连接一个单独的大型鲁尔锁注射器。
- 慢慢拉动柱塞杆,将溶液吸入注射器。
- 对每个小瓶重复此合并过程,以获得所需剂量。收集所需剂量后,请使用大型鲁尔锁注射器进行给药。
行政
仅用于静脉注射
- 给药前肉眼检查重构的Alprolix溶液中是否有颗粒物和变色。如果发现有颗粒物或变色,请勿使用。
- 请勿将重组的Alprolix与其他药物放在同一管道或容器中。
管理步骤:
- 顺时针旋转直到将其牢固固定到位,将注射器连接到输液器软管的连接器端。
- 压下柱塞,直到从注射器中清除所有空气,并且Alprolix到达输液器导管的末端。请勿将Alprolix推入针头。
- 从输液器管路上取下针头保护罩。
- 进行静脉推注。给药速率应由患者的舒适度决定,且不要超过每分钟10毫升。
输注Alprolix后,取出并正确丢弃输液器。
剂型和优势
Alprolix可作为冻干粉在单次使用小瓶中使用,每个小瓶中标称含有250、500、1000、2000、3000或4000国际单位(IU)。在每个Alprolix小瓶上均标明了实际的IX因子效价。
禁忌症
Alprolix禁止用于对产品或其赋形剂(蔗糖,甘露醇,氯化钠,L-组氨酸和聚山梨酯20)有过敏反应(包括过敏反应)的已知病史的人。
。
警告和注意事项
过敏反应
Alprolix已报道过敏反应。已经报道了因子IX替代产品的过敏型超敏反应,包括过敏反应。
抑制剂的存在与因子IX替代疗法(包括Alprolix)的过敏反应有关。评估出现过敏反应的患者是否存在抑制剂。过敏反应的早期迹象可能会发展为过敏反应,可能包括血管性水肿,胸闷,低血压,皮疹,恶心,呕吐,感觉异常,躁动不安,喘息和呼吸困难。如果出现超敏症状,请停止使用Alprolix,并开始适当的治疗。
中和抗体
据报道,在服用Alprolix后,包括先前未治疗的患者,形成了针对因子IX的中和抗体(抑制剂)。定期通过适当的临床观察和实验室检查监测所有患者的抑制剂形成情况[请参阅警告和注意事项( 5.4 )]。
评估出现过敏反应的患者是否存在抑制剂。密切观察患者的急性超敏反应的体征和症状,尤其是在接触该产品的早期阶段。
继用Alprolix攻击后,患有IX因子抑制剂的个体可能有过敏反应的风险增加。
血栓栓塞并发症
凝血因子IX产品的使用与血栓栓塞并发症的发生有关,尤其是在通过中央静脉导管接受连续输注的个人中。 Alprolix应该在数分钟内以推注方式给药[参见剂量和用法( 2.3 )]。尚未研究连续输注Alprolix的安全性。
监控实验室测试
- 为了确认已达到并维持足够的IX因子水平,请通过执行一阶段凝血测定法监测血浆IX因子的活性[参见剂量和用法( 2.1 )]。 IX因子结果可能会受到所用aPTT试剂类型的影响。使用基于高岭土的aPTT试剂进行的一级凝血测定法进行的测量可能会导致活性水平的低估。
- 如果未达到血浆中预期的IX因子活性水平,或者使用推荐剂量的Alprolix无法控制出血,请监测IX因子抑制剂的发展情况。执行Bethesda分析以确定是否存在因子IX抑制剂。
不良反应
临床试验中报告的常见不良反应(发生率≥1%)为头痛和口腔感觉异常。
临床试验经验
由于临床试验是在广泛不同的条件下进行的,因此无法将在某种药物的临床试验中观察到的不良反应率直接与另一种药物在临床试验中观察到的不良反应率进行比较,并且可能无法反映在临床实践中观察到的不良反应率。
在Alprolix的多中心,前瞻性,开放标签的临床试验中,对123位先前接受治疗的患者(PTP,暴露于含有IX因子的产品≥100暴露天)进行了评估,其中115位患者接受了至少26周的治疗和56位患者受试者接受了至少52周的治疗。
据报道,在接受常规预防或按需(按需)治疗的119名受试者中,有10名(AR)发生了不良反应(8.4%)。它们汇总在表3中。
由于不良反应,没有受试者退出试验。在该试验中,未检测到抑制剂,也未报告过敏反应事件。
* 119名接受常规治疗或按需(按需)治疗的先前接受治疗的患者(PTP) | ||
| 系统器官分类 | 不良反应(AR) | 学科数(%) N = 119 * |
| 神经系统疾病 | 头痛 头晕 味觉障碍 | 2(1.7) 1(0.8) 1(0.8) |
| 胃肠道疾病 | 口服感觉异常 呼吸异味 | 2(1.7) 1(0.8) |
| 一般疾病和给药部位情况 | 疲劳 输液部位疼痛 | 1(0.8) 1(0.8) |
| 心脏疾病 | 心pit | 1(0.8) |
| 肾脏和泌尿系统疾病 | 阻塞性尿毒症 | 1(0.8) |
| 血管疾病 | 低血压 | 1(0.8) |
据报道,一名血尿患者阻塞尿路,该尿尿在尿液收集系统中形成阻塞血块。该事件通过水合作用解决,并且受试者继续用Alprolix进行预防性治疗。血栓形成与Alprolix的因果关系尚未建立。
免疫原性
监测参加临床试验的先前治疗的患者中和因子IX的抗体的情况。没有受试者开发针对因子IX的中和抗体。
对因子IX具有反应性的抗体的检测高度依赖于许多因素,包括测定的灵敏度和特异性,样品处理,样品收集的时间,伴随用药和潜在疾病。
上市后经验
在Alprolix的批准后使用过程中已确认出现以下不良反应。由于这些反应是从不确定大小的人群中自愿报告的,因此并非总是能够可靠地估计其发生频率或建立与药物暴露的因果关系。
血液和淋巴系统疾病:IX因子抑制剂的发展
免疫系统疾病:超敏反应
在特定人群中的使用
怀孕
怀孕类别C
Alprolix尚未进行动物生殖研究。还不知道当给孕妇服用时,Alprolix是否会引起胎儿伤害或会影响生殖能力。仅在明确需要的情况下,才应将Alprolix给予孕妇。
人工与分娩
没有关于因子IX替代疗法对分娩和分娩的影响的信息。仅在潜在利益证明潜在风险合理时使用。
护理母亲
不知道Alprolix是否会排泄到人乳中。由于许多药物是从人乳中排出的,因此如果对哺乳妇女服用Alprolix,应格外小心。
儿科用
已经在12岁及以上的先前接受过治疗的儿科患者中评估了Alprolix的安全性,疗效和药代动力学。青少年不需要调整剂量。
12岁以下的儿童可能具有较高的IX因子体重调整后的清除率,较短的半衰期和较低的康复率。这些患者可能需要更高的每公斤体重剂量或更频繁的给药[见临床药理学( 12.3 )]。
Alprolix在12岁及12岁以上受试者中进行的临床试验以及包括2至5岁的8名受试者在内的儿科试验的中期药代动力学和安全性数据支持了在12岁以下儿童中使用Alprolix。 15名6至11岁的受试者平均暴露21.3周(1.1至45.7周)。 12岁以下受试者的安全性是可以接受的。功效可以从药代动力学数据外推至2岁以下的受试者。 [参见临床药理学( 12.3 )]
老人用
Alprolix的临床研究没有包括足够多的65岁及以上的受试者,以确定他们是否与年轻受试者反应不同。
Alprolix说明
凝血因子IX(重组),Fc融合蛋白[rFIXFc],Alprolix中的活性成分,是一种重组凝血因子IX蛋白,由与人免疫球蛋白G 1 (IgG 1 )的Fc结构域共价连接的人凝血因子IX序列组成。 。 rFIXFc的因子IX部分具有与血浆来源的因子IX的Thr 148等位基因形式相同的一级氨基酸序列,并且具有与内源性因子IX相似的结构和功能特性。 rFIXFc的Fc结构域包含IgG 1的铰链,CH2和CH3区。 rFIXFc包含867个氨基酸,分子量约为98道尔顿。
Alprolix并非源自人血,也不含防腐剂。重组因子IX Fc融合蛋白在人类胚胎肾脏(HEK)细胞系中表达,该细胞系将rFIXFc产生到确定的细胞培养基中,该培养基不含动物或人类来源的蛋白质。 rFIXFc的纯化过程不包括使用单克隆抗体试剂。为了提高病毒的安全性,生产过程还包括两个专用的病毒清除步骤-用于灭活的去污剂处理步骤和用于去除病毒的15 nm过滤步骤。活化的因子IX Fc融合蛋白(FIXaFc)的含量限制为≤0.035摩尔%的FIXaFc / FIXFc。
Alprolix是一种无菌,无热原,无防腐剂的白色至灰白色冻干粉末,呈粉饼状,可与提供的稀释剂进行重组,用于静脉注射。复溶后,溶液外观呈透明至微乳白色,并包含以下赋形剂:蔗糖,甘露醇,氯化钠,L-组氨酸和聚山梨酯20。Alprolix可在一次性小瓶中使用,其中含有标记量的IX因子活性,以国际单位。每个小瓶标称包含250 IU,500 IU,1000 IU,2000 IU 3000或4000 IU。
Alprolix-临床药理学
作用机理
Alprolix是一种重组融合蛋白,可暂时替代有效止血所需的缺失凝血因子IX。 Alprolix含有人IgG 1的Fc区,该区与新生儿Fc受体(FcRn)结合。 FcRn是天然存在的途径的一部分,该途径通过将免疫球蛋白循环回循环并延长其血浆半衰期来延迟溶酶体降解。
药效学
B型血友病是一种出血性疾病,其特征在于缺乏功能性凝血因子IX(FIX),导致活化的部分凝血活酶时间(aPTT)测定法中凝血时间的延长,这是针对因子IX的生物学活性建立的体外测试。 Alprolix的治疗可缩短有效给药期间的aPTT。
药代动力学
在单剂量50 IU / kg静脉输注10分钟后,在22位受试者中评估了Alprolix(rFIXFc)的药代动力学(PK)。 PK参数(表4 )基于通过一阶段凝血测定法测量的血浆FIX活性。给药前和给药后240小时(10天)之前的11个时间点收集用于PK分析的血样。 PK数据表明Alprolix具有延长的循环半衰期。
缩写:IR =增量恢复; AUCinf = FIX活动时间曲线下的面积; T 1/2 =消除半衰期; MRT =平均停留时间; CL =体重调整后的间隙; Vss =体重调整后的稳态分布量,达到1%FIX活性的时间=服药后FIX活性下降至比基线高约1 IU / dL的估计天数 | |
| PK参数 | rFIXFc(50 IU /千克) (N = 22) |
| Cmax(IU / dL) | 46.04(68.3%) |
| AUCinf(h * IU / dL) | 1619.1(26.1%) |
| CL(mL / kg / h) | 3.304(28.4%) |
| 比重(mL / kg) | 327.0(28.2%) |
| 航站楼T 1/2 (h) | 86.52(37.2%) |
| 捷运(h) | 101.96(29.7%) |
| IR(IU / dL / IU / kg) | 1.0154(58.7%) |
| 达到1%FIX活性的时间(d) | 11.489(23.8%) |
如第26周的可比较PK参数所示,Alprolix PK曲线在重复给药后稳定。
在27名受试者中评估了100 IU / kg剂量的Alprolix后的PK参数。对于该子集,平均药物清除率(CL)为2.65(21.7%)mL / kg / h,最大活性(Cmax)为99.89 IU / dL(20.1%),达到1%FIX活性的时间为15.8天( 21.3%)。
小儿和青少年药代动力学
在以前治疗过的患者的开放标签,多中心研究中,确定了青少年(12至17岁)和儿童(2至11岁)的Alprolix(rFIXFc)药代动力学(PK)参数[请参见人口( 8.4 )]。
在11位接受单剂量Alprolix的可评估青少年中,静脉输注10分钟后,评估了药代动力学参数。在给药前以及给药后多达336小时(14天)的多个时间点收集PK样品。在另一项研究中,在接受单剂Alprolix的18位可评估儿童(2至11岁)中静脉输注10分钟后评估了PK参数。在给药前以及给药后长达168小时(7天)的多个时间点收集PK样品。根据血浆FIX活性随时间变化曲线估算Alprolix的PK参数。
表5给出了根据29位2至17岁受试者的儿科数据计算出的PK参数。与成年人相比,12岁以下儿童的增量恢复似乎较低,而体重调整后的清除率似乎较高。这可能导致12岁以下儿童需要每公斤体重剂量和间隔时间调整。 [参见在特定人群中的使用( 8.4 )]
1个PK参数以算术平均值(CV%)表示 | |||
缩写:IR =增量恢复; AUC = FIX活动时间曲线下的面积; T 1/2 =消除半衰期; MRT =平均停留时间; CL =体重调整后的间隙; Vss =体重调整后的稳态分布量 | |||
| PK参数1 | 2至5年 (N = 5) | 6至11岁 (N = 13) | 12至17岁 (N = 11) |
| IR(IU / dL / IU / kg) | 0.5980(15.7%) | 0.7422(29.2%) | 0.8929(36.4%) |
| AUC /剂量(IU·h / dL / IU / kg) | 23.18(15.9%) | 29.38(26.6%) | 30.23(22.2%) |
| T 1/2 (小时) | 66.40(32.1%) | 72.23(23.1%) | 83.59(19.1%) |
| 捷运(h) | 80.52(22.3%) | 84.06(18.6%) | 95.13(19.4%) |
| CL(mL / h / kg) | 4.406(16.8%) | 3.613(25.1%) | 3.483(25.6%) |
| 比重(mL / kg) | 349.0(19.2%) | 303.0(28.5%) | 326.0(24.9%) |
非临床毒理学
致癌,诱变,生育力受损
还没有在动物中进行长期研究以评估Alprolix的致癌潜力,或进行确定Alprolix对遗传毒性或生殖力影响的研究。已完成对Alprolix致癌潜力的评估,尚未发现产品使用引起的致癌风险。
临床研究
在一项多中心,前瞻性,开放标签的临床试验中评估了Alprolix的安全性和有效性,该试验比较了两种预防性治疗方案(每周固定和个性化间隔)与常规(按需)治疗的比较;确定止血药的止血功效;并在接受大外科手术的患者围手术期处理期间确定止血功效。总共对12到71岁的123名严重B型血友病(≤2%内源性FIX活性)的先前治疗的患者(PTP)进行了长达77周的随访。
固定每周间隔治疗组中的63名受试者接受Alprolix进行常规预防,起始剂量为50 IU / kg。调整剂量以将FIX谷值维持在基线以上1%至3%或更高的水平(如临床指示可预防出血)。五十名受试者需要至少一次剂量调整,且剂量调整的中位数为一。研究的总中位剂量为45.2 IU / kg(四分位间距:38.1、53.7)。在过去的6个月中,对至少研究9个月的58名受试者的每周平均剂量为40.7 IU / kg(四分位间距:32.3、54.1)。
个体化间隔臂中的29名受试者接受了每10天100 IU / kg剂量的Alprolix常规预防,并调整了间隔以将FIX谷水平维持在基线以上1%到3%或更高,如临床上表明可以预防流血的。研究的总体中位间隔为12.5天(四分位间距:10.4、13.4)。最近6个月研究的至少9个月的26位受试者的平均间隔为13.8天(四分位间距:10.5、14.0)。
二十七名受试者根据需要接受了Alprolix来治疗发作性(按需)治疗组的出血事件。
12名受试者接受了14种主要外科手术的围手术期管理的Alprolix。大手术定义为任何全身麻醉或不进行全身麻醉的手术程序,其中会穿透或暴露大体腔,或造成身体或生理功能的严重损害。该手臂中的四名受试者未参加其他手臂。
按需治疗和控制出血发作
在固定的每周间隔预防,个体化间隔预防和发作(按需)治疗组中,共有114名受试者观察到总共636次出血事件。治疗出血发作的中位总剂量为46.99 IU / kg(四分位间距:33.33、62.50)。在治疗后8-12小时,受试者记录对每次注射的反应的评估。表6总结了控制出血发作的功效。
| 新出血事件 | (n = 636) |
|---|---|
*极好:突然止痛和/或出血迹象改善;良好:可以明显缓解疼痛和/或改善出血迹象,但可能需要在1-2天内再次注射;中度:可能或轻微的有益作用,需要多次注射;无反应:无改善或恶化。治疗后约8小时评估反应。 | |
| 治疗出血发作的注射次数 | |
| 1次注射 | 575(90.4%) |
| 2次注射 | 44(6.9%) |
| 3次注射 | 17(2.7%) |
| 对第一次注射的反应* | (n = 613) |
| 优秀或好 | 513(83.7%) |
| 中等 | 90(14.7%) |
| 没有反应 | 10(1.6%) |
常规预防
使用负二项式模型,固定周间隔组中受试者的年出血率(ABR)降低83%(76-89%),个性化期间中受试者的年化出血率(ABR)降低87%(80-92%)观察到与常规(按需)治疗组相比,该治疗组。
研究的中位治疗时间为51.4周(范围<1-77)。疗效评估对象中ABR的比较总结于
表7 。
* IQR =四分位间距 | |||
5名受试者(2名在每周固定的预防性固定间隔治疗中,3名在个体化的预防性固定间隔治疗中3名)没有足够的数据包含在疗效分析中。 | |||
| 出血情节病因 | 每周固定预防(N = 61) | 个体化预防间隔(N = 26) | 情景式(按需)(N = 27) |
| 整体ABR (IQR)* | 2.95 (1.01、4.35) | 1.38 (0.00,3.43) | 17.69 (10.77,23.24) |
| 自发ABR(IQR)* | 1.04 (0.00,2.19) | 0.88 (0.00,2.30) | 11.78 (2.62,19.78) |
围手术期管理
在12位受试者中进行了14次主要外科手术,包括5次膝关节置换,腹部手术和复杂的牙科手术。围手术期IX用Alprolix替代仅通过推注输注。没有评估连续输注的安全性。止血由研究人员在手术后24小时进行评估,采用4分制的优,良,中和无评估。在100%的大手术中,止血反应被评为优秀(n = 13)或良好(n = 1)。 13名受试者另外进行了15次小手术。没有任何受试者的血栓并发症的临床证据。
供应/存储和处理方式
供应方式
Alprolix作为套件提供,包括:
- 一个一次性rFIXFc小瓶,
- 一个装有5 mL稀释剂并用柱塞塞和尖端盖密封的预填充注射器,以及
- 一个无菌小瓶适配器(重构装置)。
Alprolix小瓶的标称剂量强度为250、500、1000、2000、3000或4000 IU。在每个rFIXFc小瓶和试剂盒纸箱标签上都标明了用IU表示的实际IX因子效价。 Alprolix包装中使用的组件不含天然橡胶胶乳。
| 强度 | 套件NDC编号 |
|---|---|
| 250 IU | 64406-966-01 |
| 500 IU | 64406-911-01 |
| 1000 IU | 64406-922-01 |
| 2000 IU | 64406-933-01 |
| 3000 IU | 64406-944-01 |
| 4000 IU | 64406-977-01 |
储存和处理
- 将Alprolix存放在原始包装中以防止光照。
- 将Alprolix储存在2°C至8°C(36°F至46°F)下。
- 如果在室温下存放,则在单个6个月内不要超过30°C(86°F)。在纸箱上,记录产品从冷藏柜中取出的日期。在此6个月的期限结束前使用产品或将其丢弃。升温至室温后,请勿将产品放回冰箱。
- 不要冻结。冻结会损坏预填充的稀释剂注射器。
- 请勿在纸箱,小瓶或注射器上印刷的失效日期后使用产品或稀释剂。
- 复原后的产品可以在室温下(不超过30°C(86°F))保存不超过3小时。避免阳光直射。重新配制后3小时内,请丢弃所有未使用的产品。
病人咨询信息
- 劝告患者阅读FDA批准的患者标签(患者信息和使用说明)。
- 建议患者在Alprolix给药后向其医生或保健提供者报告任何不良反应或问题。
- 如果患者缺乏对IX因子疗法的临床反应,建议患者联系其医疗保健提供者或治疗机构进行进一步治疗和/或评估,因为这可能表明抑制剂的发展。
- 告知患者过敏反应的早期迹象(包括荨麻疹,胸闷,喘息,呼吸困难和面部肿胀)和过敏反应。指示患者停止使用该产品,如果出现这些症状,请联系其医疗保健提供者。
- 如果发生血栓栓塞事件,建议患者立即联系其医疗保健提供者或立即去急诊室。
由制造
百健公司
剑桥,MA 02142美国
美国牌照#1697
©Bioverativ 2014-2017。版权所有。
患者信息
Alprolix®/全部” PRO链接才可/
[凝血因子IX(重组),Fc融合蛋白]
请在使用Alprolix之前和每次补充笔芯之前仔细阅读此患者信息,因为可能会有新信息。本患者信息并不能代替您的医疗保健提供者谈论您的医疗状况或治疗。
什么是Alprolix?
Alprolix是一种可注射的药物,用于帮助控制和预防B型血友病患者的出血。B型血友病也被称为先天性因子IX缺乏症。
进行手术时,您的医疗保健提供者可能会给您Alprolix。
谁不应该使用Alprolix?
如果您对Alprolix或Alprolix中的任何其他成分过敏,则不应使用Alprolix。使用Alprolix之前,请告知您的医疗保健提供者您是否对任何IX因子产品有过敏反应。
使用Alprolix之前我应该告诉我的医疗保健提供者什么?
告知您的医疗保健提供者您服用的所有药物,包括所有处方药和非处方药,例如非处方药,补品或草药。
告诉医生您所有的医疗状况,包括以下情况:
- 正在怀孕或打算怀孕。不知道Alprolix是否会伤害未出生的婴儿。
- 正在母乳喂养。不知道Alprolix是否会进入母乳或是否会损害您的宝宝。
- 有人告诉您您有IX因子抑制剂(因为Alprolix可能对您无效)。
我应该如何使用Alprolix?
Alprolix应按照您的医疗保健提供者的指示进行管理。您的医疗保健提供者应就如何进行输液对您进行培训。许多患有B型血友病的人学会自己或在家庭成员的帮助下输注Alprolix。
有关输注Alprolix的说明,请参见使用说明。使用说明中的步骤是使用Alprolix的一般准则。始终遵循医疗保健提供者的任何特定说明。如果您不确定该程序,请询问您的医疗保健提供者。不要使用Alprolix作为连续静脉输液。
如果使用Alprolix后无法控制出血,请立即与您的医疗保健提供者联系。
Alprolix可能有哪些副作用?
Alprolix的常见副作用包括头痛和口中异常感觉。
可能发生过敏反应。如果您有以下任何症状,请致电您的医疗保健提供者或立即获得紧急治疗:荨麻疹,胸闷,喘息,呼吸困难或面部肿胀。
Alprolix可能会增加体内形成异常血凝块的风险,特别是如果您有形成血凝块的危险因素时。如果您有可能出现异常血凝块的症状,请致电您的医疗保健提供者或寻求急诊护理,包括:胸痛,呼吸困难,手臂或腿部意外肿胀,有或没有疼痛或压痛。
您的身体还可以产生抗Alprolix的抗体,称为“抑制剂”,这可能会阻止Alprolix正常工作。您的医疗保健提供者可能需要不时测试您的血液中的抑制剂。
这些并不是Alprolix的所有可能的副作用。
与您的医疗保健提供者讨论任何困扰您或不会消失的副作用。
我应该如何储存Alprolix?
将Alprolix小瓶存储在2°C至8°C(36°F至46°F)下。不要冻结。
Alprolix小瓶也可以在最高30°C(86°F)的室温下保存6个月。
如果您选择在室温下存储Alprolix:
- 在纸箱上注明从冷藏柜中取出产品的日期。
- 在此6个月的期限结束前使用产品或将其丢弃。
- 请勿将产品退回冰箱。
请勿在纸箱,小瓶或注射器上印刷的失效日期后使用产品或稀释剂。
重建后:
- 尽快使用复原后的产品;但是,您可以在30°C(86°F)的室温下将重构的产品保存3个小时。保护再生产品免受阳光直射。重新配制后3小时内,请丢弃所有未使用的产品。
- 如果重新配制的溶液浑浊,含有颗粒或无色,请勿使用Alprolix。
我还应该了解Alprolix吗?
有时出于此处列出以外的目的开出药物。请勿在没有规定的条件下使用Alprolix。即使他人有与您相同的症状,也不要与他人共享Alprolix。
由制造
百健公司
剑桥,MA 02142美国
美国牌照#1697
©Bioverativ 2014-2017。版权所有。
Alprolix™
凝血因子IX(重组),Fc融合蛋白
使用说明
在开始使用Alprolix™之前,以及每次补充时,请阅读使用说明。可能有新的信息。此信息不能代替您与医疗保健提供者谈论您的医疗状况或治疗方法。
您的医疗保健提供者应向您或您的照护者展示首次使用Alprolix™时如何重构和管理Alprolix™。
检查Alprolix™套件上的失效日期。
过期后请勿使用产品。
让Alprolix™小瓶和稀释液达到室温。
请勿使用外部热源,例如将小瓶和/或稀释剂放入热水中。
找到干净,平坦的工作表面,并收集重组和管理Alprolix™所需的所有耗材。
用肥皂和清水洗手。应当使用无菌技术(清洁和无菌)。
您的套件包含:

重构
| 第1步 从Alprolix™小瓶上取下塑料盖。 用酒精布擦拭小瓶的橡胶塞,然后使其干燥。 清洁后,请勿用手触摸橡胶塞或使其接触任何表面。 |  | ||||||||
| 第2步 剥去盖子,从样品瓶适配器包装中完全取下衬板。 不要从包装中取出样品瓶适配器,也不要触摸样品瓶适配器的内部。 |  | ||||||||
| 第三步 将小瓶放在平坦的表面上。 Hold the vial adapter package with one hand and using the other hand, place the vial adapter over the vial. The spike should be placed directly above the center of the rubber stopper. Push the vial adapter straight down until the adapter spike punctures the center of the vial stopper and is fully inserted. |  | ||||||||
| Step 4 提起包装盖,使其脱离样品瓶适配器,并丢弃该盖。 |  | ||||||||
| Step 5 Only use the diluent syringe provided to reconstitute the drug product. 将柱塞杆固定在圆盘上。 将柱塞杆的尖端放入注射器的末端。 Turn in a clockwise motion until it is securely attached. |  | ||||||||
| Step 6 With one hand, hold the diluent syringe right under the cap, and with the cap pointing up. Make sure you are holding the diluent syringe by the ridged part directly under the cap. Do not use if the cap has been removed or is not securely attached. |  | ||||||||
| Step 7 用另一只手抓住盖子,并以90°的角度弯曲盖子,直至其折断。 After the cap snaps off, you will see the glass tip of the syringe. Do not touch the glass tip of the syringe or inside of the cap. | <a 已知总共有2种药物与Alprolix(凝血因子ix)相互作用。
检查互动已知与Alprolix相互作用的药物(凝血因子ix)注意:仅显示通用名称。
Alprolix(凝血因子ix)疾病相互作用与Alprolix(凝血因子ix)有两种疾病相互作用,包括:
药物相互作用分类
药物状态
美国日本医生 Gregory Aaen MD经验:11-20年  Brian Aalbers DO经验:11-20年  Glen Scott DO经验:21年以上  Cecile Becker MD经验:11-20年  Shruti Badhwar DO经验:11-20年  渡邊剛经验:21年以上  村上和成 教授经验:21年以上  中山秀章 教授经验:21年以上  村田朗经验:21年以上  溝上裕士 医院教授经验:21年以上 临床试验
|







