4006 776 356
免费咨询 9:00-18:00
获取国外盐酸盐列型片0.125 mg“ sawai” / pramipexole盐酸片0.5mg“ sawa药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / 盐酸盐列型片0.125 mg“ sawai” / pramipexole盐酸片0.5mg“ sawa
盐酸盐列型片0.125 mg“ sawai” / pramipexole盐酸片0.5mg“ sawa
2013年6月
盐酸盐列型片0.125 mg“ sawai” / pramipexole盐酸片0.5mg“ sawai”
创建或修订年
- ** 2019年8月修订(第七版)
- *修订于2018年3月
日本标准产品分类编号
- 871169
*87119
日本标准产品分类编号,等等。
- 功效或效力额外批准日期(最新)
- *2018年3月
医学分类名称
- 多巴胺手术帕金森氏病治疗剂
- *不安的腿综合症治疗剂
批准,等等
- 销售名称
- 普拉米甲醇盐酸片0.125mg“ sawai”
销售名称代码
- 1169012F1154
批准 /许可号码
- 批准编号
- 22500AMX00061000
- 商标
- 普拉克索型脑氯化物
药品价格标准日期
- 2013年六月
销售日期
- 2013年六月
储蓄,到期日期等
- 储蓄
- 保存并存放剃须室以避免水分
- 截止日期
- 显示在外盒子上
法规类别
- 阳性药物
- 处方药
- 预防措施 - 通过医生等处方使用
作品
- 盐酸盐片0.125 mg“ sawai” :1片剂中含有0.125 mg盐水盐酸盐。
包括毫克硬脂酸盐,硬脂酸盐,Tomolo Chocolate Dick,Hydrox Propillulose和D-Mannitol。
构图与性表
| 药物 | 直径(mm) | 重量(毫克) | 厚度(mm) | 特点 | 识别代码 | 外形 |
| 原始平板电脑 | 6.0 | 大约85 | 2.3 | 白色的 | SW PM1 |  |
- 销售名称
- 普拉米甲醇盐酸片0.5mg“ sawai”
销售名称代码
- 1169012F2150
批准 /许可号码
- 批准编号
- 22500AMX00062000
- 商标
- 普拉克索型脑氯化物
药品价格标准日期
- 2013年六月
销售日期
- 2013年六月
储蓄,到期日期等
- 储蓄
- 保存并存放剃须室以避免水分
- 截止日期
- 显示在外盒子上
法规类别
- 阳性药物
- 处方药
- 预防措施 - 通过医生等处方使用
作品
- 盐酸盐列型片0.5 mg“ sawai” :在1片中含有0.5毫克的脑甲苯盐酸盐。
包括毫克硬脂酸盐,硬脂酸盐,Tomolo Chocolate Dick,Hydrox Propillulose和D-Mannitol。
构图与性表
| 药物 | 直径(mm) | 重量(毫克) | 厚度(mm) | 特点 | 识别代码 | 外形 |
| 用电线锁 | 10.6 x 7.6 | 大约210 | 2.8 | 白色的 | SW PM2 |  |
一般名称
- 盐酸盐盐片
警告- 在某些情况下,可能会看到突然的睡眠和睡眠,而没有前体,并且已经报道了由于突然睡眠等导致车祸的例子,因此可以向患者解释有关这种药物的突然睡眠和象牙。服用这种药物时,请注意不要从事危险的任务,例如驾驶汽车,操作机和高空工作。 (请参阅“重要的基本预防措施”和“副作用”)
|
限制(请勿对下一个患者进行管理)- 1。
- 孕妇或可能怀孕的妇女(动物(大鼠)是前列的毒性测试,这些测试降低了妊娠率,存活率降低以及出生儿童的减少。 (请参阅“孕妇管理,产科妇女,护理妇女等”部分)]
- 2。
- 对该药物成分过敏的患者
|
功效或效果
- 1。
- 帕金森氏病
- 2。
- *高度至高度丰富的弹性腿综合征(下肢未凝结综合症)
与效果相关的使用预防措施
- *应根据国际恢复腿综合征研究小组的诊断标准和严重程度仔细进行诊断腿综合征(下肢不稳定综合征),并且只有在满足标准时才进行。
用法和剂量
- 1. *帕金森氏病
- 通常,对于成年人来说,每天从0.25毫克开始,作为盐盐盐酸盐盐盐盐盐,每天的量为0.5 mg,每周观察进度时,一天的数量每周增加0.5 mg。确定体积(标准1.5至4.5 mg)。如果每日数量小于1.5毫克,则作为盐酸盐酸盐盐水,将其分为两次,将其分为早上晚餐后的3次。应该注意的是,根据年龄和症状,它可以适当地增加或减少,但每天不超过4.5 mg。
- 2. *中度至高度丰富的弹性腿综合征(下肢不敏感综合征)
- 通常,成年人每天睡前2-3小时口服对成年人的口服,每天一次作为盐酸盐酸盐盐盐。给药从每天0.125 mg开始,并且在每天不超过0.75 mg的程度上会增加或减少,但在一周以上的时间间隔增加数量。
与使用和剂量有关的预防措施
- 1. *帕金森氏病
- (1)
- 该药物的给药始于少量,精神症状,胃肠道症状,血压等应充分观察到,并且维护量仔细地增加到维持量(标准的1.5至4.5 mg) 。 (请参阅“护理”,“重要的基本预防措施”,“副作用”部分)
- (2)
- 肾功能障碍患者的给药方法主要在尿液中排泄,因为未经涂抹。如果将此药物用于肾功能障碍患者(肌酐清除率少于50 mL/min),则将给药方法的数量调整为以下给药方法的指南,因为该药物的损失一半将被延长减少了肾脏清除率。仔细地增加肾功能。肾功能障碍患者的最多一天和最大含量应如下。另外,由于透析患者或非常高级的肾功能障碍患者没有足够的用途,因此应在观察病情的同时仔细治疗此类患者。 (请参阅有关“谨慎管理”和“老年人行政”的部分)
- 肌酐清除率(ML/min):肌酐清除率≧50
- 管理方法:每天两次给药1.5毫克小于1.5 mg,1.5 mg或以上1.5 mg或以上1.5毫克或以上,第一天的第一天每天3次:0.125 mg×2次2次至1天: 4.5 mg(1.5(1.5)mg x 3次)
- 肌酐清除率(ml/min):50>肌酐清除率≧20
- 管理方法:每天2次管理1天1天给药:0.125 mg×2次,最高1天:2.25 mg(1.125 mg×2次)
- 肌酐清除率(ml/min):20>肌酐清除率
- 管理方法:每天一次,管理的第一天1天剂量:0.125 mg×1次,最高1天:1.5 mg(1.5 mg×1次)
- 2. *中度至高度丰富的弹性腿综合征(下肢不敏感综合征)
- 特异性不安腿综合征(0.75 mg)每天的最大剂量(0.75 mg)低于帕金森氏病患者,因此在肌酐20 ml/min或更多的患者中不需要体重减轻,但在透析期间。该药物在尚未确定少于20 mL/min的晚期肾功能障碍患者中的有效性和安全性,尚未确定该药物对这些患者的给药被认为考虑治疗的益处和危险。 (请参阅有关“谨慎管理”和“老年人行政”的部分)
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 精神科,妄想或其历史病史的患者[症状可能更有可能加剧或表达。 (请参阅“重要的基本预防措施”,“副作用”部分)
- 2。
- 肾功能障碍的患者[副作用可能更有可能出现,并且该药物主要在尿液中排泄为不变。 (请参阅“与使用和剂量有关的预防措施”的部分,“副作用”)。
- 3。
- 严重的心脏病或有历史史的人[可能更有可能显示副作用。 (请参阅“重要的基本预防措施”,“副作用”部分)
- 四个。
- 低血压患者[症状可能恶化。 (请参阅“重要的基本预防措施”,“副作用”部分)
- 五。
- 老年人(请参阅“老年人行政”部分)
重要的基本预防措施
- 1。
- 报道了由于突然睡眠而导致的车祸的一个例子。一些突然睡眠的病例据报道,他们没有识别出任何前身,例如困倦或过度困倦,或者是在开始管理后的第一次。应仔细向患者解释这种药物的突然睡眠和饥饿,并注意不要从事危险工作,例如驾驶汽车,操作机和高海拔。 (请参阅有关“警告”和“副作用”的部分)
- 2。
- 特别是,在管理的早期阶段,可能会根据暴风雨的低血压(例如头晕,头晕和流浪性)发现症状,因此应从少量和足够的观察结果(例如血压)中施用这种药物。此外,如果表达了这些症状,则根据症状程度采取适当的措施,例如减少或停止给药。 (请参阅有关“副作用”的部分)
- 3。
- 在其他公司进行的临床试验中,当使用plaamipexole盐酸盐与其他抗Packinson(Levodopa,anticholin剂,抗盐酸盐)识别时,很容易表达副作用,例如Dyskinzia,幻觉,混乱等。 。如果出现这些副作用,我们将停止体重减轻或给药,如果看到精神症状,则应考虑抗精神病药的给药。 (请参阅有关“相互作用”和“副作用”的部分)
- 四个。
- **,*在帕金森氏病的患者中,如果需要减肥或取消这种药物,则逐渐减少。突然的体重减轻或取消可能引起恶性综合征。此外,多巴胺受体的快速体重减轻或停用可能会导致药物戒断综合征(具有无情,焦虑,抑郁,疲劳,疲劳,出汗和疼痛等症状)。 (请参阅有关“副作用”的部分)
在患有特定弹性腿综合征的患者中,由于剂量低于帕金森氏病患者,因此不必逐渐减少。 - 五。
- 左旋多巴或多巴胺受体参与者的给药具有病理赌博(尽管社会上的劣势,例如个人生活的崩溃,但在不断重复赌博的状态下),因为性行为损害(例如性行为购买和猖ramp),如果表达了这种症状,则应采取适当的措施,例如停止体重或取消。此外,解释了患者及其家人的这种障碍的症状。
- 6。
- *在腿部不安综合征的患者中,包括这种药物在内的多巴胺受体激动剂的给药可能会增加(夜间症状早于2个小时以上,症状较差,以及其他四肢症状的增加)。被认可,将采取适当的措施,例如停止体重或停药。
相互作用
- 这种药物很少受到肝脏代谢酶P450的代谢,并且主要在尿液中排出,因为它不愉快。
合并用途的注释
(请注意联合使用)
| 毒品名称,等等 | 临床症状 /度量方法 | 机械 /危险因素 |
| 化学替丁氨酸 - 氨塔丁盐酸盐,通过阳离子在肾脏中排泄 | 副作用,例如运动障碍,幻觉等。在这种情况下,减轻了这种药物的重量。 | 在Kation运输系统中排泄的药物的结合可以减少两种药物或任何药物的肾脏管分泌,并且可以降低肾脏清除率。 |
| 镇静剂酒精 | 动作可能会增加。 | 该机制尚不清楚,但是通过将其与该药物一起使用可能会增加作用。 |
| 基于多巴胺拮抗剂基于AGIN的药物buitirofenon的药物metocrplamide donperidon | 该药物的作用可能会削弱。 | 这种药物是多巴胺参与者,并且有风险两种药物的作用在一起使用时可能会竞争。 |
| 抗parkinson levodpa -Colin amanantadine盐酸盐 | 副作用,例如运动障碍,幻觉和混乱可能会增加。 | 影响可能会相互增加。 |
副作用
概述表达状态,副作用
- 该药物不进行调查,以阐明副作用的频率,例如用法调查。
严重的副作用
(频率未知)- 1。
- 睡眠睡眠:在这种情况下,可能会出现突然没有前体的睡眠,因此采取适当的措施,例如减肥,取消药物或取消给药。
- 2。
- 可能会出现堕落,妄想,妄想,克服,混乱:幻觉(主要是视觉),妄想,妄想,克服和混乱,因此在这种情况下,我们将停止体重减轻或需要。采取适当的措施,例如使用抗精神病药。
- 3。
- 抗性尿激素不合格分泌综合征(SIADH) :降低,降压剂,低遗传压力,尿钠排泄增加,高度尿液,抽搐,意识障碍等具有抗尿激素的无支撑性激素综合征综合征(SIADH)。发现异常,应停止管理,并应适当执行对饮水的限制。
- 四个。
- *恶性综合征:在帕金森氏病患者中,可能由于快速减肥或该药物取消而发生恶性综合征。如果您进行足够的观察,发烧,意识,无限期的沉默,高肌肉僵硬,异常运动,吞咽困难,心动过速波动,血压波动,血清CK(CPK)出汗(CPK)等。综合征,应在重新管理后逐渐减少,并采取适当的措施,例如身体冷却和水合。
- 五。
- 水平肌肉融化:肌肉疼痛,无力,CK(CPK)增加,rodal肌肉融化,其特征是血液和尿肌红蛋白的兴起,因此,如果发现异常,则取消并采取适当的措施。还要注意由于水平肌肉融化而引起的急性肾脏疾病的发展。
- 6。
- 肝功能障碍:AST(GOT),ALT(GPT),LDH,γ-GTP,总胆红素等。
另一个副作用
| 未知频率 |
| 高敏性 | 高敏性 |
| 皮肤 | 汗水,皮疹,瘙痒,荨麻疹,网状皮肤斑 |
| 肌肉 /骨骼系统 | CK(CPK)增加,背痛,背痛 |
| 中央 /外周神经系统 | 睡觉,头晕,头晕,头痛,头晕,头晕,感知感知的降低,加剧帕金森氏症,张力增加,舌头瘫痪,过度运动,发声,异常感,晕厥,晕厥,晕厥,晕厥。 |
| 自主神经系统 | 口服干燥,体位性低血压,高血压,唾液增加 |
| 感官器官 | 苦味,眼睛的闪烁,双视,纯净,雾,视力丧失 |
| **精神病神经系统 | 不体,失眠,面条,神经敏感性,情绪 - 胜利,清晨觉醒,Nehke -Sama,指控,徘徊(体重增加),义务(体重增加),强迫,强制性购买,药物戒断综合症)抑郁,疲劳,出汗,疼痛等) ,增加性欲,性欲减少,横冲直撞,疾病,不适当 |
| 消化 | 顽皮,消化不良,便秘,胃部不适,呕吐,腹痛,胃溃疡,胃炎,上腹痛,口腔炎,肠道,肠道,肠道,体重减轻 |
| 肝 | 肝功能异常(AST(GET)增加,ALT(GPT)增加,LDH上升等),γ-GTP增加 |
| 内分泌 | proractin降低,生长激素上升 |
| 代谢 | 血糖上升 |
| 心血管 | 低血压,呼吸症 |
| 泌尿科 | 尿频,尿液蛋白阳性,尿液关闭 |
| 一般全身障碍 | 外围水肿,胸痛,不适,无力,跌倒,口干,疲劳,刺痛手 |
| 呼吸器官 | 由于呼吸,肺炎,打ic |
- 如果出现上述副作用,请根据症状采取适当的措施。
- **注意)如果发生异常,请采取适当的措施,例如恢复给药或在减肥前恢复剂量。
老年人的管理
- 1。
- *在其他公司进行的帕金森氏病患者进行的临床试验中,与65岁及65岁的非老年人相比,已经认识到高表达精神症状(例如幻觉)的趋势。使其在观察时精心管理。如果出现诸如幻觉之类的精神症状,我们应该停止减肥或取消,并采取适当的措施,例如在必要时使用抗精神病药。
- 2。
- 该药物主要在尿液中排出,因为它没有变化,但在老年人中,肾功能通常会降低,因此患者的患者从少量开始给药(每天0.125 mg一次)。在观察病情时仔细管理。
管理孕妇,妇产科妇女等。
- 1。
- 不要为可能怀孕的孕妇或妇女管理。 [我没有孕妇的经验,尚未确定安全。在使用动物(大鼠)的生殖有毒试验中识别以下内容。这是给出的
- (1)
- 胎儿容量和一般生殖能力测试(SEG.I)(2.5 mg/kg)表明,基于血清催乳素浓度降低,妊娠率降低。
- (2)
- 在器官形成期间给药测试(SEG.II)(1.5 mg/kg)中,已经发现基于血清催乳素浓度降低的存活率胎儿数量。
- (3)
- 在围产期和护理阶段(SEG.III)(0.5 mg/kg或更多),已经发现了基于血清催乳素浓度降低的出生儿童的出生。
- 2。
- 避免给母乳喂养的妇女管理,如果您必须进行母乳喂养,请停止母乳喂养。 [据报道,它可以抑制人类中的催乳素分泌,并可能抑制牛奶分泌。在动物实验(大鼠)中,已允许将其转移到牛奶中。这是给出的
给儿童的管理等
- 尚未确定低出生体重,新生儿,婴儿,婴儿或儿童的安全性(没有经验)。
过量
- 1。
- 症状:预计该药物的逾期症状会表达出恶心,呕吐,镇静,运动,幻觉,超人,低血压等。
- 2。
- 治疗:如果您看到精神症状,请考虑使用抗精神病药。此外,我们还考虑一般支持疗法,以及诸如胃清洁,活性炭,输注输注,心电图监测器等的适当措施。无法预期通过血液透析去除。
适用的预防措施
- 在药物时:
- 1。
- PTP包装药物应从PTP纸中取出并教给它。 (据报道,PTP薄板的难度 - 到末期在食管粘膜上有一个尖锐的角,甚至是严重的并发症,例如纵隔炎)。
- 2。
- 打开铝制枕头后,应将其存储以避免轻盈和水分,并指示在服用之前将PTP纸取出(这种药物在光线下特别不稳定)。
其他预防措施
- 在大鼠的大鼠(24个月混合诱饵给药)中,据报道视网膜变性为2 mg/kg/day或更多。但是,据报道,临床试验人类没有认识到含有这种药物和视网膜变性的抗Packinson剂的相关性。
药代动力学
- 生物等效测试○盐酸盐片0.125mg“ sawai”
盐酸葡萄球片0.125毫克的“ sawai”和1片健康的成年男孩(0.125 mg李甲甲苯盐酸盐盐酸盐)。由于对获得的药代动力学参数(AUC,CMAX)的统计分析,证实了两种药物的生物等效性。 1) 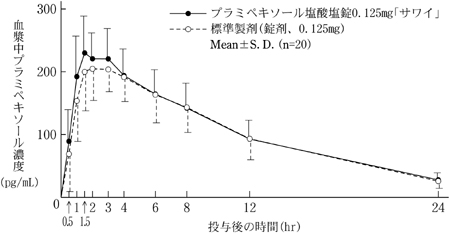
- 血浆浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,体内果汁的时间和时间的时间)而有所不同。
- ○盐酸盐片0.5mg“ sawai”
pramede pexole盐酸剂片0.5 mg“ sawai”基于“生物等效测试指南,针对具有不同含量的口服固体形成(药物和食物检查号1124004)”,“使用0.125 mg“ sawai”时,用作标准制备,洗脱行为,是平等的,被认为是生物学上的。 2)
0.125mg平板电脑1片剂1药代动力学参数
| cmax(pg/ml) | tmax(HR) | T 1/2 (HR) | AUC 0-24hr (pg/hr/ml) |
| 普拉米甲醇盐酸片0.125mg“ sawai” | 251±55 | 2.1±0.9 | 6.8±1.1 | 2597±601 |
| 标准准备(片剂,0.125 mg) | 233±50 | 2.7±1.3 | 6.4±0.9 | 2512±616 |
(平均±SD)
药物
- plamypexol是一种基于非麦角角的多巴胺角色,它表明对多巴胺D 2受体家族具有高亲和力(D 2 ,D 3 ,D 4 )。抗 - parkinson疾病效应通过直接作用于线性突触后膜的D 2受体来表达。
有关活性成分的物理和化学知识
- 通用名称
- 盐酸盐列甲醇水合物
(列二曲羟基水合物) - 化学名称
- ( S )-2-Amino-4,5,6,7-四氢-6-丙氨酸苯甲苯甲酰氮唑二氯化物一水合物
- 分子
- C 10 H 17 N 3 S / 2HCL / H 2 O
- 分子量
- 302.26
- 熔点
- 大约290°C(分解)
- 结构公式
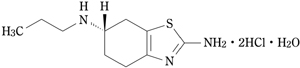
- 特点
- 盐酸盐水水合物是白色至细的黄色晶体或结晶粉。溶解在水中,略微溶于甲醇,略微溶解在乙醇中(95),几乎不溶于四氢铁氟乙醇非常容易。
处理的预防措施
- ・稳定性测试
由于使用PTP包装(PTP纸(带有干燥剂))的加速度测试(40°C 75%RH,6个月),假定它在正常市场分布下稳定3年。 3),4)
包装
- 普拉米甲醇盐酸片0.125mg“ sawai”:
PTP:100片(10片X 10) - 普拉米甲醇盐酸片0.5mg“ sawai”:
PTP:100片(10片X 10)
主要文献和文档请求目的地
主要文献
- 1)
- Takano Kazuhiko,新药和临床实践, 62 (3),530(2013)。
- 2)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 3)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
- 四)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
文学要求
- [请索取以下的主要文件(包括 - 房屋材料)]
Sawai Pharmaceutical Co.,Ltd.制药信息中心 - 532-0003 532-0003 Miyahara,Yodogawa-ku,大阪 - 2-30
- 电话:0120-381-999
- 传真:06-6394-7355
制造商等的姓名或名称和地址等。
- 制造和分销商
- Sawai Pharmaceutical Co.,Ltd。
- 5-130 Miyahara,大阪Yodogawa-ku