4006 776 356
免费咨询 9:00-18:00
获取国外atomokisetin胶囊5mg“ nissho” / atmoxetine胶囊10mg“ nik药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / atomokisetin胶囊5mg“ nissho” / atmoxetine胶囊10mg“ nik
atomokisetin胶囊5mg“ nissho” / atmoxetine胶囊10mg“ nik
2018年12月
atmoxetine胶囊5mg“ nissho” / atmoxetine胶囊10mg“ nissho” / atmoxetine胶囊25 mg“ nissho” / atmoxetine胶囊40mg“ Nissho” Nissho“
创建或修订年
- *修订于2020年2月(第二版)
- 创建于2018年8月
日本标准产品分类编号
- 871179
医学分类名称
- 注意缺陷 /超疾病治疗剂(选择性去甲肾上腺素抑制剂)
批准,等等
- 销售名称
- Atomokisetin胶囊5mg“ Nikko”
销售名称代码
- 1179050M1040
批准 /许可号码
- 批准编号
- 23000AMX00655000
- 欧洲商品名称
- 阿托西汀
药品价格标准日期
- 2018年12月
销售日期
- 2018年12月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在外部盒子上的显示器的到期日期内使用,等等。
法规类别
- 阳性药物
- 处方药
- (注意 - 根据医生的处方等使用)
作品
- 活性成分的名称
- Atmoxetine盐酸盐
- 包括(在1胶囊中)
- 5.71毫克(5mg作为原子苷)
- 添加剂
- 部分α粘胶,二甲基聚乙烷(口服)
胶囊体:黄色322氧化物,硫酸钠钠,明胶
特点
- 表面形状 /色调
- 帽子和身体部分多样化的彩色硬胶囊
- 外形
编号:3- 身体指标
- atmoxetine
5mg
日本医务人员 - 包装代码
 137
137
- 销售名称
- Atomokisetin胶囊10mg“ Nikkyo”
销售名称代码
- 1179050M2046
批准 /许可号码
- 批准编号
- 23000AMX00656000
- 欧洲商品名称
- 阿托西汀
药品价格标准日期
- 2018年12月
销售日期
- 2018年12月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在外部盒子上的显示器的到期日期内使用,等等。
法规类别
- 阳性药物
- 处方药
- (注意 - 根据医生的处方等使用)
作品
- 活性成分的名称
- Atmoxetine盐酸盐
- 包括(在1胶囊中)
- 11.43毫克(10mg作为原子苷)
- 添加剂
- 部分α粘胶,二甲基聚乙烷(口服)
胶囊主体:氧化钛,硫酸钠,明胶
特点
- 表面形状 /色调
- 帽子和身体部分白色不透明硬胶囊
- 外形
编号:3- 身体指标
- atmoxetine
10mg
日本医务人员 - 包装代码
 138
138
- 销售名称
- Atomokisetin胶囊25mg“ Nikkyo”
销售名称代码
- 1179050M3042
批准 /许可号码
- 批准编号
- 23000AMX00657000
- 欧洲商品名称
- 阿托西汀
药品价格标准日期
- 2018年12月
销售日期
- 2018年12月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在外部盒子上的显示器的到期日期内使用,等等。
法规类别
- 阳性药物
- 处方药
- (注意 - 根据医生的处方等使用)
作品
- 活性成分的名称
- Atmoxetine盐酸盐
- 包括(在1胶囊中)
- 28.57毫克(25 mg As atomoxetine)
- 添加剂
- 部分α粘胶,二甲基聚乙烷(口服)
胶囊主体:蓝色2,氧化钛,硫酸钠,明胶
特点
- 表面形状 /色调
- 硬胶囊剂的帽子部分是蓝色不透明的,身体部位不确定
- 外形
编号:3- 身体指标
- atmoxetine
25毫克
日本医务人员 - 包装代码
 139
139
- 销售名称
- Atomokisetin胶囊40mg“ Nikkyo”
销售名称代码
- 1179050M4049
批准 /许可号码
- 批准编号
- 23000AMX00658000
- 欧洲商品名称
- 阿托西汀
药品价格标准日期
- 2018年12月
销售日期
- 2018年12月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在外部盒子上的显示器的到期日期内使用,等等。
法规类别
- 阳性药物
- 处方药
- (注意 - 根据医生的处方等使用)
作品
- 活性成分的名称
- Atmoxetine盐酸盐
- 包括(在1胶囊中)
- 45.71毫克(40mg作为atomokicetin)
- 添加剂
- 部分α粘胶,二甲基聚乙烷(口服)
胶囊主体:蓝色2,氧化钛,硫酸钠,明胶
特点
- 表面形状 /色调
- 帽子和身体部分是蓝色不透明的硬胶囊
- 外形
编号:3- 身体指标
- atmoxetine
40 mg
日本医务人员 - 包装代码
 140
140
一般名称
- Atmoxetine盐酸胶囊
限制(请勿对下一个患者进行管理)- 1。
- 对该药物成分过敏的患者
- 2。
- *Patients within or within 2 weeks after the mao inhibitor (selegilline hydrochloride, lasagirin mesylate, safinamidomesylate) within 2 weeks after canceling
- 3。
- 严重心血管疾病的患者[血压增加或心率增加并恶化症状。请参阅“重要的基本预防措施”和“其他预防措施”部分]
- 四个。
- 据报道,棕色细胞瘤或其病史的患者[据报道血压升高和心率升高。这是给出的
- 五。
- 闭角青光眼患者这是给出的
|
功效或效果
- 注意缺陷/多动症(AD/HD)
与效果相关的使用预防措施
- 1。
- 尚未确定6岁以下患者的疗效和安全性。
- 2。
- AD/HD的诊断应根据标准和已建立的诊断标准仔细进行,例如诊断和统计手册(DSM Note)(DSM Note) ,并且仅在满足标准时才进行。
注意)精神障碍的诊断和统计手册
用法和剂量
- 1. 18岁以下的患者
- 通常,对于18岁以下的患者,他们每天以0.5 mg/kg的速度开始,每天为0.8 mg/kg,每天增加到0.8 mg/kg,每天增加到1.2 mg/kg,每天1.2至1.8 mg /// 。
但是,增加的增加应以超过一周的时间间隔进行,并且剂量每天口服两次。
另外,尽管根据症状适当增加或减少了数量,但每日量不得超过1.8 mg/kg或120 mg的量。 - 2. 18岁以上的患者
- 通常,18岁以上的患者从每天40 mg开始,每天增加到80 mg,每天保持80至120 mg。
但是,每天增加到80毫克的增加应增加一周以上,随后的增加应以2周或更长时间的间隔进行,剂量每天或每天两次分为口服一次。 。
另外,尽管症状适当增加或减少,但每日剂量不超过120 mg。
与使用和剂量有关的预防措施
- 1。
- 服用CYP2D6抑制作用的药物或患者(代谢剂差)的患者(发现在遗传上缺乏CYP2D6活性(Pooor代谢剂))会增加该药物的血液浓度,表明副作用。很容易,应仔细观察和仔细地施用患者的病情,例如,只有在服用时没有问题时增加数量。 [请参阅“互动”部分]
- 2。
- 对于中度肝功能障碍(B类B类)的患者,将开始和维持剂量降低到50%。在严重的肝功能障碍(C Child-Pub C类)的患者中,起始剂量和维持剂量应降低至25%。 [请参阅“谨慎行政”的部分]
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 肝功能障碍的患者[血液浓度可能增加。 (请参阅“与使用和剂量有关的预防措施”部分)]]
- 2。
- 肾功能障碍的患者[血液浓度可能增加。这是给出的
- 3。
- 抽搐性癫痫发作或患有病史的患者[可能引起抽搐。这是给出的
- 四个。
- 心脏病(包括扩展QT)或患者病史[可能恶化或重复症状。这是给出的
- 五。
- 先天性QT扩展综合征或具有QT扩展家族史的患者[可能发生QT扩展。这是给出的
- 6。
- 高血压或患有病史的患者[症状可能恶化或复发。这是给出的
- 7。
- 脑血管疾病或患有病史的患者[症状可能恶化或复发。这是给出的
- 8。
- 具有体位性低血压病史的患者这是给出的
- 9。
- 以下患有精神疾病的患者[行为障碍,思维障碍或躁狂发作可能会恶化。这是给出的
精神疾病,躁郁症 - 十。
- 排尿困难的患者[可能会恶化症状。这是给出的
重要的基本预防措施
- 1。
- 在管理之前,治疗该药物的副作用以及该药物给药的副作用,对这种药物(患者,父母或适当的人)进行治疗的医生或医疗保健专业人员。教授适当的用法。
- 2。
- 在长时间服用该药物时,应定期重新评估有用性,应根据需要设置毒品假期。
- 3。
- 在另一家公司进行的临床试验中,在Atmoxetine的给药下,在儿童的患者中,观察到自杀思维和相关行为,因此接受该药物的患者应仔细观察这些症状的表达。 [请参阅“其他预防措施”部分]
- 四个。
- 在AD/HD中经常观察到攻击和敌意,但据报道,在Ampoxetine给药期间,还报道了侵略性,敌意表达和恶化。在管理过程中,观察积极行动,敌对行动的表达或恶化。 [请参阅“其他预防措施”部分]
- 五。
- 在服用正常精神疾病或躁狂患者原莫西汀的患者中,已经报道了精神病或伪造的症状。如果识别出这种症状的表达,请考虑与该药物有关的可能性。在某些情况下,取消是合适的。
- 6。
- 由于您可能会嗜睡,头晕等,因此请注意不要从事伴随危险汽车(例如驾驶汽车)的机器操作。
- 7。
- 为了观察对心血管系统的影响,请在该药物的预科期之前和期间定期测量血压和心率(脉搏率)。 [请参阅“禁忌症”,“谨慎行政”和“其他预防措施”的部分]
- 8。
- 由于该药物可能会影响血压或心率,因此在为心血管疾病患者施用该药物时,请咨询专门从事心血管的医生,并考虑是否仔细施用。此外,建议这种药物适用于心脏不认真并且由于患者的心脏病病史,猝死或严重心脏病而可能具有可能性的患者。考虑到给药时,请通过心电图评估心血管系统的状况在开始之前的检查。 [请参阅“禁忌症”,“谨慎行政”和“其他预防措施”的部分]
- 9。
- 在施用Atmoxetine的早期,据报道儿童可以减轻体重增加和增长。在给药期间,请注意儿童的生长,如果身高和体重增加不好,请考虑减肥或给药中断。 [请参阅“儿童管理等”部分]
相互作用
- 该药物主要由CYP2D6 CYP2D6代谢。
禁忌症(不要一起使用)
| 毒品名称,等等 | 临床症状 /度量方法 | 机械 /危险因素 | MAO抑制剂Selegirin盐酸盐(F -PEE)
雷萨吉林梅赛酸盐(绣球花)
*saffinamidomomomomemomopomomomemopomopomopomemopomemopomemapate(ekfina) | 两种药物的作用都可以增强。在停用MAO抑制剂后使用该药物时,必须将其间隔超过两个星期。另外,如果在停用该药物后施用MAO抑制剂,则必须将间隔持续两周以上。 | 大脑中的单胺浓度可能会增加。 |
|
合并用途的注释
(请注意联合使用)
| 毒品名称,等等 | 临床症状 /度量方法 | 机械 /危险因素 |
| 硫酸盐核酸盐(全身给药,例如静脉内给药,不包括吸入和给药) | 据报道,心率和血压增加了,因此请小心。 | 它可能会增加对心血管系统的作用。 |
| β受体刺激剂(不包括硫酸沙丁胺醇) | 小心,因为这些药物的心率和血压升高可能会增加。 | 它可能会增加这些药物对心血管系统的作用。 |
| CYP2D6抑制剂帕罗西汀盐酸水合物,等等。 | 由于该药物的血液浓度可能会增加,因此有必要在观察进度的同时花费时间来增加这种药物。 | 由于这些药物的CYP2D6抑制作用,该药物的血液浓度可能会增加。 [请参阅“与使用 /剂量有关的预防措施”部分] |
| 具有增强作用的药物,盐酸多巴胺等。 | 请注意,这些药物可能会增加血压的血压升高。 | 这可能会影响这些药物对血压的作用。 |
影响去甲肾上腺素的药物(侵入盐酸盐等)
选定的5-羟色胺 /去甲肾上腺素的重新IMPORT抑制剂甲基化盐酸,等等。 | 请注意,这些药物的影响可能会得到增强。 | 这些药物对去甲肾上腺素的影响可能会添加或协同作用。 |
副作用
概述表达状态,副作用
- 该药物不进行调查,以阐明副作用的频率,例如用法调查。
严重的副作用
- 1.肝功能障碍,黄疸,肝衰竭(频率未知)
- 肝功能障碍,黄疸和肝功能衰竭可能是由于肝功能检查值的增加而发生的,因此可以充分观察到,如果发现异常,请采取适当的措施,例如停用施用。
- 2.过敏反应(频率未知)
- 可能会出现过敏反应,例如血管水肿和荨麻疹,因此请确保观察它,如果发现异常,请停止给药并采取适当的措施。
另一个副作用
- 如果发现副作用,请根据需要采取适当的措施,例如减肥和暂停给药。
| 未知频率 |
| 消化器官 | 怀旧,食欲减少,腹痛,呕吐,便秘,口干,腹泻,消化不良,口干,干肠干 |
| 精神科 | 头痛,饥饿,浮动的头晕,位置头晕,睡眠障碍,易于刺激,不适,失眠,失眠,清晨觉醒,情绪不断变化,漫步,沮丧,沮丧,幻觉,焦虑,焦虑,感觉,感官和幻觉。侵略,性欲衰落,抽动,凶猛,平静和沮丧 |
| 高敏性 | 所以瘙痒,皮疹,荨麻疹 |
| 心血管 | 心pit,心动过速,血压升高,心率增加,心电图延伸,晕厥,雷诺现象,洪水 |
| 皮肤 | 多汗症,皮炎 |
| 尿 /生殖器 | 难度,勃起功能障碍,生殖器疼痛,尿液闭合,月经障碍,射精障碍,月经不规则,前列腺炎,频繁排尿,勃起疼痛,射精,射精,睾丸疼痛,尿液疼痛,尿水等紧急性,排尿。 |
| 其他的 | 体重减轻,胸痛,胸部刺激,疲劳,热闪光,发冷,风味异常,结膜炎,胸部不适,外周冷却,冷静,凉爽,肌肉收缩,肌肉收缩,尖端 |
老年人的管理
- 尚未确定老年人的疗效和安全性。
管理孕妇,妇产科妇女等。
- 1。
- 对于可能怀孕的孕妇或妇女,只有确定治疗要超过危险。 [尚未确定怀孕期间的管理安全。此外,在动物实验(大鼠)中识别胎盘可传递性。这是给出的
- 2。
- 母乳喂养妇女应避免在这种药物服用期间母乳喂养。 [在动物实验(大鼠)中,已经观察到向牛奶的过渡。这是给出的
给儿童的管理等
- 1。
- 尚未确定低出生体重,新生儿,婴儿和6岁以下的婴儿的有效性和安全性。 [尚未对6岁以下儿童进行检查。这是给出的
- 2。
- 在早期给药中,已经报道了体重增加和生长延迟。 [请参阅“重要的基本预防措施”部分]
过量
- 体征,症状
- 在服用过量时,抽搐,QT延伸,睡眠,兴奋,运动,行为异常,行为异常,消化症状,心动过速,心动过速,头晕,头晕,头晕,vades和增加血压。此外,当触原子和其他药物同时给药时,已经报告了死亡。
- 治疗
- 确保气道,对心脏功能和生命体征进行监测,并提供适当的症状治疗。如有必要,进行胃清洁或活化碳。透析无效,因为该药物的蛋白质组合率很高。
适用的预防措施
- 1.发出药物时
- PTP包装药物应从PTP纸中取出并教给它。 (据报道,PTP纸的硬尖角插入食管粘膜中,然后引起严重的并发症,例如纵隔炎)。
- 2。
- 由于刺激的眼球,请打开胶囊并指示不要服用。如果胶囊含量粘附在眼球上,请立即用水洗涤并教咨询医生。此外,应用水和其他可能粘附的地方洗涤指导。
其他预防措施
- 1。
- 在对外国儿童和青少年的Plasebo对照简短测试的合并分析中(11例AD/HD患者的11次检查和1例尿病患者的测试),据报道,Plasebo管理组的Atmoxetine早期给药,据报道自杀思想的风险很大(Atmoxetine给药组5/1357(0.37%),安慰剂给药组0/851(0%))。这些考试中没有加速的例子。还据报道,外国报告称,AD/HD中的精神病与自杀思维有关,并增加了自杀行为的风险。
- 2。
- 在控制外国儿童和青少年短期测试的安慰剂的组合分析中(AD/HD患者的11个测试),侵略性行为和敌对表达率为21/1308(1.6%),Plasebo给药组。它是9 /806(1.1%)。在对日本和国外成年人的安慰剂控制短期测试的合并分析中(AD/HD患者的9个测试),侵略性行为和敌意的速度是阿托莫西汀行政部门6/1697(0.35%),即0.35% Plasebo给药组为4/1560(0.26%)。
- 3。
- 据报道,在日本和海外临床试验数据中,发现5.9%至11.6%的儿童和成年人的血压升高(合同期为20 mmHg或更多,扩张期为15 mmHg或更高)或心率增加(20 bpm或更多)。 (请参阅“禁忌有”,“谨慎行政”和“重要的基本预防措施”的部分)
- 四个。
- 在年轻的大鼠中重复大约75天的Atmoxetine 1,10和50 mg/kg,但性成熟度略有延迟,在10 mg/kg或以上的睾丸体重减轻,尽管有睾丸的重量精子减少,但对性成熟后的生殖能力和概念没有影响。由大鼠引起的这些变化是温和的,但是与AUC相比,当时的血浆浓度(AUC)为1 mg/kg,最高0.2倍,这是最大的临床剂量(1.8 mg/kg)。正常活动,EM)或0.02次(CYP2D6默认值,PM),10 mg/kg高达1.9次(EM)或0.2次(PM),并且没有临床剂量的安全性。在研究外国儿童和青少年对次生性别的影响的临床试验中,没有提出对阿托莫基汀的性成熟的影响。
- 五。
- 在口服怀孕兔子形成的三个检查中,最大剂量为100 mg/kg,生存胎儿体的数量,早期吸收性胚胎的增加,异常宫颈动脉和亚热视动脉缺陷。尽管表达速率略有增加,但这些变化在背景数据的范围内。在这种剂量中,与AUC(1.8 mg/kg)的最大临床剂量(1.8 mg/kg)相比,产妇毒性(例如轻度体重增加和降低)是2.6倍。 )。此外,这些发现对三项考试中的一项认可,并且尚未清楚阿诺西汀给药和人类外包的相关性。
药代动力学
- 生物当量测试
- (1) atmoxetine胶囊5mg“ Nikkyo”
- Atmoxetine Capsule 5mg“ Nikkyo”基于“具有不同内容的口服固体公式的生物形式形式的正式正式测试指南(2012年2月29日,2012年2月29日,药品和食品检查0229 No. 10)”,Atmoxetetin cagkyo 10mg” Nikkyo” Nikkyo何时工作。用作标准制剂,洗脱行为相等,被认为是生物学的。 1)
- (2) atmoxetine胶囊10mg“ nissho”
- Atmosoxetine胶囊10 mg“ Nikkono”和标准制剂(10 mg AS Atomoxetine)每个胶囊(10毫克作为阿托莫西汀)健康的成年男性被施用,以快速食用单个口腔轨道,以测量血浆中阿托莫西汀的恐吓。由于AUC和CMAX的统计分析)在90%的置信区法律下,它在log(0.80)到log(1.25)的范围内,并确认了两种药物的生物等效性。 2)
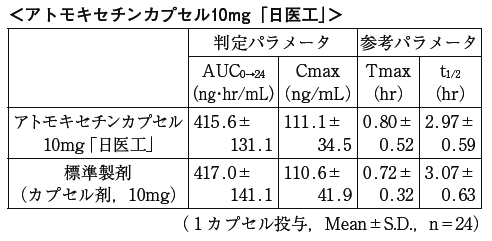
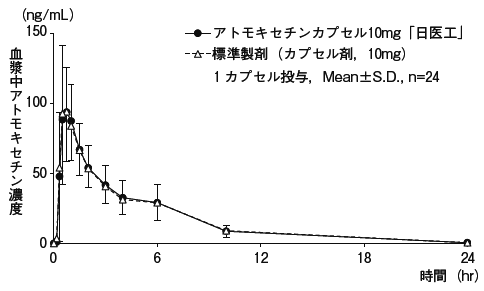
血浆浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,幼年的时间数量等)而有所不同。 - (3) Atmoxetine胶囊25mg“ Nikkyo”
- Atmoxetine Capsule 25mg“ Nikkyo”基于“生物外的形式形式的口服固体配方的形式式配方,其含量不同(2002年2月29日,2012年2月29日,2012年2月29日,制药和食品评论0229 No. 10)”,Atmosoxetin capsule 40mg” Nisshin Medical时这项工作被用作标准准备,洗脱行为相等,被认为是生物学的。 3)
- (4) Atmoxetine胶囊40mg“ Nissho Medicine”
- Atmosoxetine胶囊40毫克的“ Nikyaku”和标准制剂是通过交叉方法和药物对象(这是健康成年男子的消耗轨道器官)的一个胶囊(40 mg As aromoxetine),测量Arrostro的轨道器官,测量rharostro的rhinoxetine浓度根据90%置信区定律的统计分析,测量了Arromoxetine的浓度。由于AUC和CMAX的统计分析,它在log(0.80)到log(1.25)的范围内,并确认了两种药物的生物等效性。 2)
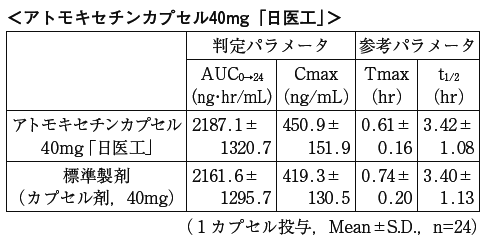
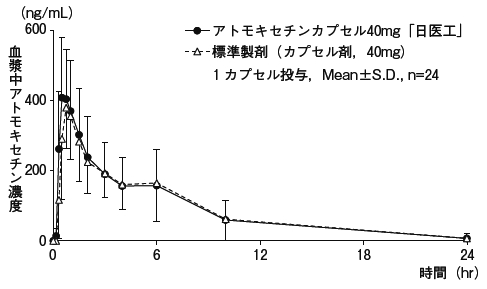
血浆浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,幼年的时间数量等)而有所不同。
药物
- 据信,脑皮质水平与脑皮质水平的控制有关,Atmoxetine选择性地抑制去甲肾上腺素的聚会,去甲肾上腺素的团聚,该聚会是神经突触间隙中的神经递质,选择性地抑制了抗-Adhd。影响。 4),5)
有关活性成分的物理和化学知识
- 通用名称
- 原子苷羟基甲基(原子苷氢智)
- 化学名称
- (3 r ) -n-甲基-3-(2-甲基苯氧基)-3-苯基丙烷-1-氨基单胺单氯化物
- 结构公式
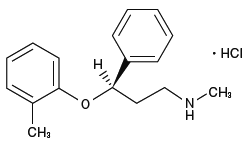
- 分子
- C 17 H 21否 / HCl
- 分子量
- 291.82
- 性欲
- 这是白色粉末。
很容易溶解在二甲基亚氧化二甲醇中,稍微溶于乙醇(99.5),并且溶解在水中略有少量。
处理的预防措施
- 稳定性测试
- 由于该产品的加速测试(40°C,相对湿度75%,6个月),5 mg的原子苷胶囊,阿托莫西汀胶囊10 mg,蛋白苷酸胶囊,阿托莫西汀胶囊,25 mg atomoxetetine capsules和25 mg atomoxetine Capsules和Atomoxetetine Capsules 40 mg“ 40 mg” 40 mg“ 40 mg” “据推测,在正常市场分布下,“ Nikkai”稳定了三年。 6)
包装
- Atomokisetin胶囊5mg“ Nikko”
140个胶囊(14个胶囊X 10; PTP) - Atomokisetin胶囊10mg“ Nikkyo”
140个胶囊(14个胶囊X 10; PTP) - Atomokisetin胶囊25mg“ Nikkyo”
140个胶囊(14个胶囊X 10; PTP) - Atomokisetin胶囊40mg“ Nikkyo”
140个胶囊(14个胶囊X 10; PTP)
主要文献和文档请求目的地
主要文献
- 1)
- Nisshin II Co.,Ltd。in -House Materials:生物当量测试(5mg)
- 2)
- Kamiya Arihuhisa等人:医疗与药房,75(9),1061(2018)
- 3)
- Nisshin III Co.,Ltd。in -House Materials:生物等效测试(25mg)
- 四)
- Goodman Gilman Pharmaceutical Book(上)药物治疗和第12临床第12版373,Hirokawa Shoten,2013年
- 五)
- Goodman Gilman Pharmaceutical Books(Upper)药物治疗的基础知识和临床实践中的第十二章495,Hirokawa Shoten,2013年
- 6)
- Nisshin II Co.,Ltd。在房屋材料中:稳定性测试
文学要求
- 请索取下面“主文档”列中描述的文档和房屋材料。
Nissin II Corporation客户支持中心 - 〒930-8583工会城索戈学院1-6th 21
- 免费拨号(0120)517-215
- 传真(076)442-8948
制造商等的姓名或名称和地址等。
- 制造和分销商
- Nisshin II公司
- 富山城市sora chang 1-6-6 21
137
138
139
140