4006 776 356
免费咨询 9:00-18:00
获取国外抗逆境果仁酰胺片3mg nipro / soburazole片6mg niprolt药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / 抗逆境果仁酰胺片3mg nipro / soburazole片6mg niprolt
抗逆境果仁酰胺片3mg nipro / soburazole片6mg niprolt
2017年6月
抗乳果片3mg“ nipro” / alipipurazole片剂6mg“ nipro” / apiprazole 12 mg“ nipro” nipro“ / alipiprazole 1%” nipro“ / alipipurazole” / alipipurazole OD片剂3mg“ nipro” nipro“ nipro” / alipipurazole od dipiproaz 6mg od plaz nipro od plaz nipro'nipro'nipro'nipro'nipro''nipro'' / al'nipro'' nipro“ / apipyprazole OD片剂24mg“ nipro”
创建或修订年
- **于2021年7月修订(第七版)
- *修订于2020年11月
日本标准产品分类编号
- 871179
日本标准产品分类编号,等等。
- 功效或效力额外批准日期(最新)
- 2020年7月
医学分类名称
- 抗精神病药
批准,等等
- 销售名称
- 阿利皮拉唑片3mg“ nipro”
销售名称代码
- 1179045F1112
批准 /许可号码
- 批准编号
- 22900AMX00221
- 商标
- Aripiprazole片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- 阿利皮拉唑3mg
- 添加剂
- 乳糖氢纤维素,玉米纤维素,晶体纤维素,羟基丙糖,硬脂酸镁,蓝色2
特点
- 产品性能外形

- 形状
- 米片
- 尺寸
- 6.0mm
- 厚度
- 2.5mm
- 重量
- 95mg
- 身体指标
- 阿立卜拉唑3/3尼普罗
- 销售名称
- α-拉唑6mg“ nipro”
销售名称代码
- 1179045F2119
批准 /许可号码
- 批准编号
- 22900AMX00222
- 商标
- Aripiprazole片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- α6mg的α
- 添加剂
- 乳糖水合物,玉米纤维素,羟基耐糖,硬脂酸镁
特点
- 产品性能外形



- 形状
- 白色裸锁
- 尺寸
- 7.0mm
- 厚度
- 2.7mm
- 重量
- 135mg
- 身体指标
- 抗氯唑6尼普罗
- 销售名称
- 甲状腺脂肪片12mg“ nipro”
销售名称代码
- 1179045F3115
批准 /许可号码
- 批准编号
- 22900AMX00223
- 商标
- Aripiprazole片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- 阿利皮拉唑12mg
- 添加剂
- 乳糖水合物,玉米纤维素,羟基尿素,硬脂酸镁,黄色322氧化物
特点
- 产品性能外形



- 形状
- 黄色平板电脑
- 尺寸
- 8.0mm
- 厚度
- 2.8mm
- 重量
- 180毫克
- 身体指标
- 阿立比12尼普罗
- 销售名称
- 阿立卜拉唑1%“ nipro”
销售名称代码
- 1179045B1072
批准 /许可号码
- 批准编号
- 22900AMX00215
- 商标
- 阿立哌唑粉
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(1G)
- 甲状腺酸普拉唑10毫克
- 添加剂
- 乳糖氢,tomolo koshidemin,羟基酚纤维素,轻度无水源
特点
- 表述的特征
- 白色溢出
- 销售名称
- 阿利皮拉唑OD片3mg“ nipro”
销售名称代码
- 1179045F4111
批准 /许可号码
- 批准编号
- 22900AMX00194
- 商标
- Aripiprazole OD片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- 阿利皮拉唑3mg
- 添加剂
- D-甘露醇,晶体纤维素,低替代羟基丙糖,硬脂酸镁,蓝色2
特点
- 产品性能外形
- 形状
- 米片含有蓝线(口腔塌陷片)
- 尺寸
- 6.0mm
- 厚度
- 2.6mm
- 重量
- 95mg
- 身体指标
- 铝酸OD 3 / OD 3 nipro
- 销售名称
- 阿利皮拉唑OD片6mg“ nipro”
销售名称代码
- 1179045F5118
批准 /许可号码
- 批准编号
- 22900AMX00195
- 商标
- Aripiprazole OD片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- α6mg的α
- 添加剂
- D-甘露醇,晶体纤维素,低替代羟基耐酚,硬脂酸镁
特点
- 产品性能外形
- 形状
- 白色平板电脑(口腔中锁定)
- 尺寸
- 7.0mm
- 厚度
- 2.8mm
- 重量
- 135mg
- 身体指标
- Apiprazole OD 6 Nipro
- 销售名称
- 脂唑OD片12mg“ nipro”
销售名称代码
- 1179045F6114
批准 /许可号码
- 批准编号
- 22900AMX00196
- 商标
- Aripiprazole OD片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- 阿利皮拉唑12mg
- 添加剂
- D-甘露醇,晶体纤维素,低替代羟基丙糖,硬脂酸镁,黄色5
特点
- 产品性能外形



- 形状
- 错过的彩色奖励片(口腔塌陷片)
- 尺寸
- 8.0mm
- 厚度
- 2.9mm
- 重量
- 180毫克
- 身体指标
- 阿利皮拉唑OD 12 nipro
- 销售名称
- 阿利皮拉唑OD片剂24mg“ nipro”
销售名称代码
- 1179045F7110
批准 /许可号码
- 批准编号
- 22900AMX00197
- 商标
- Aripiprazole OD片剂
药品价格标准日期
- 2017年6月
销售日期
- 2017年6月
储蓄,到期日期等
- 储蓄
- 室温保存
- 截止日期
- 在容器中描述,等等。
- 笔记
- 请参阅“处理预防措施”
法规类别
- 阳性药物
- 处方药1)
- 注意1)注意 - 医生的处方使用。
作品
- 活性成分(在1片中)
- 阿利皮拉唑24mg
- 添加剂
- D-甘露醇,晶体纤维素,低替代羟基丙糖,硬脂酸镁,红色102
特点
- 产品性能外形


- 形状
- 浅红色裸锁(口腔倒塌片)
- 尺寸
- 9.0mm
- 厚度
- 3.2mm
- 重量
- 230mg
- 身体指标
- Apriprazole OD 24 nipro
一般名称
- 甲状腺酸普拉唑的准备
警告- 1。
- 请注意这种药物期间高血糖的重要性和症状,因为该药物可能具有严重的副作用,从而导致糖尿病性酮症酸中毒和糖尿病性昏迷死亡。特别是,只有确定治疗以超过危险的治疗,并且在给药的情况下,观察到血糖水平的测量。
- 2。
- 在管理的情况下,上述副作用可能会事先表示给患者及其家人,并注意异常,例如干口,驾驶员,尿液,尿液,尿液频繁排尿,多态性和弱点。如果这些症状出现。出现,立即中断管理,并指示他们去看医生。 (请参阅“护理4.”部分,“重要的基本预防措施4,6。”和“侧面探索严重的副作用6.”)
|
限制(请勿对下一个患者进行管理)- 1。
- 昏迷的患者[可能会使昏迷恶化。这是给出的
- 2。
- 在中枢神经系统抑制剂(例如芭比抗酸衍生物和麻醉剂)下的强烈影响下[中枢神经系统抑制作用可能会增强。这是给出的
- 3。
- 肾上腺素正在施用的患者(不包括使用肾上腺素进行过敏反应治疗的病例)(请参阅相互作用部分)
- 四个。
- 对该药物成分过敏的患者
|
功效或效果
- 精神分裂症
- 改善躁郁症的躁狂症状
用法和剂量
- 精神分裂症
- 通常,对于成年人,每天6至12 mg是阿替普唑,每天保持6至24毫克,口服给药分为一两次。此外,尽管根据年龄和症状而增加和减少,但每日剂量不超过30 mg。
- 改善躁郁症的躁狂症状
- 通常,每天为阿哌他二唑一次给成年人服用12-24毫克。起始剂量应为24 mg,根据年龄和症状的不同,量将适当地增加或减少,但每日剂量不超过30 mg。
与使用和剂量有关的预防措施
- 1.与所有有效性不同
- 该药物达到稳态大约需要两个星期,因此希望在两周内不增加量。
- 2.对于精神分裂症
- (1)
- 通过仔细观察每位患者,请仔细地调节该药物的剂量,以使其最小必要。 [没有验证体重增加的效果增加。这是给出的
- (2)
- 由于其他开始治疗精神分裂症的患者更有可能出现在从其他抗精神病药变为该药物的患者中,因此更有可能具有副作用。
- 3.在改善躁郁症的躁狂症状的情况下
- 如果改善了躁狂症状,请考虑继续使用该药物,并注意不要使用该药物。
- 4.脂肪吡唑OD片“ nipro”的预防措施
- 这种药物只能用唾液(没有水)服用,因为它在口腔中很快倒塌,但是这不是预期通过口服粘膜吸收的效果表达的准备,因此在倒塌后用唾液或水吞下它。
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 肝脏损伤的患者[可能导致肝脏损伤。这是给出的
- 2。
- 患有心灵 /血管疾病,低血压或怀疑是这种怀疑的患者[可能会发生过度血压下降。这是给出的
- 3。
- 抽搐性疾病,例如癫痫或患有这些病史的患者[可能会减少抽搐。这是给出的
- 四个。
- 糖尿病或其病史的患者,或糖尿病家族史,高血糖,肥胖等患者[血糖水平可能升高。 (请参阅“警告”部分,“重要的基本预防措施4,6。”和“ Surseful Side Effects 6.”)
- 五。
- 有自杀或自杀计划,自杀护理病史的患者[自杀思维,自杀计划可能会出现。这是给出的
- 6。
- 老年人(请参阅有关“老年管理”的部分)
重要的基本预防措施
- 1。
- 请注意,不要让正在使用汽车的患者(例如驾驶汽车),例如嗜睡,注意力,注意力,集中度,集中和反射性运动能力,例如驾驶汽车。
- 2。
- 就精神分裂症而言,诸如兴奋,敌意和胡德之类的精神病症状可能会恶化,因此应充分观察到,如果看到恶化,请采取适当的措施,例如切换到其他治疗方法。物质。
从先前的治疗中切换时,希望逐渐减少先前治疗的剂量并给予这种药物。 - 3。
- 对于患有急性焦虑,沮丧和兴奋症状的患者,如果该药物的给药没有足够的影响,请考虑其他措施,例如镇静剂。
- 四个。
- 在该药物管理期间,您可能会产生严重的副作用,这可能导致糖尿病性酮症酸中毒,糖尿病性昏迷等死亡。注意高血糖的症状和症状,以及患有糖尿病,病史或其危险因素,危险因素的症状和症状。并彻底观察血糖水平。 (请参阅“警告”,“护理4”部分和“副作用6”的部分。
- 五。
- 由于可能会发生低血糖,因此在药物管理期间,请注意低血糖症状,例如虚弱,不适,汗水,震颤,睡眠和意识障碍,以及足够观察到的血糖水平。 (请参阅“ Suseful Side Effects 7.”的部分。)
- 6。
- 在服用该药物时,上述4.和5的副作用可能会事先表达给患者及其家人,以及高血糖症状(口干,饮酒,polyuria,polyuria,频繁排尿多种食物,弱点等)和降血糖症状(弱点,疲劳,汗水,漫步,睡眠,意识障碍等),如果出现这种症状,请立即中断给药。接受医生的指导。 (请参阅“警告”部分,“护理4.”和“ Suroseful副作用6.,7。”的部分。)
- 7。
- 尽管可能存在潜在的疾病,但这种药物给药后的病理赌博(尽管社会上有不利的结果,例如个人生活的崩溃,反复反复赌博的状态)以及病理性性欲的改善。出现了冲动性控制障碍,例如强迫性购买和暴饮暴食。冲动控制障碍的症状应提前向患者及其家人进行充分说明,如果出现症状,请指示他们咨询医生。此外,仔细观察患者状况和状况的变化以及病情状况,并采取适当的措施,例如症状出现时,根据需要进行体重减轻或取消。
- 8。
- 由于该药物的给药可能会导致体重波动(增加,减少),因此我们仔细观察到该药物给药期间体重的变化,如果确认体重波动,原因是并发症的并发症。影响等),并根据需要采取适当的措施。
- 9。
- 如果当血清催乳素浓度(例如已经施用其他抗精神病药)时使用该药物,则血清催乳素的浓度可能会降低并可能恢复,因此月经,贫血,子宫内膜异位症。请注意诸如这样的表达。
- 十。
- 由于可能会出现吞咽困难,尤其是在为患有抽吸肺炎风险的患者施用这种药物时,请仔细观察进展。
- 11。
- 在抗精神病药中报道了诸如肺栓塞和静脉血栓形成之类的血液固定主义,例如无法移动,长期挥之不去,肥胖,脱水等患者时要小心。 (请参阅“ Suseful副作用10.”的部分)
相互作用
互动的轮廓
- 该药物主要由CYP3A4和CYP2D6代谢,主要用于肝脏代谢。
禁忌症(不要一起使用)- 1。
- 毒品名称,等等
- 肾上腺素(用于过敏反应的紧急治疗时) (Bosmin)
- 临床症状 /度量方法
- 肾上腺素的作用可能会逆转,血压可能会下降。
- 机械 /危险因素
- 肾上腺素是肾上腺素工作α和β受体的兴奋剂。
|
合并用途的注释
(请注意联合使用)
- 1。药物名称,中枢神经系统抑制剂:芭比娃娃衍生物,麻醉药等。
- 临床症状 /度量方法
- 注意不要减肥,因为它具有中枢神经系统抑制作用。
- 机械 /危险因素
- 两者都有中枢神经约束。
- 2。药品名称等。
- 临床症状 /度量方法
- 由于可以彼此增加降压效应,因此应仔细施用它,例如减肥。
- 机械 /危险因素
- 两者都有降压作用。
- 3。具有抗胆碱作用的药物,例如药物名称
- 临床症状 /度量方法
- 由于可以增强抗胆碱效应,因此请仔细给药,例如减肥。
- 机械 /危险因素
- 两者都有抗磷脂作用。
- 四个。毒品名称等。多巴胺演员:左旋多巴准备
- 临床症状 /度量方法
- 多巴胺的操作可以减少,因此请仔细给予它,例如调整剂量。
- 机械 /危险因素
- 该药物具有多巴胺受体阻断效果。
- 五。酒精(酒精),例如毒品名称
- 临床症状 /度量方法
- 它可能会增加中枢神经系统抑制作用。
- 机械 /危险因素
- 两者都有中枢神经约束。
- 6。药物名称等。CYP2D6抑制药物:Kinjin,Paroxetine等。
- 临床症状 /度量方法
- 由于该药物的作用可能会增加,因此请考虑减少该药物的重量。
- 机械 /危险因素
- 该药物的血液浓度可能会增加,因为它抑制了该药物的主要代谢酶CYP2D6。
- 7。药物,例如药物名称CYP3A4可抑制的药物:Itolaconazole,Clarislycon等。
- 临床症状 /度量方法
- 由于该药物的作用可能会增加,因此请考虑减少该药物的重量。
- 机械 /危险因素
- 该药物的血液浓度可能会增加,因为它抑制了该药物的主要代谢酶CYP3A4。
- 8。药物名称(尤其是CYP3A4)药物:瓦尔瓦马泽金,利福平等。
- 临床症状 /度量方法
- 该药物的作用可能会削弱。
- 机械 /危险因素
- 该药物的主要代谢酶CYP3A4的诱导可能会降低该药物的血液浓度。
副作用
概述表达状态,副作用
- 该药物没有进行阐明副作用频率的调查。
严重的副作用
- 1.恶性综合征(频率未知)
- 如果没有动态的沉默,强度肌肉,吞咽困难,心动过速波动,血压波动,出汗等,则将继续表达,发烧以及一般管理,例如冷却体冷却和水分。应采取适当的措施。在疾病发作时,经常发现白细胞的增加和血清CK(CPK)的兴起,并且可能会发现肾功能伴随着肌红蛋白尿液。高烧可能会持续并且可能死亡,转变为意识障碍,呼吸困难,循环崩溃,脱水,急性肾脏疾病。
- 2.延迟运动障碍(频率未知)
- 由于长期给药可能会出现不寻常的运动,例如口腔外围,如果出现这种症状,我们应该考虑减肥或取消。即使在暂停行政后,症状也可能会继续。
- 3.瘫痪的回肠(频率未知)
- 肠瘫分析(症状,恶心,呕吐,显着的便秘,腹部浮动和肠道含量的停滞)可能会转移到瘫痪的回肠,因此,如果出现肠道瘫痪。
- 4.过敏反应(频率未知)
- 过敏反应可能会出现,因此请确保足够观察,停止给药并采取适当的措施。
- 5.水平肌肉熔化(频率未知)
- 由于可能发生了水平的肌肉融化,请注意CK(CPK)的兴起,血液和泌尿肌球蛋白的兴起等。
- 6.糖尿病性酮症酸中毒,糖尿病性粉状(频率频率)
- 在这种药物期间,已经报道了这种药物,例如糖尿病性酮症酸中毒和糖尿病性昏迷,因此渴求,尿液,尿液频繁,尿液,多重,多重,多重,无力,无力。足够的观察结果,例如测量血糖水平,如果发现异常,请采取适当的措施,例如胰岛素制剂的给药。 (请参阅“重要的基本预防措施4.,6。”部分)
- 7.低血糖(频率未知)
- 如果可能出现低血糖,应停用低血糖,例如虚弱,不适,冷汗,漫步,悬挂和意识障碍,应停止进行适当的治疗。 (请参阅“重要的基本预防措施5.,6。”部分)
- 8.抽搐(频率未知)
- 由于可能出现抽搐,如果发现异常,请采取适当的措施,例如停止管理。
- 9. Wramanulocytellia,白细胞减少(频率未知)
- 应该采取适当的措施,例如进行适当的观察,因为可能会发生凝聚的脉搏和白细胞,如果发现异常,则停止给药。
- 10.肺栓塞,深静脉血栓形成(频率未知)
- 由于已经据报道了抗精神病药的血液卷轴栓塞,例如肺栓塞和静脉血栓形成,因此可以很好地观察到它因呼吸急促,胸痛,肢体疼痛,水肿等而被识别。采取适当的措施,例如取消。 (请参阅“重要的基本预防措施11”部分)
- 11.肝功能障碍(频率未知)
- 可能会出现使用AST(GOT),ALT(GPT),γ-GTP,Al-P等的肝功能障碍,因此进行了足够的观察,如果发现异常,则停止给药。采取适当的措施。
另一个副作用
- *精神神经系统
- (频率未知)
- 失眠,神经敏感,焦虑,饥饿,头晕,头痛,抑郁,幻觉,性欲,性欲,性欲,性欲,自杀,自杀,侵略性反应,异常思维,厌食,细菌,厌食症,细菌,降低感知,降低感知,假障碍,假疾病,假疾病。勃起,射精障碍,勃起,晕厥,情绪不稳定性,神经病学,神经症,妄想,躁狂反应,躁狂反应,心理症状,双相情感障碍,双相情感障碍,痴呆症,健忘症,睡眠障碍,镇静,镇静,舌头瘫痪。 ,挫败感,兴奋),恐慌反应,米达,面部抽搐,面部幻觉,记忆障碍,挤压感觉,梦幻,噩梦,控制障碍受损(病理赌博,增强的病理性性欲) ,过度运动,心理功能障碍,感觉障碍,眉毛反射,方形短语,无情感,情绪波动,异常行为,下肢不可或缺的综合症
- 在外向路径症状
- (频率未知)
- Akacia,Tremor,流口水,动员,行走异常,发育不良(肌肉张力异常),Dyskinzia,声音障碍,声音障碍,肌肉僵硬,吞咽,吞咽,身体僵硬,肌肉张力,嘴巴张力,嘴巴pittuisee,pittuisee,Parkson综合征,Parkson综合征,帕克森综合症,眼球旋转,眼球旋转攻击。 , - per- pyramidal道路障碍,反射增加
- *心血管
- (频率未知)
- 心动过速,高血压,呼吸症,心动过缓,低血压,异常低血压,异常(外部收缩,QT延伸,第一个心脏块等),擦除的血压,心绞痛
- *消化
- (频率未知)
- 便秘,恶心,呕吐,腹痛,腹泻,食欲不振,食欲增加,幽灵炎,胃炎,胃炎,胃炎,附加炎,起步性炎,气孔炎,口臭,阴道炎,唇彩肿胀,腹部弹力弹性,酸性疾病,酸性疾病,牙周炎,粘液症,粘液性,粘液性,粘液性,粘液性,粘液性痛苦舌障,牙齿超敏反应
- 血
- (频率未知)
- Red blood cells, leukocytes, leukocytes increased, neutrophiled, neutrophils, eosinophils increased, monocular reduction, lymphocytes, lymphocytes increased, hemoglobin decreased, hematocrit value, anemia, red blood cells. Masuta, good base baseball, good salt baseball ball, eosinophils increase,单球减少,血小板减少,血小板增加,血红蛋白增加,hematon栗子值增加。
- 内分泌
- (频率未知)
- 处方降低,月经异常,催乳素升高,血甲状腺刺激激素增加,卵巢疾病
- 肝
- (频率未知)
- Alt(GPT)增加,AST(GOT),LDH上升,γ-GTP增加,Al-P增加,脂肪肝,Al-P降低,LDH降低,总胆红素,总胆红素,胆红素,肝炎,黄疸病
- 肾
- (频率未知)
- 面包上升,降低面包,蛋白尿,尿液沉积,肌酐上升,尿液 - 胰蛋白脂蛋白升高,尿billillbin上升,尿液NAG升高,尿比重力,尿比重力,尿神圣犹豫,血液尿液减少,减少血液尿液,减少血液尿酸。尿液尿酸的减少。减少量,酮尿液
- 泌尿科
- (频率未知)
- 尿液,尿液障碍,血尿,膀胱炎,尿液闭合,尿液频繁,尿液,尿失禁
- 高敏性
- (频率未知)
- 皮疹,轻易激反应,湿疹,红斑,Soarchy,酒,血管水肿,荨麻疹,药物超敏反应
- 皮肤
- (频率未知)
- acnia,皮炎,皮肤干燥,皮肤剥皮,皮肤干燥,色素沉着障碍,脂肪症,雄性图案聚合物,真菌感染,脱毛
- 新陈代谢
- (频率未知)
- CK(CPK)上升,口干,胆固醇,HDL-胆固醇,甘油三酸酯的增加,脂质减少,高血糖,高乳液中毒,高脂血症,高脂血症,脂质代谢,胆固醇升高,胆固醇上升。血糖波动,血液胰岛素增加
- *呼吸器
- (频率未知)
- 鼻炎,咽炎,支气管炎,支气管痉挛,鱼类症状,打ic,鼻腔干燥,吞咽肺炎,上呼吸道感染,呼吸困难
- *眼睛
- (频率未知)
- Kiri视觉,眼睛 - 束缚,视觉障碍,调节障碍,清晰,眼睛疼痛,眼痛,眼痛,糖尿病性白内障,瞬时
- *其他人
- (频率未知)
- 体重,减少倦怠感,脱力感,発热多汗,减少総,,グロブリン分画分画分画分画异常,ナトリウムナトリウムナトリウム低下,カリウムカリウムカリウム低下低下,クロール低下低下, Joint pain, muscle pain, cervical pain, stiff shoulders, muscle spasm, chills, peripheral hemorrhage, genital hemorrhage, miscarriage, thoracic pain, abscess, bruxism, astonatry, nasal bleeding, peripheral edema, poor mood, taste abnormal , Tinnitus, night汗水,不愉快的感觉,吸毒,面部水肿,降低,抓地力,下降,总蛋白质,A / G的增加,白蛋白增加,白蛋白减少,钠升高,钾升高,爬行,爬行。低体温,疼痛,疼痛,下颌疼痛,乳头疼痛,乳腺,外阴阴道干燥,无死,垂死,关节脱位,牙齿,肌肉痉挛,肌肉痉挛,尿路感染,干草热,关节炎,肌肉萎缩,肌肉萎缩,肌肉萎缩,脂肪,脂肪。
老年人的管理
- 通常,老年人的生理功能降低了,因此在观察患者病情的同时仔细给药。
管理孕妇,妇产科妇女等。
- 1。
- 对于可能怀孕的孕妇或妇女,只有在确定治疗要超过危险的情况下才有必要管理。 [尚未确定怀孕期间的管理安全。据报道,新生儿在怀孕后期被施用,新生儿患有戒断症状,例如喂养,饥饿,呼吸系统疾病,通风,肌肉张力和易感性。此外,在其他公司进行的阿吡唑配方的临床试验中,还有一份报道说流产。这是给出的
- 2。
- 在哺乳女士管理时,请停止母乳喂养。 [人类允许牛奶过渡。这是给出的
给儿童的管理等
- 尚未确定低出生体重,新生儿,婴儿,婴儿或儿童的安全性(没有经验)。
过量
- 1.迹象,症状
- 在其他公司和自发报告进行的外国临床试验中,据报道,帕迪,舌头,血压和呕吐等症状是在意外或紧急服用高达1,260毫克的成年人中。在不小心达到195毫克的儿童中,表达了过度意识和饥饿等症状。
- 2.行动
- 特定的解毒剂尚不清楚。如果该药物过改造,则集中于辅助治疗,确保气道,氧气吸入,通风和症状。立即开始对心脏功能的监测,并观察患者康复,同时通过心电图连续监测心律不齐的表达。早期给药活性碳是有用的。血液透析不被认为有用。如果有可能服用其他药物,请注意这些作用。
适用的预防措施
- 1.发出药物时
- PTP包装药物应从PTP纸中取出并教给它。据报道,食管粘膜的难度很难在食管粘膜上具有硬尖角,然后引起严重的并发症,例如纵隔炎。这是给出的
- 2.服用时(alipipurazole OD片剂“ nipro”)
- 不要在没有水的情况下服用这种药物。
- 3。
- 指示使孩子遥不可及。
其他预防措施
- 1。
- 据报道,这种药物的治疗突然死亡未知。
- 2。
- げっ歯類(マウス、ラット)のがん原性試験において、乳腺腫瘍(雌マウス3mg/kg/日以上、雌ラット10mg/kg/日)及び下垂体腫瘍(雌マウス3mg/kg/日以上)の発生頻度の上昇が報告されている。これらの腫瘍はげっ歯類では血中プロラクチンの上昇と関連した変化としてよく知られている。ラットのがん原性試験において、60mg/kg/日(最高臨床推奨用量の100倍に相当)の雌の投与群で副腎皮質腫瘍の発生頻度の上昇が報告されている。
- 3.
- サルの反復経口投与試験において胆のう内の沈渣(泥状、胆砂、胆石)が4週間〜52週間試験の25mg/kg/日以上の用量で、肝臓に限局性の肝結石症様病理組織所見が39週間試験の50mg/kg/日以上の用量で報告されている。沈渣はアリピプラゾール由来の複数の代謝物がサル胆汁中で溶解度を超える濃度となり沈殿したものと考えられた。なお、これら代謝物のヒト胆汁中における濃度(1日目15mg/日投与、その後6日間30mg/日反復経口投与時)はサル胆汁中における濃度の5.6%以下であり、また、ヒト胆汁中における溶解度の5.4%以下であった。
- 4.
- 外国で実施された認知症に関連した精神病症状(承認外効能・効果)を有する高齢患者を対象とした17の臨床試験において、本剤を含む非定型抗精神病薬投与群はプラセボ投与群と比較して、死亡率が1.6〜1.7倍高かったとの報告がある。死因は様々であったが、心血管系(心不全、突然死等)又は感染症(肺炎等)による死亡が多かった。なお、本剤の3試験(計938例、平均年齢82.4歳;56〜99歳)では、死亡及び脳血管障害(脳卒中、一過性脳虚血発作等)の発現率がプラセボと比較して高かった。また、外国での疫学調査において、定型抗精神病薬も非定型抗精神病薬と同様に死亡率の上昇に関与するとの報告がある。
薬物動態
- 生物学的同等性試験
- (1)アリピプラゾール錠3mg「ニプロ」
- アリピプラゾール錠3mg「ニプロ」は「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」(平成24年2月29日 薬食審査発0229第10号)に基づき、アリピプラゾール錠6mg「ニプロ」を標準製剤としたとき、溶出挙動が等しく、生物学的に同等とみなされた。 1)
- (2)アリピプラゾール錠6mg「ニプロ」
- アリピプラゾール錠6mg「ニプロ」と標準製剤のそれぞれ1錠(アリピプラゾールとして6mg)を、クロスオーバー法により健康成人男子に絶食単回経口投与して血漿中アリピプラゾール濃度を測定した。得られた薬物動態パラメータ(AUC 0→168hr 、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。 2)
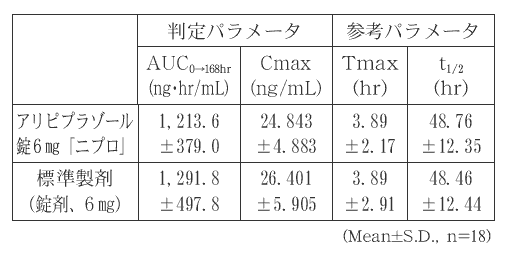
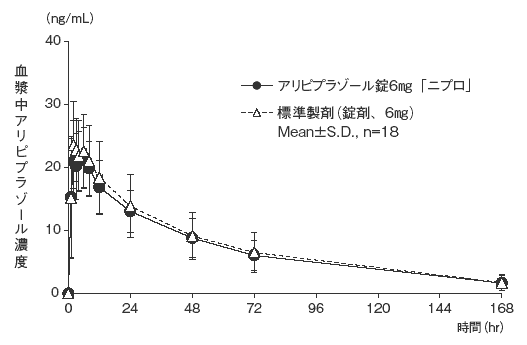
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。 - (3)アリピプラゾール錠12mg「ニプロ」
- アリピプラゾール錠12mg「ニプロ」と標準製剤のそれぞれ1錠(アリピプラゾールとして12mg)を、クロスオーバー法により健康成人男子に絶食単回経口投与して血漿中アリピプラゾール濃度を測定した。得られた薬物動態パラメータ(AUC 0→168hr 、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。 3)
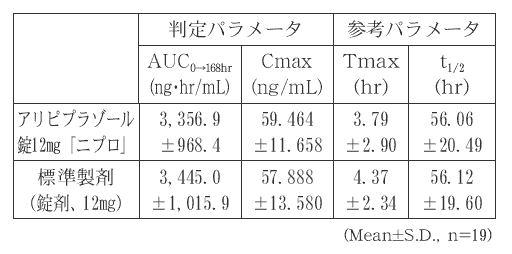
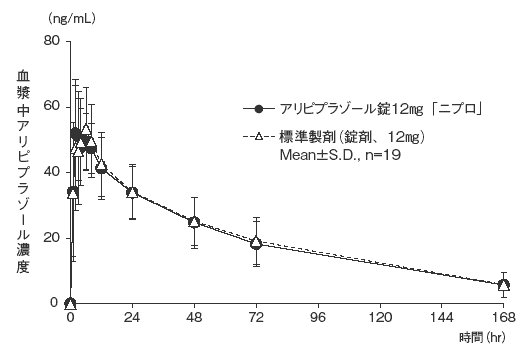
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。 - (4)アリピプラゾール散1%「ニプロ」
- アリピプラゾール散1%「ニプロ」と標準製剤のそれぞれ0.6g(アリピプラゾールとして6mg)を、クロスオーバー法により健康成人男子に絶食単回経口投与して血漿中アリピプラゾール濃度を測定した。得られた薬物動態パラメータ(AUC 0→168hr 、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。 4)
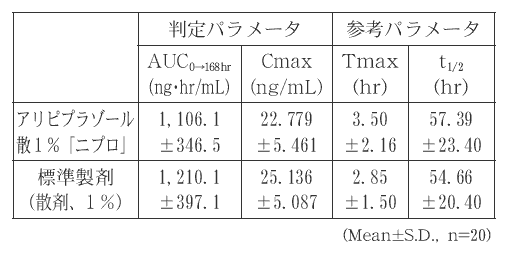
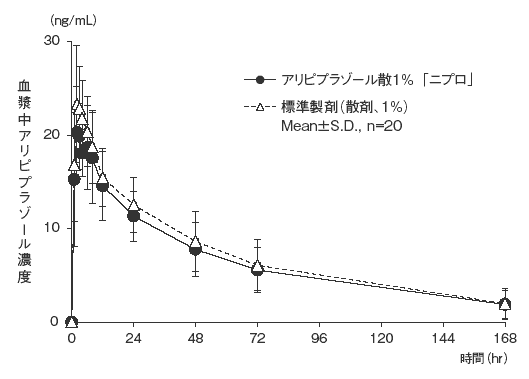
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。 - (5)アリピプラゾールOD錠3mg「ニプロ」
- アリピプラゾールOD錠3mg「ニプロ」は「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」(平成24年2月29日 薬食審査発0229第10号)に基づき、アリピプラゾールOD錠6mg「ニプロ」を標準製剤としたとき、溶出挙動が等しく、生物学的に同等とみなされた。 5)
- (6)アリピプラゾールOD錠6mg「ニプロ」
- アリピプラゾールOD錠6mg「ニプロ」と標準製剤のそれぞれ1錠(アリピプラゾールとして6mg)を、クロスオーバー法により健康成人男子に絶食単回経口投与して血漿中アリピプラゾール濃度を測定した。得られた薬物動態パラメータ(AUC 0→168hr 、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
- 1)水あり投与6)
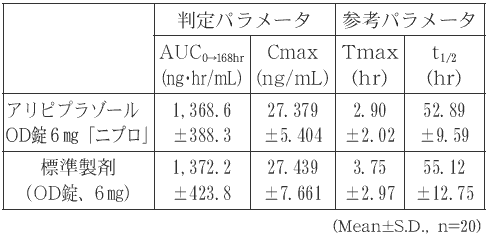
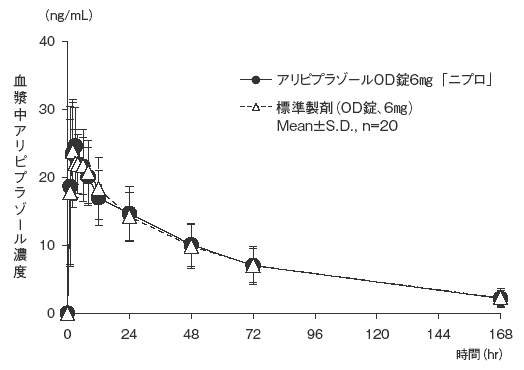
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。- 2)水なし投与7)
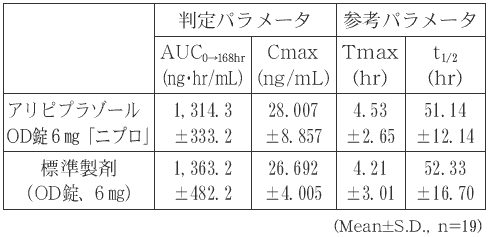
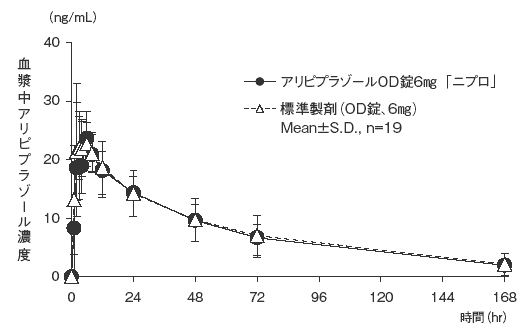
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
- (7)アリピプラゾールOD錠12mg「ニプロ」
- アリピプラゾールOD錠12mg「ニプロ」と標準製剤のそれぞれ1錠(アリピプラゾールとして12mg)を、クロスオーバー法により健康成人男子に絶食単回経口投与して血漿中アリピプラゾール濃度を測定した。得られた薬物動態パラメータ(AUC 0→168hr 、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)〜log(1.25)の範囲内であり、両剤の生物学的同等性が確認された。
- 1)水あり投与8)
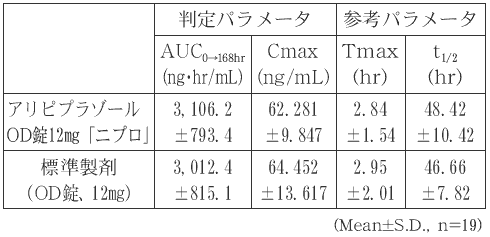
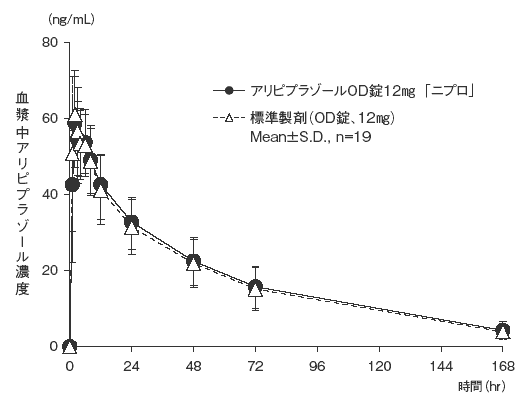
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。- 2)水なし投与9)
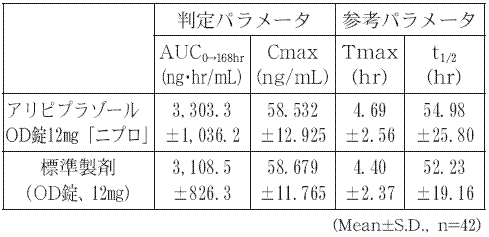
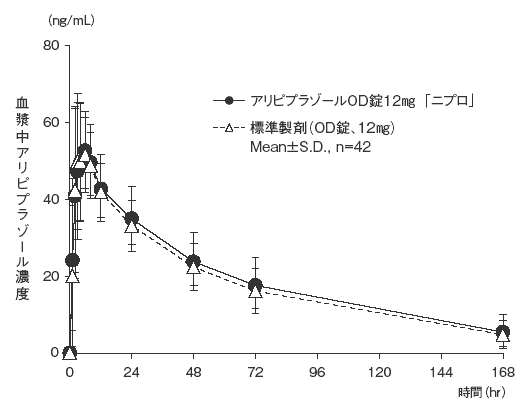
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
- (8)アリピプラゾールOD錠24mg「ニプロ」
- アリピプラゾールOD錠24mg「ニプロ」は「含量が異なる経口固形製剤の生物学的同等性試験ガイドライン」(平成24年2月29日 薬食審査発0229第10号)に基づき、アリピプラゾールOD錠12mg「ニプロ」を標準製剤としたとき、溶出挙動が等しく、生物学的に同等とみなされた。 10)
薬効薬理
- アリピプラゾールはD 2受容体部分アゴニストである。脳内でドパミンが大量に放出されているときは抑制的に、少量放出時には促進的に作用し、ドパミン神経系を安定させる。5-HT 2A受容体アンタゴニスト作用及び5-HT 1A受容体部分アゴニスト作用を併せもち、陽性症状にも陰性症状にも有効である。 11)
有効成分に関する理化学的知見
- 一般名
- アリピプラゾール(Aripiprazole)
- 化学名
- 7-{4-[4-(2,3-Dichlorophenyl)piperazin-1-yl]butoxy}-3,4-dihydroquinolin-2(1 H )-one
- 分子式
- C 23 H 27 Cl 2 N 3 O 2
- 分子量
- 448.39
- 構造式
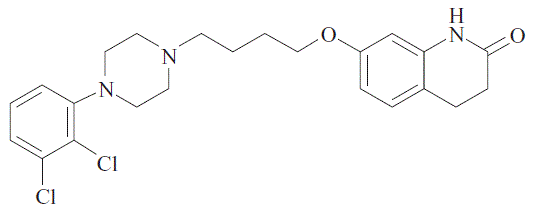
- 性状
- ・白色の結晶又は結晶性の粉末である。
・ベンジルアルコールに溶けやすく、酢酸(100)にやや溶けやすく、水、アセトニトリル、メタノール、エタノール(99.5)又はヘキサンにほとんど溶けない。
・結晶多形が認められる。
取扱い上の注意
- 1.
- アリピプラゾール錠・OD錠「ニプロ」の注意事項
- (1)
- バラ包装品は、使用の都度キャップをしっかり締めること。
- (2)
- PTP包装品は、アルミピロー開封後は高温・高湿を避けて保存すること。
- 2.
- 安定性試験
- (1)アリピプラゾール錠3mg「ニプロ」
- 最終包装製品を用いた加速試験(40℃、相対湿度75%、6カ月)の結果、アリピプラゾール錠3mg「ニプロ」は通常の市場流通下において3年間安定であることが推測された。 12)
- (2)アリピプラゾール錠6mg「ニプロ」
- 最終包装製品を用いた加速試験(40℃、相対湿度75%、6カ月)の結果、アリピプラゾール錠6mg「ニプロ」は通常の市場流通下において3年間安定であることが推測された。 13)