4006 776 356
免费咨询 9:00-18:00
获取国外Ethesolam片剂0.25mg“ SW” / Ethesolam片0.5mg“ SW” / Et药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / Ethesolam片剂0.25mg“ SW” / Ethesolam片0.5mg“ SW” / Et
Ethesolam片剂0.25mg“ SW” / Ethesolam片0.5mg“ SW” / Et
1992年7月
Ethesolam片剂0.25mg“ SW” / Ethesolam片0.5mg“ SW” / Ethizolam 1mg“ SW”
创建或修订年
- ** 2019年7月修订(第22版)
- *2017年3月修订
日本标准产品分类编号
- 871179
医学分类名称
- 镇静剂
批准,等等
- 销售名称
- ethesolam锁定0.25mg“ SW”
销售名称代码
- 1179025F3070
批准 /许可号码
- 批准编号
- 22600AMX00975000
- 商标
- etizolam
药品价格标准日期
- 2014年12月
销售日期
- 2014年12月
储蓄,到期日期等
- 储蓄
- 剃须室温存储
- 截止日期
- 显示在外盒子上
标准名称
- 日本药房
- Etizolam锁
法规类别
- 精神药物
- 处方药
- 预防措施 - 通过医生等处方使用
作品
- Ethesolum片剂0.25 mg“ SW” :在1片中包含0.25 mg日本局。
添加剂包括狂欢氏菌,晶体纤维素,氧化钛,二氧化铁,硬脂酸mg,mg,tumoro koshidepin,乳糖,羟基丙糖,羟基丙糖,Hypromeros和6000 Macrool 6000。
构图与性表
| 药物 | 直径(mm) | 重量(毫克) | 厚度(mm) | 特点 | 识别代码 | 外形 |
| 膜涂料锁 | 6.1 | 大约98 | 3.4 | 淡红色 | SW 036 |  |
- 销售名称
- Ethesolam平板电脑0.5mg“ SW”
销售名称代码
- 1179025F1239
批准 /许可号码
- 批准编号
- 22300AMX01266000
- 商标
- etizolam
药品价格标准日期
- 2012年6月
销售日期
- 1992年7月
储蓄,到期日期等
- 储蓄
- 剃须室温存储
- 截止日期
- 显示在外盒子上
标准名称
- 日本药房
- Etizolam锁
法规类别
- 精神药物
- 处方药
- 预防措施 - 通过医生等处方使用
作品
- Ethesolam 0.5mg“ SW” :包括1片片的日本乙佐糖0.5毫克。
包括添加剂包括carnavarou,晶体纤维素,氧化钛,硬脂酸盐,Tark,Tomolo koshidepin,乳糖,氢化脂蛋白和6000。
构图与性表
| 药物 | 直径(mm) | 重量(毫克) | 厚度(mm) | 特点 | 识别代码 | 外形 |
| 膜涂料锁 | 6.1 | 大约98 | 3.0 | 白色的 | SW 037 |  |
- 销售名称
- Ethesolam平板电脑1mg“ SW”
销售名称代码
- 1179025F2197
批准 /许可号码
- 批准编号
- 22300AMX01267000
- 商标
- etizolam
药品价格标准日期
- 2012年6月
销售日期
- 1992年7月
储蓄,到期日期等
- 储蓄
- 剃须室温存储
- 截止日期
- 显示在外盒子上
标准名称
- 日本药房
- Etizolam锁
法规类别
- 精神药物
- 处方药
- 预防措施 - 通过医生等处方使用
作品
- Ethosolum片剂1毫克“ SW” :一片含有1mg的日本乙醇液。
包括添加剂包括carnavarou,晶体纤维素,氧化钛,硬脂酸盐,Tark,Tomolo koshidepin,乳糖,氢化脂蛋白和6000。
构图与性表
| 药物 | 直径(mm) | 重量(毫克) | 厚度(mm) | 特点 | 识别代码 | 外形 |
| 膜涂料锁 | 7.1 | 大约134 | 3.1 | 白色的 | SW 038 |  |
限制(请勿对下一个患者进行管理)- 1。
- **角度青光眼患者的急性阻塞性角[抗蛋白的作用可能增加眼内压力并恶化症状。这是给出的
- 2。
- 严重肌肉的患者[肌肉放松动作可能会使症状恶化。这是给出的
|
功效或效果
- 焦虑,张力,抑郁,神经划分症状,神经症的睡眠障碍
- 焦虑,紧张,抑郁症的睡眠障碍
- 身体疾病(高血压,胃 /十二指肠溃疡)和身体综合征和焦虑,紧张,抑郁,睡眠障碍
- 精神分裂症的睡眠障碍
- 焦虑,紧张,抑郁和肌肉张力颈脊椎病,背痛,肌肉控制的头痛在以下疾病中
用法和剂量
- 在神经症或抑郁症的情况下,通常每天将其分为3 mg,作为ethosolam作为etzolam。
- 就心身疾病,宫颈脊柱瘤,背痛或肌肉控制的头痛而言,通常每天3次以etzolam的身份口服对成年人的口服。
- 当用于睡眠障碍时,通常将其用于每天1至3毫克的成年人,然后上床睡觉。
- 在每种情况下,根据年龄和症状,它都会适当增加或减少,但是对于老年人来说,它每天为Etzolam每天1.5 mg。
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 心脏障碍的患者[可能发生血压,心脏病患者可能导致症状恶化。这是给出的
- 2。
- 肝脏和肾脏疾病的患者这是给出的
- 3。
- 大脑中有机残疾患者[可能有强烈的作用。这是给出的
- 四个。
- 儿童(请参阅“儿童管理等”部分)
- 五。
- 老年人(请参阅“老年人行政”部分)
- 6。
- 弱化的患者[可能会出现强烈的行动。这是给出的
- 7。
- 当对呼吸功能高度降低的患者施用时,患有中度呼吸疾病或严重呼吸疾病(呼吸衰竭)的患者可能会导致二氧化碳。这是给出的
重要的基本预防措施
- 1。
- 请注意,可能会发生嗜睡,注意力,注意力,集中度,集中度和反射性电动机容量,而不必驾驶汽车(例如驾驶汽车)的机器操作。
- 2。
- *避免连续给药长期使用,因为它可能由于连续使用而导致药物依赖性。在继续使用该药物时,请仔细考虑需要治疗(请参阅“严重副作用”部分)。
相互作用
- 该药物由CYP2C9和CYP3A4代谢。
合并用途的注释
(请注意联合使用)
| 毒品名称,等等 | 临床症状 /度量方法 | 机械 /危险因素 |
| 中枢神经抑制剂示例势词衍生物巴孔酸衍生物等。 | 它可能导致嗜睡,降低血压,运动和意识障碍。 | 中枢神经系统组合的组合被认为具有额外的增强。 |
| MAO抑制剂 | 有过度昏迷,抽搐和兴奋的风险。 | MAO抑制剂抑制了该药物肝脏中的代谢,延长了一半的生命并增加了血液浓度,因此可能会增加其作用。 |
| 全酰胺马来酸 | 由于该药物的血液浓度可能会增加,因此会仔细给药,例如减少该药物的剂量。 | 雌激素的恶心可能会抑制该药物肝脏中的代谢,并增加血液浓度以增加该药物的作用。 |
酒精
(喝) | 精神功能,感知和运动功能可能会降低。 | 乙醇和该药物可能具有额外的中心抑制作用。 |
副作用
概述表达状态,副作用
- 该药物不进行调查,以阐明副作用的频率,例如用法调查。
严重的副作用
(频率未知)- 1。
- *依赖性:因为它可能由于连续使用而导致药物依赖性,因此应充分观察到它用于剂量和使用期。同样,由于连续使用或取消管理的剂量迅速降低,因此可能会出现抽搐,del妄,短,短缺,失眠,焦虑,幻觉,妄想等等戒断症状。逐渐减肥。
- 2。
- 呼吸抑制,二氧化碳coocis :可能发生呼吸道抑制。此外,如果将呼吸功能施用给高度降低呼吸功能的患者,则可能引起二氧化碳,因此在这种情况下,应固定气道并应适当进行通风。
- 3。
- 恶性综合征:由于服用该药物,抗精神病药的组合或突然的体重减轻和该药物的取消,可能发生恶性综合征。如果身体冷却,水合等进行身体管理,则在发烧,强度,吞咽困难,心动过速,血压波动,出汗,白细胞增加,血清CK(CPK)等做治疗。另外,在一组综合征中,可能会发生肾功能伴随着肌红蛋白尿液。
- 四个。
- 在水平肌肉肌肉旋律的情况下:肌肉疼痛,无力,血清CK(CPK)增加,杆肌肉融化,其特征在于血液和尿肌红蛋白的兴起,因此在这种情况下,要取消并采取适当的措施。 。
- 五。
- 间质性肺炎:可能会发生间质性肺炎,因此,发现发烧,咳嗽,呼吸困难,肺部声音异常(扭曲的声音)等,请停止使用,并且胸部X射线迅速进行X射线。采取适当的措施,例如施用肾上腺皮质激素药物。
- 6。
- 肝功能障碍,黄疸:肝功能障碍(AST(GOT),ALT(GPT),γ-GTP,LDH,Al-P,胆红素等),黄疸等。例如中断政府。
另一个副作用
| 未知频率 |
| *精神神经系统 | 嗜睡,涉水,头晕,步行,头痛 /头痛,语言障碍,失眠,醉酒,兴奋,沮丧,变化,眼睛症状(雾,配位障碍),健忘,刺激,混乱,混乱,混乱 |
| 呼吸器官 | 呼吸困难 |
| 心血管 | 心p,头晕 |
| 消化器官 | 口渴,恶心,厌食,胃 /腹部不适,呕吐,腹痛,便秘,腹泻 |
| 高敏性注1) | 皮疹,荨麻疹,如此发痒,红斑 |
| 骨骼肌 | 肌肉张力症状,例如疲劳,无力,易于疲劳,肌肉放松等。 |
| 其他的 | 出汗,尿液障碍,水肿,鼻子闭合,牛奶分泌,女性乳房,高嗜血杆菌血症,丰满痉挛2) |
- 注意1)如果出现这种症状,请停止给药。
- 注2)在服用该药物期间进行足够的观察,如果可以识别出瞬时,恐惧和干燥等眼睛症状,请进行适当的治疗。
老年人的管理
- 在老年人中,很可能表达诸如运动意义之类的副作用,因此应仔细给药,例如从少量开始给药。
管理孕妇,妇产科妇女等。
- 1。
- 对于可能怀孕(3个月内)或孕妇的妇女,只有确定治疗的益处超过危险时。 [动物实验报告了宝库形的作用,以及在怀孕期间怀孕期间对其他苯并二氮卓药物(Diazepam)施用的患者中生育畸形儿童的例子。它比这更重要。这是给出的
- 2。
- 仅当确定治疗以超过危险状态时,才应在怀孕晚期对妇女进行管理。 [基于苯二氮卓类药物,具有新生儿,呕吐,呕吐,肌肉张力减轻,肌肉张力减少,肌肉张力,倾斜,睡眠,睡眠,呼吸抑制,磨损,硫仙,易于刺激,紧张,高敏,超敏,低温,低温,tachycycemia等据报道。这些症状可能被报告为戒断症状或新生儿。据报道,苯二氮卓类药物会增加黄疸为新生儿。血清CK(CPK)上升可能会出现在怀孕后期使用该药物的患者出生的新生儿中。这是给出的
- 3。
- 苯二氮卓类药物据报道,新生儿在分娩后生下新生儿后会出现。
- 四个。
- 希望避免给护理妇女管理,但是如果您必须这样做,请避免母乳喂养。 [搬到人类母乳中,新生儿可能正在增加体重。此外,据报道,其他苯二氮卓类药物(地西eepam)会导致恶作剧,体重减轻等,并可能增加黄疸。这是给出的
给儿童的管理等
- 尚未确定儿童的安全性(使用的经验更少)。
过量
- 1。
- 用药过量可能导致运动,低血压,呼吸道抑制和意识障碍。
- 2。
- 当使用过量或怀疑该药物的药物过量时,使用全麦唑(苯二氮卓受体拮抗剂)作为一种程序时,请在使用前使用fulmazenyl(禁忌症,谨慎,相互作用等)进行预防。在没有鉴定药物的情况下给药的患者,该患者的给药已被施用,该药物的镇静和抗惊魂效应可能会发生变化,并且可能会延迟。
适用的预防措施
- 在药物时:PTP包装中的药物应从PTP纸中取出并指示服用。 (据报道,PTP薄板的难度 - 到末期在食管粘膜上有一个尖锐的角,甚至是严重的并发症,例如纵隔炎)。
药代动力学
- 1.生物等效测试○乙佐糖锁0.25mg“ SW”
Etizolam片剂0.25mg“ SW”基于“生物学外向的等价,具有不同含量的口服固体配方(药物和食物检查0229 No. 10)” SW用作标准准备,洗脱行为是相等的,并且是被视为生物学。 1) - ○Etisolam锁定0.5mg“ SW”
乙醇片片剂0.5 mg“ SW”和标准制剂用于空腹(交叉)的健康成年男孩(0.5 mg作为Etizolam),并测量了血清中etzolum的浓度。由于对获得的药代动力学参数(AUC,CMAX)的统计分析,证实了两种药物的生物等效性。 2) 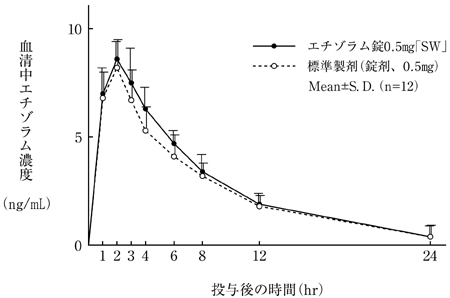
- 血清浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,身体的时间和体液的时间)而有所不同。
- ○埃托佐兰平板电脑1mg“ SW”
精神片剂1 mg“ SW”和标准制剂分别用于健康的成年男孩(1 mg作为乙醇粒),并测量了血清中etzolum的浓度。由于对获得的药代动力学参数(AUC,CMAX)的统计分析,证实了两种药物的生物等效性。 3) 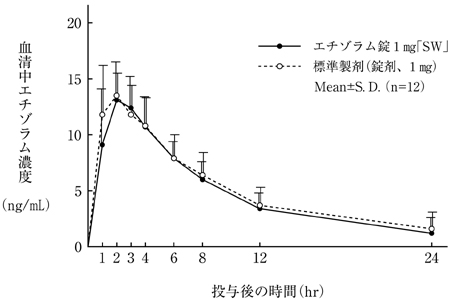
- 血清浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,身体的时间和体液的时间)而有所不同。
- 2.已确认,洗脱行为簿的准备适合日本药房指定的洗脱标准。
0.5 mg片剂1药代动力学参数在1片剂时
| cmax(ng/ml) | tmax(HR) | T 1/2 (HR) | AUC 0-24hr (Ng/hr/ml) |
| Ethesolam平板电脑0.5mg“ SW” | 8.9±1.2 | 2.1±0.3 | 5.7±1.8 | 69.5±11.3 |
| 标准制备(片剂,0.5mg) | 8.4±1.1 | 2.0±0.4 | 6.2±2.6 | 64.2±10.5 |
(平均±SD)
1mg片剂1用于给药1片剂的药代动力学参数
| cmax(ng/ml) | tmax(HR) | T 1/2 (HR) | AUC 0-24hr (Ng/hr/ml) |
| Ethesolam平板电脑1mg“ SW” | 14.0±2.8 | 2.2±0.7 | 7.1±4.2 | 119.3±33.7 |
| 标准准备(平板电脑,1mg) | 14.3±2.3 | 1.8±0.6 | 8.2±5.3 | 128.0±33.0 |
(平均±SD)
药物
- 它作用于苯二氮卓类联合部位,表现出焦虑和催眠。也就是说,通过与GABA A受体亚基中存在的苯二氮卓类接合的位点结合,它增加了抑制剂GABA的受体亲和力,从而增强了CL-通道的开口效果,并促进了神经功能抑制。四)
有关活性成分的物理和化学知识
- 通用名称
- etizolam
- 化学名称
- 4-(2-氯苯基)-2-乙基-9-甲基-6H-6H-thieno [3,2-f] [1,2,4] Triaszolo [4,3-A] [1,4]
- 分子
- C 17 H 15 CLN 4 S
- 分子量
- 342.85
- 熔点
- 146-149℃
- 结构公式
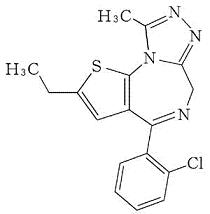
- 特点
- 乙醇是白色至浅黄色的结晶粉。溶解在乙醇(99.5)中的略容易,在某种程度上很难溶于乙腈或无水乙酸,并且几乎溶于水中。
处理的预防措施
- ・稳定性测试片0.25 mg:由于使用PTP包装的物品加速测试(40°C 75%,6个月)的结果,假定在正常市场分布下它稳定了三年。五)
- 片剂0.5 mg/片剂1 mg:使用PTP包装和玫瑰包装的长期保存测试(室温,3年),可以证实,在正常市场分布下,它稳定了三年。 6),7)
包装
- ethesolam锁定0.25mg“ SW”:
PTP:100片(10片X 10) - Ethesolam片剂0.5mg“ SW”:
PTP:100片(10片X 10),1,000片(10片X 100)
玫瑰:1,000片 - Ethesolam平板电脑1mg“ SW”:
PTP:100片(10片X 10),1,000片(10片X 100)
玫瑰:1,000片
主要文献和文档请求目的地
主要文献
- 1)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 2)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 3)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 四)
- 第七次修订的日本药房评论,Hirokawa Shoten,2016年,C-849。
- 五)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
- 6)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
- 7)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
文学要求
- [请索取以下的主要文件(包括 - 房屋材料)]
Sawai Pharmaceutical Co.,Ltd.制药信息中心 - 532-0003 532-0003 Miyahara,Yodogawa-ku,大阪 - 2-30
- 电话:0120-381-999
- 传真:06-6394-7355
有关长期管理药物的信息
- 通过通知卫生部,劳动和福利部365号(2016年10月13日),该药物仅限于30天的药物。
制造商等的姓名或名称和地址等。
- 销售代理
- Sawai Pharmaceutical Co.,Ltd。
- 5-130 Miyahara,大阪Yodogawa-ku
- 制造和分销商
- Medisa Shinko Co.,Ltd.
- 5-2-27 Miyahara,大阪Yodogawa-Ku