4006 776 356
免费咨询 9:00-18:00
获取国外Esster氢化氢化在100mg“ AFP” / ESTEL中ig药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / Esster氢化氢化在100mg“ AFP” / ESTEL中ig
Esster氢化氢化在100mg“ AFP” / ESTEL中ig
1978年6月
- 手术冲击和冲击中的紧急或术后冲击
- 根据症状和病例,每天或每天几次将其静脉注射或静脉内注射或静脉注射2至20 mL(作为氢化软件100至1,000 mg)。
氢化酚酸Na静脉液体液体100mg“ AFP” / ESTEL Na在氢结型蛋白500mg“ AFP”的埃斯泰尔中
创建或修订年
- **于2021年7月修订(修订了第13版,使用的预防措施)
- *修订于2019年10月
日本标准产品分类编号
- 872452
日本标准产品分类编号,等等。
- 重新评估结果公告年(最新)
- 1989年3月
医学分类名称
- 肾上腺皮质激素制剂
批准,等等
- 销售名称
- 氢化核酸盐Na Interasiton 100mg“ AFP”
销售名称代码
- 2452402A1095
批准 /许可号码
- 批准编号
- 22700AMX00099000
- 商标
- 用于静脉注射的磷酸氢可软酮
药品价格标准日期
- 2015年6月
销售日期
- 1978年6月
储蓄,到期日期等
- 储蓄
- 避免阴影,室温存储(1至30°C),冷冻。
- 截止日期
- 在包装中显示的到期日期内使用。
- 笔记
- 参考处理预防措施
法规类别
- 处方药
- 预防措施 - 通过医生等处方使用
构图 /特性表
| 销售名称 | 氢化核酸盐NA静脉液体100mg“ AFP”:
100mg(在1个Ammunul中) |
| 活性成分:氢化核酸盐(日本局) | 134.2mg(100mg作为氢化皮层) |
| 添加剂:木糖醇(日本局) | 40.0mg |
| 添加剂:氯化苯盐(日本局) | 0.2mg |
| 添加剂:柠檬酸钠水合物(日本局) | 20.0毫克 |
| 添加剂:pH调节器 | 适当的金额 |
| 药物 | 安瓿 |
| 容量 | 2ml |
| 特点 | 无色至浅黄色透明水的注入溶液 |
| ph | 7.5-8.5 |
| 渗透比率 | 1.6-2.0 |
- 销售名称
- Hydocorchizonolinate Na NA 500mg“ AFP”
销售名称代码
- 2452402A5112
批准 /许可号码
- 批准编号
- 22700AMX00100000
- 商标
- 用于静脉注射的磷酸氢可软酮
药品价格标准日期
- 2015年6月
销售日期
- 1978年6月
储蓄,到期日期等
- 储蓄
- 避免阴影,室温存储(1至30°C),冷冻。
- 截止日期
- 在包装中显示的到期日期内使用。
- 笔记
- 参考处理预防措施
法规类别
- 处方药
- 预防措施 - 通过医生等处方使用
构图 /特性表
| 销售名称 | Hydocorchizonolinate Na Na Na 500mg“ AFP”:
500mg(1个小瓶) |
| 活性成分:氢化核酸盐(日本局) | 671.0mg(500mg作为氢化软管) |
| 添加剂:木糖醇(日本局) | 200.0mg |
| 添加剂:氯化苯盐(日本局) | 1.0毫克 |
| 添加剂:柠檬酸钠水合物(日本局) | 100.0mg |
| 添加剂:pH调节器 | 适当的金额 |
| 药物 | 小瓶 |
| 容量 | 10毫升 |
| 特点 | 无色至浅黄色透明水的注入溶液 |
| ph | 7.5-8.5 |
| 渗透比率 | 1.6-2.0 |
一般名称
- 氢化核酸盐注射溶液
限制(请勿对下一个患者进行管理)- 1。
- 对该药物成分过敏的患者
- 2。
- *接受乙酸盐乙酸盐水合物的患者(由于男性夜间多尿引起的夜尿)[请参见“相互作用”]
|
原则上是禁忌的(原则上,它不会对下一个患者进行管理,但请在必要时仔细管理)- 1。
- 没有有效抗菌剂的感染,整个身体具有ICOSY的患者。这是给出的
- 2。
- 患有急性心肌梗塞的患者[据报道,这会导致破裂。这是给出的
|
功效或效果
功效或效果 /用法和剂量
- 手术冲击和冲击中的紧急或术后冲击
- 根据症状和病例,每天或每天几次将其静脉注射或静脉内注射或静脉注射2至20 mL(作为氢化软件100至1,000 mg)。
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 消化溃疡的患者[由于粘膜防御能力的降低,消化溃疡可能加剧。这是给出的
- 2。
- 糖尿病患者[促糖促进(血糖水平)等可能加剧糖尿病。这是给出的
- 3。
- 传染病患者[免疫抑制作用可能导致传染病值得。这是给出的
- 四个。
- 结核病患者[免疫抑制作用可能导致结核病病加剧。这是给出的
- 五。
- 简化的角质炎患者[免疫抑制作用可能导致角质炎可能加剧。这是给出的
- 6。
- 骨质疏松症的患者[骨质疏松症可能通过引起骨形成抑制和代谢而加剧。这是给出的
- 7。
- 精神病患者[影响中枢神经系统,并可能加剧精神疾病。这是给出的
- 8。
- 后肉可肌肉的患者[影响晶状体纤维,并可能加剧后囊白色白内障。这是给出的
- 9。
- 青光眼患者[起因增加,青光眼可能更糟。这是给出的
- 十。
- 肾衰竭的患者[症状可能恶化。这是给出的
- 11。
- 高血压[钠,储能作用等的患者可能导致高血压。这是给出的
- 12。
- 电解患者[钠 /储水作用可能导致电解异常加剧。这是给出的
- 13。
- 心力衰竭的患者[钠,储水等可能会导致血腥的心脏失败。这是给出的
- 14。
- 甲状腺功能低下的患者[观察到血液的一半寿命的延伸,并且可能发生副作用。这是给出的
- 15。
- 肝硬化患者[在慢性肝病患者中,表现出一半的血液,可能会发生副作用。这是给出的
- 16。
- 脂肪肝的患者[影响脂质代谢,并可能加剧脂肪肝。这是给出的
- 17。
- 脂肪菌病的患者这是给出的
- 18。
- 严重肌肉的患者这是给出的
- 19。
- 老年人[请参阅“老年人行政”部分]
重要的基本预防措施
- 1。
- 由于服用了这种药物,可能会发生严重的副作用,例如诱导的感染,非疾病皮层功能,消化溃疡,糖尿病,精神疾病等,因此可能需要为该药物施用以下预防措施。这是。
- (1)
- 该药物的高剂量给药通常在48至72小时内,如果批准冲击,则应立即停止管理。
- (2)
- 连续使用后,如果政府突然停止,有时可能会出现发烧,头痛,厌食,弱点,肌肉疼痛,关节疼痛,震动等,因此逐渐停止。 。如果出现戒断症状,请立即重新加入或增加。
- 2。
- 乙型肝炎病毒载体的患者可能是由皮质类固醇给药的,可能是丙型肝炎丙型肝炎病毒引起的。请注意丙型肝炎病毒增殖的体征和症状,例如在给药期间和该药物给药结束时,肝功能测试值和肝炎病毒标志物。如果发现异常,请采取适当的措施,例如考虑到该药物的体重减轻,以施用抗病毒剂。对于HBS抗原阴性患者,在服药开始之前,已经报道了丙型肝炎病毒。
- 3。
- 对于该药物的长期或大规模给药,或在该药物取消后的六个月内,免疫功能可能会降低,而原始疫苗的疫苗接种可能会增加或维持疫苗衍生的感染。因此,请勿接种这些患者的原始疫苗。
- 四个。
- 特别是,必须支付以下预防措施,因为在这种药物期间用水痘或麻疹感染可能导致致命病程。
- (1)
- 在服用该药物之前,请检查水痘或麻疹病史以及疫苗接种的存在或不存在。
- (2)
- 在没有水痘或麻疹病史的患者中,始终需要充分考虑和观察,以防止水痘或麻疹感染。如果怀疑感染或感染感染,请立即指导咨询并采取适当的措施。
- (3)
- 应该注意的是,水痘或麻疹可能有水痘,麻疹或疫苗接种的病史,因为该药物可能会出现水痘或麻疹。
相互作用
*联合用途的禁忌症(不要一起使用)- 毒品名称,等等
- 乙酸盐水合物(Minimin Melt)(夜间在男人的柱子上排尿)
- 临床症状 /度量方法
- 可能发生低钠血症。
- 机械 /危险因素
- 未知
|
**联合用途
(请注意联合使用)
- 1。药物名称等。BarbislicAcid衍生物:利利芬辛中的苯巴氏菌现象
- 临床症状 /度量方法
- 据报道,这种药物的作用减少。
- 机械 /危险因素
- 这些药物指导Chitochrome P450,促进该药物的代谢。
- 2。水杨酸衍生物,例如药物名称:阿司匹林
- 临床症状 /度量方法
- 据报道,它会增加在连续酸中连续酸衍生物中水杨酸衍生物的浓度,从而在组合时降低药物时会导致水杨酸中毒。
- 机械 /危险因素
- 该药物促进水杨酸衍生物中的肾脏排泄和肝代谢,从而降低了血清中水杨酸衍生物的浓度。
- 3。毒品名称等。抗果阿里亚:华尔法林钙
- 临床症状 /度量方法
- 据报道,它可以减少抗议机的作用。
- 机械 /危险因素
- 该药物具有血液凝血促进作用。
- 四个。口腔糖尿病,例如药物名称:乙酰六酰胺等。 <br>胰岛素制剂
- 临床症状 /度量方法
- 据报道,它可以减少这些药物的作用。
- 机械 /危险因素
- 该药物促进肝脏中的葡萄糖,并抑制在外周组织中使用糖的使用。
- 五。药物名称(不包括钾 - 持有利尿剂):三环形菌,氟胺等
β2-刺激性:Clemb Terrol盐酸盐,Trob Terrol盐酸盐,专业的Caterol盐酸盐酸盐盐酸盐,AM Hotelicinb- 临床症状 /度量方法
- 低钾血症可能是由于共同使用而引起的。
- 机械 /危险因素
- 该药物在尿管中具有钾的促进作用。
- 6。地高辛,等
- 临床症状 /度量方法
- 可能发生吉高素中毒。
- 机械 /危险因素
- 该药物的钾排泄作用可通过尿管降低,从而降低血液中的钾值并增加地高辛的作用。
- 7。毒品名称等。Sinakarcet
- 临床症状 /度量方法
- 血清钙浓度可能会降低。
- 机械 /危险因素
- Sinakar Seto的血钙降低了作用。
- 8。环孢素,例如药物名称
- 临床症状 /度量方法
- 据报道,大量皮质类固醇增加了使用的环孢菌素的血液浓度。
- 机械 /危险因素
- 它阻碍了环孢菌素的代谢。
- 9。药物名称等。大环内酯类抗生素:红霉素
雌激素(包括口服避孕药)- 临床症状 /度量方法
- 据报道,肾上腺皮质激素剂增强了这种作用。
- 机械 /危险因素
- 该药物的代谢可能被抑制。
- 十。麻黄碱等,例如药物名称
- 临床症状 /度量方法
- 据报道,皮质类固醇的代谢被促进,血液浓度降低。
- 机械 /危险因素
- 未知
- 11。绘制的名称等
- 临床症状 /度量方法
- 可能会发生消化系统(消化溃疡,消化管出血等)的副作用。
- 机械 /危险因素
- 两者都可能具有消化系统的副作用。
副作用
概述表达状态,副作用
- 该药物不进行调查,以阐明副作用的频率,例如用法调查。
严重的副作用
由于可能会出现以下副作用,因此,如果出现症状,请停止给药并采取适当的措施。 1.探索传染病和传染病未知频率可能发生偶然感染和传染病。肝炎可能是由于乙型肝炎病毒的增殖。如果发现异常,请进行足够的观察并采取适当的措施。 2.连续的肾上腺皮质功能障碍,糖尿病未知频率3.消化溃疡未知频率4.心理调制,抑郁状态未知频率5.骨质疏松症,股骨和乳糖的灭菌坏死,幼虫病未知频率6.青光眼,后囊白内障未知频率希望进行定期检查,因为它可能会增加眼内压,青光眼和后囊白疾病。 7.震惊未知频率过敏反应可能出现。另一个副作用
- 如果有以下症状或异常,请采取适当的措施,例如中断给药。
- 1.内分泌
- 未知频率
- 月经异常
- 2.消化
- 未知频率
- 不好的头脑 /呕吐
- 3.精神病神经系统
- 未知频率
- Taiki,失眠,头痛
- 4.肌肉 /骨骼
- 未知频率
- 肌肉疼痛,关节疼痛
- 5.脂质 /蛋白质代谢
- 未知频率
- 脸 - 脸,氮平衡平衡
- 6.体液 /电解质
- 未知频率
- 水肿,血压升高,碱性低钾
- 7.眼睛
- 未知频率
- 由于中央蛇状海豚瘤等引起的视网膜疾病,伸出了眼球
- 8.血液
- 未知频率
- 白细胞
- 9.皮肤
- 未知频率
- 缓慢的愈合障碍,痤疮,瘙痒,刺激,脂肪炎
- 10.其他
- 未知频率
- 发烧,疲劳
老年人的管理
- 如果您长时间给予老年人,则很可能会出现副作用,例如诱发感染性疾病,糖尿病,骨质疏松症,高血压,后囊性白内障,青光眼等。
管理孕妇,妇产科妇女等。
- 仅当确定治疗的治疗超过孕妇或可能怀孕的妇女的危险时,才应进行管理。 [动物实验报告了巨大的作用,并可能导致新生儿肾上腺失败。这是给出的
给儿童的管理等
- 1。
- 由于可能发生了抑制儿童的生长,因此会仔细观察。
- 2。
- 在长期给药的情况下,可能会出现颅内内压。
- 3。
- **据报道,在新生儿和婴儿中发生短暂性肥大性心肌病1) ,因此在这种药物给药之前和期间,进行心脏功能测试(Echo等)进行监测,以完全观察孩子的病情。
适用的预防措施
- 1.在管理时
- 在静脉内给药,血管疼痛,静脉炎,心律不齐或循环崩溃中,因此请谨慎注射部位,注射方法等,以防止这种情况,并尽可能降低注射速度。
- 2.管理路线
- 请勿将这种药物用于眼科。
药物
- 1.循环作用2)
- 根据Lillehei和其他人的说法,在休克和放松失衡时,组织变得不平衡。结果,整个身体的生长,周围耐药性的生长以及心率的降低。皮质类固醇激素(氢化核酸)的心率增加,降低周围血管耐药性,改善心肌收缩力,改善心肌收缩,并稳定这些休克症状的溶酶体膜。
- 2.对代谢的行动3)
- 根据Lefer和其他人的说法,对休克患者进行类固醇的血液乳酸降低。由于组织灌注降低而导致的厌氧代谢引起的血液泌乳值增加是一种正常的休克模式,而对休克的严重程度和预后,血液泌乳值的评估是一个重要的问题。
作为代谢作用,类固醇具有抑制休克期间组胺释放的功能。
有关活性成分的物理和化学知识
- 通用名称
- 磷酸氢化钠钠
- 化学名称
- 11β,17、21-三氧型元素4-烯-3、20-二酮21-(磷酸二钠)
- 结构公式
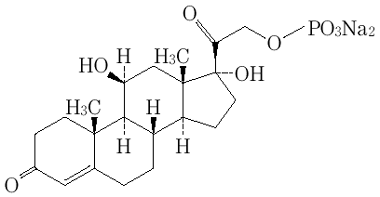
- 分子
- C 21 H 29 Na 2 O 8 P
- 分子量
- 486.40
- 性欲
- 它是白色至浅黄色粉末。
很容易溶于水,略微溶于甲醇,并且在乙醇中很难溶解(95)。
它是吸湿性的。
认识到晶体多态性。
处理的预防措施
- [稳定性测试]
- 由于使用最终包装产品的加速度测试(40°C,6个月)的结果,假定可以在阴影存储下保持稳定性。四)
- (1)
- 该药物是从无色到浅黄色的注射溶液。
- (2)
- 有时,随着时间的流逝,它可能无色至浅黄色,但不会影响质量。
包装
- 氢核酸盐NA静脉内100mg“ AFP” 2ML:10 apes
- 氢化酚酸酸Na Illanganate 500mg“ AFP” 10ml:5小瓶
主要文献和文档请求目的地
主要文献
- 1)
- ** Vimala,J。等人,Int JCardiol。2011; 150(3):E94-5
- 2)
- Lillehei,RC等人:Ann.Surg。,160,682(1964)
- 3)
- Lefer,Am等人:Clin。Pharmacol.ther。,11,630(1970)
- 四)
- Co -Creation Future Farm Co.,Ltd。:稳定材料(在房屋材料中)
*文献请求目的地
- 请在主要文档中描述的房屋材料中索取以下内容。
Alfressa Pharma Co.,Ltd。产品信息部 - 540-8575 2-2-2,伊乔,大阪的库 - 库
- 电话06-6941-0306
- 传真06-6943-8212
制造商等的姓名或名称和地址等。
- 卖方
- Alfressa Pharma Co.,Ltd。
- 2-2-19 Ishicho,Chuo -Ku,大阪
- 制造和分销商
- Co -Creation Future Pharma Co.,Ltd。
- 1-4-4 Hirocho,Shinagawa-ku,东京