4006 776 356
免费咨询 9:00-18:00
获取国外Imida Fenacin Kata 0.1mg“ Sawai” / Imida Fenacin O药品价格,使用等信息,最快 24 小时回馈
出境医 / 海外药品 / Imida Fenacin Kata 0.1mg“ Sawai” / Imida Fenacin O
Imida Fenacin Kata 0.1mg“ Sawai” / Imida Fenacin O
2020年6月
Imida Fenacin片0.1mg“ Sawai” / Imida Fenacin OD片0.1mg“ Sawai”
创建或修订年
- 创建于2020年3月(第一版)
日本标准产品分类编号
- 87259
医学分类名称
- 过度活跃的膀胱疗法
批准,等等
- 销售名称
- Imida fenacin片0.1mg“ sawai”
销售名称代码
- 2590013F1078
批准 /许可号码
- 批准编号
- 30200AMX00199000
- 商标
- 咪达法辛片[sawai]
药品价格标准日期
- 2020年6月
销售日期
- 2020年6月
储蓄,到期日期等
- 储蓄
- 室温存储(密封容器)
- 截止日期
- 显示在外盒子上
法规类别
- 处方药
- 预防措施 - 通过医生等处方使用
构图与性表
·作品
| 活性成分[1片] | 添加剂 |
| Imida fenacin 0.1mg | 基于α的淀粉,纤维素晶体纤维素,氧化钛,铁二,硬脂酸含量,tark二氧化衣,乳糖,羟基丙糖,羟丙糖 |
・配方的特征
| 外形 | 药物 | 特点 | 直径(mm) | 厚度(mm) | 重量(毫克) | 身体指标 |
 | 膜涂料锁 | 浅红色 - 红色红色棕色或浅红色紫色 | 7.2 | 3.4 | 大约138 | Imida Fenacin 0.1 Sawai |
- 销售名称
- Imida fenacin OD片剂0.1mg“ sawai”
销售名称代码
- 2590013F2082
批准 /许可号码
- 批准编号
- 30200AMX00154000
- 商标
- 伊发展苯二酚OD片[sawai]
药品价格标准日期
- 2020年6月
销售日期
- 2020年6月
储蓄,到期日期等
- 储蓄
- 室温存储(密封容器)
- 截止日期
- 显示在外盒子上
法规类别
- 处方药
- 预防措施 - 通过医生等处方使用
构图与性表
·作品
| 活性成分[1片] | 添加剂 |
| Imida fenacin 0.1mg | 跨杆菌,晶体纤维素,硬脂酸含量,羟丙基,d-甘露醇 |
・配方的特征
| 外形 | 药物 | 特点 | 直径(mm) | 厚度(mm) | 重量(毫克) | 身体指标 |
 | 米片(口腔塌陷片) | 白色的 | 7.0 | 3.5 | 大约150 | Imida Fenacin OD0.1 Sawai |
一般名称
- 伊米达富纳辛的制剂
限制(请勿对下一个患者进行管理)- 1。
- 尿闭合患者[抗蛋白作用可减少排尿期间膀胱收缩,并可能恶化症状。这是给出的
- 2。
- 菌,十二个肠或肠道的患者受到阻塞,患有瘫痪的Ileus的患者。这是给出的
- 3。
- 胃肠道运动和紧张局势的患者已减少。这是给出的
- 四个。
- 闭角青光眼患者[抗磷脂作用可能会增加眼内压,并可能恶化症状。这是给出的
- 五。
- 严重肌肉的患者[抗酸素作用可能会恶化症状。这是给出的
- 6。
- 严重的心脏病患者[ECG异常(例如相促收术),症状可能恶化。这是给出的
- 7。
- 对该药物成分过敏的患者
|
功效或效果
- 迫在眉睫的排尿,尿液频繁,过度活跃的膀胱尿失禁
与效果相关的使用预防措施
- 1。
- 应用这种药物时,通过足够的访谈和类似的症状(例如尿路感染,尿道结石,膀胱癌和前列腺癌等新生物)证实临床症状。 。根据需要考虑专门测试。
- 2。
- 遵守较低的尿路阻塞性疾病(前列腺肥大等)的患者应优先考虑治疗。
用法和剂量
- 通常,早餐和晚餐后,早餐和晚餐后两次是伊米达富纳辛。如果效果不足,则可以每次增加剂量为0.2 mg,每天为0.4 mg作为Imida fenacin。
与使用和剂量有关的预防措施
- 1。
- 每天两次退出0.1 mg,作为Imida fenacin,如果没有足够的效果并且安全性没有问题,请考虑增加。 [尚未建立每天0.2 mg一次启动一次0.2 mg时,该药物的功效和安全性尚未确定。这是给出的
- 2。
- 对于中度或更高肝损伤的患者,每天两次给药0.1 mg。 (请参阅有关“谨慎行政”的部分)
- 3。
- 对于严重肾功能不全的患者,每天两次给药0.1 mg。 (请参阅有关“谨慎行政”的部分)
使用预防措施
谨慎的管理
(请小心地给下一个患者管理)
- 1。
- 排尿困难的患者[抗蛋白作用可能会使症状恶化。这是给出的
- 2。
- 心律不齐的患者。这是给出的
- 3。
- 肝损伤的患者[主要在肝脏中代谢,因此副作用可能更有可能出现。这是给出的
- 四个。
- 肾脏疾病的患者[肾脏排泄可能会延迟。这是给出的
- 五。
- 痴呆或认知功能障碍的患者。这是给出的
- 6。
- 帕金森症状或脑血管疾病的患者这是给出的
- 7。
- 溃疡性结肠炎患者[可能发生有毒巨型结肠。这是给出的
- 8。
- 甲状腺功能亢进症的患者[抗蛋白作用可能会恶化诸如心动过速等交感神经症状。这是给出的
重要的基本预防措施
- 1。
- 对于尿路阻塞性较低的患者,例如前列腺增生,在服用该药物之前进行生存尿液测量,并根据需要进行专门测试。给药后,请注意不要增加残余尿液的量,并遵循足够的跟随。
- 2。
- 服用这种药物的患者应注意伴随着药物操作的机器操作,例如驾驶汽车,因为它可能会引起愤怒的疾病(清晰,雾,眼睛的视力,眼睛异常,眼睛异常,等),头晕和嗜睡。
- 3。
- 痴呆或认知功能障碍的患者无法清楚地识别出过度活跃的膀胱症状。
- 四个。
- 如果该药物的给药未识别出效果,请考虑适当的治疗而无需给予。
- 五。
- OD片剂(口腔塌陷片)在口腔中塌陷,但没有从口腔粘膜中吸收,因此它们被唾液或水吞咽。 (请参阅有关“适用预防措施”的部分)
相互作用
- 该药物主要由肝脏药物代谢酶CYP3A4和UGT1A4代谢。
合并用途的注释
(请注意联合使用)
| 毒品名称,等等 | 临床症状 /度量方法 | 机械 /危险因素 |
| 抑制CYP3A4 Itlaconazole Ellislomai Synclomycin等的化学物质等。 | 据报道,这种药物的CMAX与健康成年男性中的Itlaconazole一起使用了约1.3倍,而AUC的CMAX升高了约1.8倍。 | 由于该药物主要在CYP3A4中代谢,因此这些药物被抑制了该药物的代谢。 |
| 基于抗抗组织药物的抗组织药物抗抑郁药抗抑郁药基于基于阳极阳极的药物氧化物抑制作用 | 副作用,例如干口,口中干燥,便秘和排尿困难,可能会出现强烈的副作用。 | 抗胆碱作用得到增强。 |
副作用
概述表达状态,副作用
- 该药物不进行调查,以阐明副作用的频率,例如用法调查。
严重的副作用
(频率未知)- 1。
- 急性青光眼:眼内压力增加,据报道会产生急性青光眼,因此应观察到足够的观察,如果出现这种症状,请停止给药并立即采取适当的措施。
- 2。
- 关闭尿液:可能会仔细观察尿液,如果出现症状,请停止给药并采取适当的措施。
- 3。
- 肝功能障碍:AST(GOT),ALT(GPT),胆红素等可能会出现,因此进行了足够的观察,如果发现异常,则停止使用并立即采取给药。应采取适当的措施。
严重的副作用(药物类似)
- 1。
- 瘫痪的回肠:有一份报告说,瘫痪的肠胃出现在类似的化合物中(其他频繁的泌尿治疗剂)。应采取适当的措施。
- 2。
- 幻觉和del妄:有报道称幻觉和del妄出现在类似的化合物中(其他频繁的泌尿疗法),因此,如果出现这种症状,请务必观察它们并停止给药。
- 3。
- QT延伸,心室心动过速:有报道称QT延伸,心室心动过速,管状块,心动过缓等出现在类似的化合物(其他频繁的排尿剂)中,因此是这种情况。措施。
另一个副作用
| 未知频率 |
| 高敏注意) | 皮疹,所以发痒,等等。 |
| 精神科 | 嗜睡,味道异常,头晕,头痛,麻木,幻觉,妄想 |
| 消化器官 | 便秘,胃和腹部不适,恶心,腹痛,腹胀,腹泻,厌食症,消化不良,胃炎,呕吐,呕吐,粪便异常,口腔炎 |
| 心血管 | 心pit,相控制,血压升高 |
| 呼吸器官 | 喉痛,咳嗽,喉咙干,嘶哑 |
| 血 | 红细胞,白细胞还原,血小板还原 |
| 泌尿科 /肾脏 | 难度,残留尿液,尿血细胞,红细胞阳性,尿路感染(膀胱炎,肾盂肾炎等),尿蛋白阳性,clare chinin增加 |
| 眼睛 | 更少的,雾气,异常的眼睛,眼球干燥,眼睛疲劳,眼睑水肿,双视感 |
| 肝 | γ-GTP,碱性hosfatase,AST(GOT),ALT(GPT),胆红素的增加 |
| 其他的 | 口腔,干燥,甘油三酸酯干燥,肿胀,LDH增加,血液尿酸增加,不适,胸痛,背痛,无力,皮肤干燥。 |
- 注意)如果表达,请采取适当的措施,例如停用管理。
老年人的管理
- 通常,由于老年人的生理功能降低,因此仔细管理。
管理孕妇,妇产科妇女等。
- 1。
- 希望不对可能怀孕的孕妇或妇女进行管理。 [尚未确定怀孕期间的管理安全。已经向胎儿报告了动物实验(大鼠)。这是给出的
- 2。
- 希望不给护理妇女管理,但是如果您不可避免,请停止母乳喂养。 [据报道,动物实验(大鼠)正在转移到牛奶中。这是给出的
给儿童的管理等
- 尚未确定低出生体重,新生儿,婴儿,婴儿或儿童的安全性(没有经验)。
过量
- 1。
- 症状:关闭尿液,尖端,兴奋,心动过速等。
- 2。
- 行动:进行胃清洁或激活的木炭给药,然后进行与阿托蛋白过量的情况相同的处理。此外,根据每种症状进行适当的措施,例如尿液关闭的尿液推导,以及每种症状的Brust的焦油钙蛋白酶给药。
适用的预防措施
- 1。
- 在药物时:PTP包装中的药物应从PTP纸中取出并指示服用。 (据报道,PTP薄板的难度 - 到末期在食管粘膜上有一个尖锐的角,甚至是严重的并发症,例如纵隔炎)。
- 2。
- 服用时:
- (1)
- OD片剂(口腔塌陷片)放在舌头上,浸润的唾液,用舌头轻轻压碎,仅在倒塌后才能服用。也可以用水服用。
- (2)
- OD片剂(口腔塌陷片)在躺下时不应在没有水的情况下服用。
其他预防措施
- 据报道,在口服给药的小鼠或口中(30、100和300 mg/kg),在300 mg/kg的雄性和女性中观察到肝细胞瘤的增加。据报道,在癌症原始测试(3、7、15和30 mg/kg)中不允许肝细胞腺瘤的增加,该测试口服对大鼠口服两年。
药代动力学
- 生物当量测试○伊米达富甲酸片0.1mg“ sawai”
米达芬宁片0.1 mg的“ sawai”,标准制剂是健康的成年男孩(0.1 mg作为伊米达富纳辛)的片剂,在等离子体中测量了米达芬辛的密度。根据90%的信任部分法律所获得的药物体参数(AUC,CMAX)的统计分析的结果,它在日志(0.80)内(1.25)(1.25),并确认了两种药物的生物学等效物。已完成。 1) 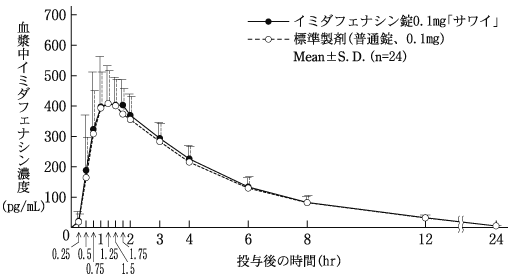
- ○Imida fenacin OD片剂0.1mg“ sawai”
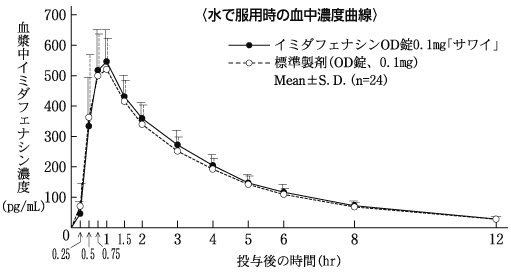
Imida fenacin OD片剂0.1 mg“ Sawai”,并将标准制剂用于健康的成年男孩(0.1 mg为Imida fenacin),并且在流氓中测量了咪达二芬法蛋白的捐赠。根据90%的信任部分法律所获得的药物体参数(AUC,CMAX)的统计分析的结果,它在日志(0.80)内(1.25)(1.25),并确认了两种药物的生物学等效物。已完成。 2) 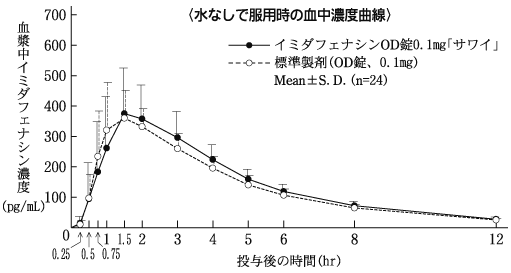
- 血浆浓度和参数(例如AUC和CMAX)可能会根据测试条件(例如选择受试者的选择,体内果汁的时间和时间的时间)而有所不同。
0.1 mg片剂1药代动力学参数在1片剂时
| cmax(pg/ml) | tmax(HR) | T 1/2 (HR) | AUC 0-24hr (pg/hr/ml) |
| Imida fenacin片0.1mg“ sawai” | 457±126 | 1.4±0.4 | 3.9±0.4 | 2209±451 |
| 标准准备(普通锁,0.1 mg) | 443±90 | 1.4±0.4 | 3.8±0.5 | 2132±459 |
(平均±SD,n = 24)
0.1mgod片剂1 1片剂用于药物的药物
| | cmax(pg/ml) | tmax(HR) | T 1/2 (HR) | AUC 0-12hr (pg/hr/ml) |
| 没有水 | Imida fenacin OD片剂0.1mg“ sawai” | 454±89 | 1.5±0.6 | 2.8±0.3 | 1754±253 |
| 没有水 | 标准制备(OD片剂,0.1 mg) | 410±71 | 1.5±0.6 | 2.9±0.3 | 1632±228 |
| 有水 | Imida fenacin OD片剂0.1mg“ sawai” | 566±119 | 1.0±0.3 | 2.9±0.4 | 1983±312 |
| 有水 | 标准制备(OD片剂,0.1 mg) | 558±134 | 0.9±0.2 | 3.0±0.4 | 1898±310 |
(平均±SD,n = 24)
药物
- 米达芬素是一种抗胆碱性药物,在毒素 - 性质乙酰胆碱(ACH)受体亚型中具有M 3和M 1受体。据认为,在副交感神经刺激引起的膀胱尖峰的收缩反应中,它不仅通过m 3受体显示拮抗作用,而且还可以在神经末端通过m 1受体抑制ACH的发挥。 3)
有关活性成分的物理和化学知识
- 通用名称
- 咪达芬辛
- 化学名称
- 4-(2-甲基-1 H -Imidazol-1-基)-2,2-二苯基丁酰胺
- 分子
- C 20 H 21 N 3 O
- 分子量
- 319.40
- 熔点
- 192-196℃
- 结构公式
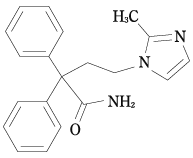
- 特点
- 它是白色晶体或结晶粉。溶解在乙酸(100)中,有点溶于甲醇,在某种程度上很难溶于乙醇(99.5),并且几乎不会溶于水中。
处理的预防措施
- ・稳定性测试片0.1 mg:由于加速器(40°C 75%RH,6个月),使用PTP包装(PTP纸包装铝制枕头包装)和玫瑰包装,在正常市场分布下稳定3年。成为。四)
- OD片剂0.1 mg:由于加速测试(40°C 75%RH,6个月),使用PTP包装(PTP纸包装铝制枕头包装),据推测,在正常市场分布下它是3年稳定的。场地。五)
包装
- Imida Fenacin片0.1mg“ Sawai”:
PTP:100片(10片X 10)
玫瑰:200片 - Imida Fenacin OD片0.1mg“ Sawai”:
PTP:100片(10片X 10),500片(10片X 50)
主要文献和文档请求目的地
主要文献
- 1)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 2)
- Sawai Pharmaceutical Co.,Ltd。in -House材料[生物当量测试]
- 3)
- Fumiyoshi Kobayashi等人,日本泌尿功能学会, 18 (2),292(2007)。
- 四)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
- 五)
- Sawai Pharmaceutical Co.,Ltd。 - 房屋材料[稳定性测试]
文学要求
- [请索取以下的主要文件(包括 - 房屋材料)]
Sawai Pharmaceutical Co.,Ltd.制药信息中心 - 532-0003 532-0003 Miyahara,Yodogawa-ku,大阪 - 2-30
- 电话:0120-381-999
- 传真:06-6394-7355
制造商等的姓名或名称和地址等。
- 制造和分销商
- Sawai Pharmaceutical Co.,Ltd。
- 5-130 Miyahara,大阪Yodogawa-ku