获取国外卢帕内塔背包药品价格,使用等信息,最快 24 小时回馈
卢帕内塔背包
什么是Lupaneta Pack?
Lupaneta Pack是用于治疗子宫内膜异位症(子宫外子宫内膜过度生长)症状的组合药物。
亮丙瑞林有助于治疗子宫内膜异位症引起的疼痛。
炔诺酮有助于防止骨骼变薄(亮丙瑞林的副作用)。
Lupaneta Pack不适用于65岁以上的女性。
Lupaneta Pack也可用于本用药指南中未列出的目的。
重要信息
如果您有以下情况,则不应使用Lupaneta Pack:未确诊的阴道出血,肝病或肝癌,或者曾经心脏病发作,中风,血液凝块或乳腺癌,子宫/宫颈癌或阴道癌。
如果您正在怀孕或哺乳,请不要使用。
在服药之前
如果您对亮丙瑞林或炔诺酮过敏,或者患有以下疾病,则不应使用这种药物:
未经医生检查的异常阴道出血;
肝病或肝癌;
有心脏病,中风或血液凝块的病史;要么
激素相关癌症或乳腺癌,子宫/子宫颈或阴道癌的病史。
告诉医生您是否曾经:
骨质疏松症或骨矿物质密度低(在您或家人中);
心脏问题,高血压,高胆固醇;
偏头痛;
癫痫;
萧条;
糖尿病;
肾脏疾病;要么
如果你抽烟。
开始此治疗之前,您可能需要接受阴性的妊娠试验。
如果您怀孕,请勿使用Lupaneta Pack。它可能会伤害未出生的婴儿或导致先天缺陷。使用这种药物时,请采取有效的节育措施以防止怀孕。如果您怀孕,请立即告诉您的医生。
接受亮丙瑞林注射液时,请勿使用荷尔蒙形式的避孕药(丸剂,注射剂,植入物,皮肤贴剂,阴道环)来防止怀孕。使用非激素避孕药,例如子宫内铜制器械(IUD)或避孕套或带有杀精子剂的隔膜。
Leuprolide可能会导致您在6个月的治疗期内不排卵或有月经期。但是,您仍然可以怀孕。
使用这种药物时请勿母乳喂养。
Lupaneta Pack未被18岁以下的任何人使用。
我应该如何服用Lupaneta Pack?
遵循处方标签上的所有说明,并阅读所有用药指南或说明表。完全按照指示使用药物。
该药物是联合治疗,包括亮丙瑞林注射液和炔诺酮片口服。医护人员会给您注射亮丙瑞林。您将在家服用炔诺酮片。
Leuprolide通常以每1至3个月单次注射到肌肉中的方式服用,最多6个月。注射亮丙瑞林后,每天需服用炔诺酮片1至3个月。
首次开始使用Lupaneta Pack时,您可能会出现子宫内膜异位症的症状加重。继续使用该药物后症状会改善。如果症状最终没有改善,请致电医生。
您将需要频繁的医学检查。
Lupaneta Pack可能会影响某些医学测试的结果。告诉任何治疗您的医生您正在使用Lupaneta Pack。
将炔诺酮片在室温下保存,远离湿气和热源。
根据您对Lupaneta Pack治疗的反应,您的医生可能希望您再接受6个月的治疗。
如果我错过剂量怎么办?
尽快服用错过的炔诺酮剂量,但如果您下一次服用的时间差不多了,则跳过错过的剂量。不要一次服用两剂。
如果您错过了亮丙瑞林注射剂的预约,请致电医生。
如果我服药过量怎么办?
寻求紧急医疗护理或致电1-800-222-1222,拨打毒药帮助热线。
使用Lupaneta Pack时应避免什么?
关于食物,饮料或活动的任何限制,请遵循医生的指示。
Lupaneta Pack的副作用
如果您有过敏反应迹象,请寻求紧急医疗救助:荨麻疹,皮肤发红,严重瘙痒;快速或剧烈的心跳;满头大汗,觉得自己可能会昏倒;喘息,呼吸困难;脸,嘴唇,舌头或喉咙肿胀。
如果您有垂体问题的征兆,请寻求医疗救助:头痛,视力问题,呕吐,精神状态变化,严重虚弱,皮肤发冷或发粘,脉搏微弱或感觉像病发作一样。
如果您有以下情况,请立即致电您的医生:
突然的视力问题,突然的眼睛改变或不适;
突然而剧烈的头痛;
情绪变化,抑郁
肿胀,体重迅速增加;
子宫内膜异位症的持续症状;
癫痫发作;
胸部疼痛或压力,疼痛蔓延到您的下巴或肩膀;
肝脏问题-食欲不振,胃痛(右上方),尿色深,黄疸(皮肤或眼睛发黄);要么
血块的迹象-突然的麻木或虚弱,视力或言语问题,手臂或腿肿胀或发红,咳嗽,喘息,咳血。
常见的副作用可能包括:
头痛;
弱点;
情绪低落
轻微的阴道流血或斑点,白带或瘙痒;
潮热,出汗;
恶心,呕吐,腹泻,便秘;
感到焦虑或紧张;
睡眠问题(失眠);
体重增加;要么
粉刺。
这不是副作用的完整列表,并且可能会发生其他副作用。打电话给您的医生,征求有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。
还有哪些其他药物会影响Lupaneta Pack?
告诉您的医生您所有其他药物的信息,尤其是:
癫痫发作药物;要么
类固醇(泼尼松和其他)。
此列表不完整。其他药物可能会影响Lupaneta Pack,包括处方药和非处方药,维生素和草药产品。此处未列出所有可能的药物相互作用。
版权所有1996-2018 Cerner Multum,Inc.版本:2.01。
注意:本文档包含有关亮丙瑞林/炔诺酮的副作用信息。此页面上列出的某些剂型可能不适用于Lupaneta Pack品牌。
综上所述
Lupaneta Pack的常见副作用包括:抑郁症和偏头痛。有关不良影响的完整列表,请参见下文。
对于消费者
适用于亮丙瑞林/去甲炔诺酮:悬浮粉1个月,悬浮粉3个月,片剂
需要立即就医的副作用
除其所需的作用外,亮丙瑞林/炔诺酮可能会引起一些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
服用亮丙瑞林/炔诺酮时,请立即咨询医生或护士是否出现以下任何副作用:
比较普遍;普遍上
- 哭泣
- 去个人化
- 烦躁不安
- 欣快感
- 温暖的感觉
- 精神抑郁
- 偏执狂
- 情绪上反应迅速或反应过度
- 快速变化的心情
- 脸部,脖子,手臂发红,偶尔上胸部发红
- 突然出汗
- 肿胀
发病率未知
- 焦虑
- 膀胱疼痛
- 血尿或浑浊
- 模糊的视野
- 胸痛
- 混乱
- 抽搐
- 咳嗽
- 黑尿
- 排尿困难,灼热或疼痛
- 说话困难
- 吞咽困难
- 头晕或头晕
- 双重视野
- 晕倒
- 快速的心跳
- 流感样症状
- 尿频
- 头痛
- 荨麻疹
- 无法移动手臂,腿部或面部肌肉
- 增加皮肤对阳光的敏感性
- 瘙痒
- 关节或肌肉疼痛或僵硬
- 下背部或侧面疼痛
- 恶心和呕吐
- 脸,手臂或腿麻木或刺痛
- 腹股沟或生殖器疼痛
- 手臂或腿部疼痛,发红或肿胀
- 敲打耳朵
- 眼睑或眼睛,面部,嘴唇或舌头周围浮肿或肿胀
- 皮肤发红
- 右上腹压痛
- 严重晒伤
- 肋骨下方剧烈的背部疼痛
- 皮疹
- 缓慢或快速的心跳
- 言语缓慢
- 突然呼吸急促或呼吸困难
- 出汗
- 自杀的想法或企图
- 胸闷
- 呼吸困难
- 睡眠困难
- 思维或行走困难
- 异常疲倦或虚弱
- 眼睛或皮肤发黄
不需要立即就医的副作用
可能会产生亮丙瑞林/炔诺酮的一些副作用,通常不需要医疗。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。
请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
比较普遍;普遍上
- 胃酸或酸
- 健忘
- ching
- 出血,起泡,灼热,寒冷,皮肤变色,压力感,荨麻疹,感染,炎症,瘙痒,肿块,麻木,疼痛,皮疹,发红,疤痕,酸痛,刺痛,肿胀,触痛,刺痛,溃疡,或注射部位的温度
- 皮肤上的斑点
- 肿胀或饱满的感觉
- 灼烧,爬行,发痒,麻木,刺,“针刺”或刺痛感
- 食欲变化
- 对性交的兴趣减少
- 腹泻
- 排便困难(凳子)
- 胃或肠中过量的空气或气体
- 自我或周围环境不断运动的感觉
- 脱发或头发稀疏
- 头痛,剧烈和跳动
- 胃灼热
- 无法勃起或勃起
- 消化不良
- 力量不足或丧失
- 性能力,欲望,动力或表现丧失
- 乳房疼痛或压痛
- 通过气体
- 青春痘
- 旋转感
- 胃部不适,不适或疼痛
- 体重增加
不常见
- 遗漏或月经不调
- 阴道或生殖器部位瘙痒
- 性交时的疼痛
- 停止月经出血
- 白带厚实,白带,无异味或有轻微气味
对于医疗保健专业人员
适用于亮丙瑞林/炔诺酮:口服和注射试剂盒
一般
导致治疗中断的最常见不良反应包括潮热(4%),情绪不稳(4%),抑郁症(4%)和痤疮(2%)。
观察到的最常见的不良反应是潮热和头痛。 [参考]
心血管的
亮丙瑞林-去甲炔诺酮:
很常见(10%或更多):潮热/汗水(高达87%)
亮丙瑞林:
非常常见(10%或更多):潮热/汗水(98%)
售后报告:低血压,高血压,严重的静脉和动脉血栓形成和血栓栓塞事件(深静脉血栓形成,肺栓塞,心肌梗塞,中风,短暂性脑缺血发作[参考]
皮肤科
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更多):雄激素样效应(痤疮,脱发)(高达18%),皮肤/粘膜反应(高达11%)
亮丙瑞林:
常见(1%至10%):类雄激素作用(痤疮,脱发)(4%),皮肤/粘膜反应(4%) [参考]
胃肠道
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更多):肠功能改变(便秘,腹泻)(高达15%),恶心/呕吐(高达29%)
常见(1%至10%):胃肠道疾病(消化不良,肠胃气胀)(最高7%),食欲变化(6%)
亮丙瑞林:
非常常见(10%或更多):恶心/呕吐(25%),肠功能改变(便秘,腹泻)(14%)
常见(1%至10%):食欲变化(4%)%,胃肠道疾病(消化不良,肠胃气胀)(4%) [参考]
泌尿生殖
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更高):阴道炎(高达15 %%),乳房变化/疼痛/压痛(高达13%)
常见(1%至10%):月经失调(5%)
未报告频率:尿路感染
亮丙瑞林:
非常常见(10%或更多):阴道炎(20%)
常见(1%至10%):乳房变化/疼痛/压痛(6%),月经紊乱(2%) [参考]
血液学
亮丙瑞林:
上市后报告:白血球减少[参考]
肝的
亮丙瑞林:
上市后报告:严重肝损伤
亮丙瑞林-去甲炔诺酮:
常见(1%至10%):SGPT升高(至少是上限的两倍)(2%),GGT升高(1.5%) [参考]
过敏症
亮丙瑞林-去甲炔诺酮:
上市后报告:过敏反应(过敏,皮疹,荨麻疹,光敏性) [参考]
本地
亮丙瑞林-去甲炔诺酮:
常见(1%至10%):注射部位反应(高达9%)
亮丙瑞林:
普通(1%至10%):注射部位反应(2%)
上市后报告:注射部位的硬结和脓肿等局部反应[参考]
新陈代谢
亮丙瑞林-去甲炔诺酮:
很常见(10%或更多):体重增加(最高13%)
常见(1%至10%):水肿(高达9%),SGPT升高(至少是上限的两倍)(2%),GGT升高(1.5%)
未报告的频率:总胆固醇升高(大于240 mg / dL),HDL胆固醇降低(小于40 mg / dL),LDL胆固醇升高(大于160 mg / dL),LDL / HDL比升高(大于4) ,甘油三酸酯增加(大于200 mg / dL)
亮丙瑞林:
常见(1%至10%):体重增加(12%) [参考]
肌肉骨骼
亮丙瑞林:
上市后报告:脊柱骨折,腱鞘炎样症状,与纤维肌痛一致的症状[参考]
神经系统
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更多):头痛/偏头痛(高达51%),失眠/睡眠障碍(高达15%),头晕/眩晕(高达11%)
常见(1%至10%):神经肌肉疾病(腿抽筋,感觉异常)(高达9%),性欲降低(高达7%),记忆障碍(高达4%)
亮丙瑞林:
非常常见(10%或更多):头痛/偏头痛(65%),失眠/睡眠障碍(31%),头晕/眩晕(16%),性欲下降(10%)
常见(1%至10%):记忆障碍(6%),神经肌肉疾病(腿抽筋,感觉异常)(2%)
上市后报道:垂体中风,惊厥,周围神经病,麻痹[参考]
其他
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更多):疼痛(最高29%),乏力(最高18%)
亮丙瑞林:
非常常见(10%或更高):疼痛(24%),乏力(18%)
精神科
亮丙瑞林-去甲炔诺酮:
非常常见(10%或更多):抑郁/情绪不佳(高达34%),神经质/焦虑症(高达11%)
亮丙瑞林:
很常见(10%或更多):抑郁/情绪不稳定(31%)
常见(1%至10%):神经质/焦虑症(8%)
上市后报告:情绪波动,自杀意念和尝试[参考]
肾的
亮丙瑞林-去甲炔诺酮:
未报告频率:肾结石[参考]
呼吸道
亮丙瑞林:
上市后报告:与哮喘过程一致的症状[参考]
参考文献
1.“产品信息。LupanetaPack(亮丙瑞林-炔诺酮)。”伊利诺伊州Abbott Park的Abbott Pharmaceutical。
某些副作用可能没有报道。您可以将其报告给FDA。
醋酸亮丙瑞林注射液的重组和给药
- 重构并以单次肌内注射方式给药冻干微球。
- 立即注射混悬液,如果两小时内未使用,则将其丢弃,因为用于仓库悬浮液的醋酸亮丙瑞林不含防腐剂。
- 目视检查醋酸亮丙瑞林中的悬浮液粉末。如果明显结块或结块,请勿使用注射器。在与稀释剂混合之前,注射器壁上的粉末薄层被认为是正常的。稀释剂应看起来清晰。
- 为了准备进样,将白色柱塞拧入末端塞子,直到塞子开始转动(见图1和图2)。
图1:
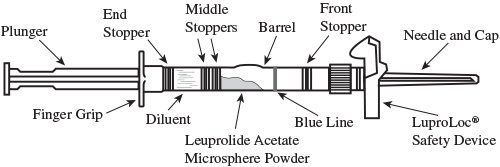
图2:
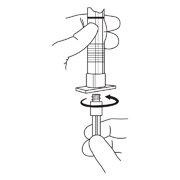
- 保持注射器直立。缓慢推入柱塞(6至8秒钟)以释放稀释剂,直到第一个中间塞子位于桶中部的蓝线处(见图3)。
图3:
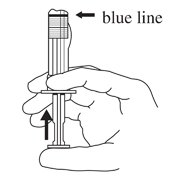
- 保持注射器直立。轻轻摇动注射器,直到粉末形成均匀的悬浮液,以充分混合微球(粉末)。悬浮液将呈现乳白色。如果粉末粘附在塞子上或出现结块/结块,请用手指轻击注射器以使其分散。如果任何粉末未悬浮,请勿使用(参见图4)。
图4:
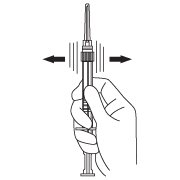
- 保持注射器直立。用另一只手向上拉动针帽,不要扭曲。
- 保持注射器直立。推动柱塞以排出注射器中的空气。现在注射器已准备好进行注射。
- 用酒精棉签清洁注射部位后,将针头以90度角插入臀区域,大腿前部或三角肌进行肌肉注射(请参见图5)。
图5:
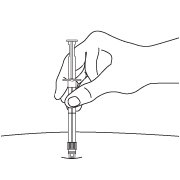
注意:如果不小心穿透了血管,则在鲁尔锁下面(参见图6)可以看到抽吸的血液,并且可以通过透明的LuproLoc安全装置看到。如果有血液,请立即取下针头。不要注射药物。
图6:
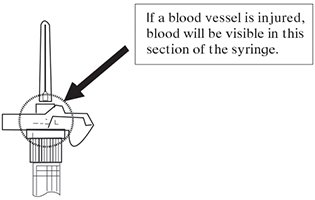
- 肌肉注射注射器的全部内容物。
- 拔针。一旦注射器已被撤回,立即通过按压箭头上的锁向上朝向针尖用拇指或手指,如图所示激活LuproLoc®安全装置中,直到在针安全装置的针盖完全伸出和听到或感觉到“咔嗒”声(见图7)。
图7:
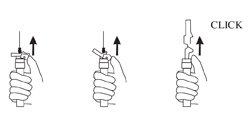
- 根据当地法规/程序处理注射器[请参阅参考文献(15)] 。
Lupaneta Pack的适应症和用法
Lupaneta Pack(用于贮存悬浮液的醋酸亮丙瑞林和醋酸炔诺酮片)适用于子宫内膜异位症的痛苦症状的初步治疗和症状复发的治疗。
使用限制:由于担心对骨矿物质密度的不利影响,使用期限受到限制[请参阅警告和注意事项(5.1) ] 。 Lupaneta Pack的初始治疗过程为六个月。如果症状复发,则在最初的治疗过程后可以进行不超过六个月的单次治疗。不建议使用Lupaneta Pack超过12个月。
卢帕内塔包装剂量和给药
剂量信息
Lupaneta Pack是醋酸亮丙瑞林用于肌肉注射的悬浮液和醋酸炔诺酮片剂的共同包装。管理如下:
- 每三个月一次肌肉注射11.25 mg醋酸亮丙瑞林,最多两次注射(治疗6个月);由医疗保健提供者管理
- 每天一次口服5毫克乙酸炔诺酮,最多治疗6个月
醋酸亮丙瑞林用于口服混悬液11.25 mg每天与醋酸炔诺酮5 mg联合治疗的初始过程不得超过六个月。
如果子宫内膜异位症的症状在最初的治疗过程后再次出现,请考虑使用Lupaneta Pack进行长达六个月的再治疗。建议在开始再治疗之前评估骨密度[见警告和注意事项(5.1) ] 。
由于担心对骨矿物质密度的不利影响,尚未研究超过两个六个月疗程的治疗方法,因此不建议进行治疗。
醋酸亮丙瑞林的不同配方
由于不同的释放特性,用于贮库悬浮液3个月贮库制剂的乙酸乙酸亮丙瑞林的部分剂量不等于每月制剂的相同剂量,因此不应给予。
醋酸亮丙瑞林注射液的重组和给药
- 重构并以单次肌内注射方式给药冻干微球。
- 立即注射混悬液,如果两小时内未使用,则将其丢弃,因为用于仓库悬浮液的醋酸亮丙瑞林不含防腐剂。
- 目视检查醋酸亮丙瑞林中的悬浮液粉末。如果明显结块或结块,请勿使用注射器。在与稀释剂混合之前,注射器壁上的粉末薄层被认为是正常的。稀释剂应看起来清晰。
- 为了准备进样,将白色柱塞拧入末端塞子,直到塞子开始转动(见图1和图2)。
图1:

图2:

- 保持注射器直立。缓慢推入柱塞(6至8秒钟)以释放稀释剂,直到第一个中间塞子位于桶中部的蓝线处(见图3)。
图3:

- 保持注射器直立。轻轻摇动注射器,直到粉末形成均匀的悬浮液,以充分混合微球(粉末)。悬浮液将呈现乳白色。如果粉末粘附在塞子上或出现结块/结块,请用手指轻击注射器以使其分散。如果任何粉末未悬浮,请勿使用(参见图4)。
图4:

- 保持注射器直立。用另一只手向上拉动针帽,不要扭曲。
- 保持注射器直立。推动柱塞以排出注射器中的空气。现在注射器已准备好进行注射。
- 用酒精棉签清洁注射部位后,将针头以90度角插入臀区域,大腿前部或三角肌进行肌肉注射(请参见图5)。
图5:

注意:如果不小心穿透了血管,则在鲁尔锁下面(参见图6)可以看到抽吸的血液,并且可以通过透明的LuproLoc安全装置看到。如果有血液,请立即取下针头。不要注射药物。
图6:

- 肌肉注射注射器的全部内容物。
- 拔针。一旦注射器已被撤回,立即通过按压箭头上的锁向上朝向针尖用拇指或手指,如图所示激活LuproLoc®安全装置中,直到在针安全装置的针盖完全伸出和听到或感觉到“咔嗒”声(见图7)。
图7:

- 根据当地法规/程序处置注射器[请参见参考文献(15) ] 。
剂型和优势
Lupaneta Pack 3个月共包装套件包含两个单独的组件:
- 醋酸亮丙瑞林用于仓库悬浮液的11.25 mg的3个月给药:醋酸亮丙瑞林冻干粉,用预先填充的双室注射器中的稀释剂进行重构
- 醋酸炔诺酮5毫克片剂:白色至灰白色椭圆形,表面平整,斜面倒角,无涂层,一侧刻有“ G带断裂线”,另一侧刻有304
禁忌症
Lupaneta Pack在女性中禁忌以下:
- 对促性腺激素释放激素(GnRH),GnRH激动剂类似物,用于储存悬浮液的醋酸亮丙瑞林中的任何赋形剂或醋酸炔诺酮过敏
- 未确诊子宫异常出血
- 在治疗过程中已知,怀疑或计划怀孕[请参阅在特定人群中使用(8.1) ]
- 哺乳期妇女[见在特定人群中使用(8.3) ]
- 乳腺癌或其他激素敏感性癌症的已知,疑似或病史
- 血栓形成或血栓栓塞性疾病的当前或历史
- 肝肿瘤或肝病
警告和注意事项
骨矿物质密度的损失
用于储存库悬浮液的醋酸亮丙瑞林会引起低雌激素状态,从而导致骨矿物质密度(BMD)下降,其中一些可能不可逆。同时使用醋酸炔诺酮可以有效减少醋酸亮丙瑞林引起的骨密度损失[见临床研究(14) ] 。尽管如此,由于担心对BMD的不利影响,Lupaneta Pack的使用期限仅限于两个六个月疗程。建议在重新治疗之前评估BMD。不建议单独使用醋酸亮丙瑞林进行再处理,以免于停药。
对于具有降低BMD的主要危险因素的女性,例如长期饮酒(每天超过3个单位)或吸烟,骨质疏松症的家族病史悠久或长期使用可以降低BMD的药物(例如抗惊厥药或皮质类固醇),请使用Lupaneta Pack可能会带来额外的风险,因此应仔细权衡风险和收益。
怀孕风险
如果对孕妇给药,醋酸亮丙瑞林用于仓库的悬浮液可能会造成胎儿伤害。在开始使用Lupaneta Pack治疗之前,应排除妊娠。当以建议的剂量和给药间隔使用时,醋酸亮丙瑞林用于贮库混悬液通常会抑制排卵并停止月经。然而,避孕药不能通过将醋酸亮丙瑞林用于贮库混悬液来确保。因此,患者应使用非激素避孕方法。如果患者认为自己可能怀孕,则建议他们告知其医疗保健提供者。如果患者在治疗期间怀孕,请中止Lupaneta Pack并告知患者胎儿的潜在危险[参见禁忌症(4)和在特定人群中的使用(8.1) ] 。
5.3视觉异常
如果突然或部分丧失视力,或突然出现眼球突出,复视或偏头痛,则应停止在Lupaneta Pack中服用醋酸炔诺酮片,以待检查。如果检查发现乳头水肿或视网膜血管病变,请停用Lupaneta Pack。
临床抑郁症
用Lupaneta Pack治疗期间,抑郁可能会发生或恶化。仔细观察有临床抑郁史的患者,如果抑郁严重程度再次发作,请停用Lupaneta Pack。
严重的过敏反应
在Lupaneta Pack的临床试验中,有哮喘,鼻窦炎和环境或药物过敏史的女性中报告了哮喘的不良事件。上市后已有与过敏反应或哮喘过程一致的症状报道。
心血管和代谢紊乱
在开始使用Lupaneta Pack之前,应评估和管理心血管疾病的危险因素。严密监测使用乙酸炔诺酮的妇女,这些妇女在使用时具有动脉血管疾病(例如,高血压,糖尿病,吸烟,高胆固醇血症和肥胖)和/或静脉血栓栓塞(例如,VTE的家族病史,肥胖和吸烟)的危险因素Lupaneta Pack [参见禁忌症(4) ] 。
症状初期
首次服用醋酸亮丙瑞林后,由于该药物的生理作用,性类固醇暂时升高至基线以上。因此,在治疗的最初几天可能会观察到与子宫内膜异位症相关的症状增加,但是随着继续治疗,这些症状会消失。
体液潴留
由于乙酸炔诺酮可能会导致一定程度的体液滞留,因此请仔细观察可能受此效应影响的妇女,例如癫痫,偏头痛,心脏或肾脏功能障碍。
抽搐
上市后有关于醋酸亮丙瑞林治疗患者惊厥的报道。这些患者包括有无同时用药和合并症的患者。
不良反应
临床试验经验
由于临床试验是在广泛不同的条件下进行的,因此不能将在某种药物的临床试验中观察到的不良反应率直接与另一种药物的临床试验中观察到的不良反应率进行比较,并且可能无法反映在临床实践中观察到的不良反应率。
在两项临床研究中评估了醋酸亮丙瑞林和缓释醋酸炔诺酮合用的安全性,该研究共对242名妇女进行了长达一年的治疗。每月单独给IM注射醋酸亮丙瑞林3.75毫克(13次注射)或每月给IM注射醋酸亮丙瑞林3.75毫克(13次注射)和每天5 mg乙酸炔诺酮治疗。人口年龄范围为17-43岁。大多数患者是白种人(87%)。
一项研究是一项对照临床试验,其中106名妇女被随机分配到仅接受乙酸亮丙瑞德单独用于长效悬浮液治疗或接受乙酸亮丙瑞德单独进行长效悬浮液和醋酸炔诺酮治疗的一年。另一项研究是一项开放标签的单臂临床研究,该研究针对136名用醋酸亮丙瑞林用于贮库混悬液和醋酸炔诺酮的妇女治疗一年,完成治疗后长达12个月的随访。
不良反应(> 1%)导致研究中断:
在对照研究中,每月有18%的患者接受醋酸亮丙瑞林治疗,而18%的每月由醋酸亮丙瑞林加乙酸炔诺酮治疗的患者由于不良反应而停药,最常见的是潮热(6%)和失眠(4%)。醋酸亮丙瑞林组和醋酸亮丙瑞林和炔诺酮组的潮热和情绪不稳(各4%)。
在开放标签研究中,每月有13%的患者接受醋酸亮丙瑞林加醋酸炔诺酮的治疗由于不良反应而中断治疗,最常见的是抑郁症(4%)和痤疮(2%)。
常见不良反应:
表1列出了在附加临床研究中,在治疗的最初6个月中,在任何治疗组中至少5%的患者中观察到的不良反应,其中,患者每月接受醋酸亮丙瑞林口服缓释剂3.75 mg或无需醋酸炔诺酮共同处理。这些研究中观察到最常见的不良反应是潮热和头痛。
| *仅LA =醋酸亮丙瑞林3.75毫克 †LA / N =醋酸亮丙瑞林3.75 mg加醋酸炔诺酮5 mg | |||||||
| 表1.子宫内膜异位症≥5%的患者在治疗的头六个月发生不良反应 | |||||||
| 对照研究 | 开放标签研究 | ||||||
| 仅洛杉矶* | LA / N† | LA / N† | |||||
| N = 51 | N = 55 | N = 136 | |||||
| 不良反应 | ñ | % | ñ | % | ñ | % | |
| 任何不良反应 | 50 | 98 | 53 | 96 | 126 | 93 | |
| 身体整体 | |||||||
| 虚弱 | 18岁 | 18岁 | 11 | ||||
| 头痛/偏头痛 | 65岁 | 51 | 46 | ||||
| 注射部位反应 | 2 | 9 | 3 | ||||
| 疼痛 | 24 | 29 | 21 | ||||
| 心血管系统 | |||||||
| 潮热/汗水 | 98 | 87 | 57 | ||||
| 消化系统 | |||||||
| 肠功能改变(便秘,腹泻) | 14 | 15 | 10 | ||||
| 食欲变化 | 4 | 0 | 6 | ||||
| 胃肠道不适(消化不良,肠胃气胀) | 4 | 7 | 4 | ||||
| 恶心,呕吐 | 25 | 29 | 13 | ||||
| 代谢和营养失调 | |||||||
| 浮肿 | 0 | 9 | 7 | ||||
| 体重增加 | 12 | 13 | 4 | ||||
| 神经系统 | |||||||
| 抑郁/情绪不稳定 | 31 | 27 | 34 | ||||
| 头晕/眩晕 | 16 | 11 | 7 | ||||
| 失眠/睡眠障碍 | 31 | 13 | 15 | ||||
| 性欲减退 | 10 | 4 | 7 | ||||
| 记忆障碍 | 6 | 2 | 4 | ||||
| 神经/焦虑 | 8 | 4 | 11 | ||||
| 神经肌肉疾病(腿抽筋,感觉异常) | 2 | 9 | 3 | ||||
| 皮肤和附属物 | |||||||
| 雄激素样效应(痤疮,脱发) | 4 | 5 | 18岁 | ||||
| 皮肤/粘膜反应 | 4 | 9 | 11 | ||||
| 泌尿生殖系统 | |||||||
| 乳房变化/疼痛/压痛 | 6 | 13 | 8 | ||||
| 月经失调 | 2 | 0 | 5 | ||||
| 阴道炎 | 20 | 15 | 8 | ||||
在对照临床试验中,单独使用醋酸亮丙瑞林组的51名患者中有50名(98%),而醋酸亮丙瑞林和炔诺酮组中的55名患者中有48名(87%)报告在治疗过程中一次或多次出现潮热。表2列出了治疗第六个月的潮热数据。
| *仅LA =醋酸亮丙瑞林3.75毫克 †LA / N =醋酸亮丙瑞林3.75 mg加醋酸炔诺酮5 mg 1在统计上显着低于仅LA组(p <0.01) 2评估的患者人数。 | |||||||
| 表2.评估访视前一个月的潮热(对照研究) | |||||||
| 评估访问 | 治疗组 | 报告潮热的患者人数 | 潮热的天数 | 24小时内的最大潮热次数 | |||
| ñ | (%) | N 2 | 意思 | N 2 | 意思 | ||
| 第24周 | 仅洛杉矶* | 32/37 | 86 | 37 | 19 | 36 | 5.8 |
| LA / N† | 22/38 | 58 1 | 38 | 7 1 | 38 | 1.9 1 | |
严重不良反应:
尿路感染,肾结石,抑郁
治疗期间实验室值的变化:
肝酵素
在两项针对子宫内膜异位症女性的临床试验中,191名接受醋酸亮丙瑞林和醋酸炔诺酮的患者中有4名长达12个月的患者SGPT升高(至少是正常上限的两倍),而136名患者中有2例GGT升高。在治疗6个月后观察到6种增加中的5种。没有人与胆红素浓度升高有关。
血脂
下表概述了醋酸亮丙瑞林和醋酸炔诺酮的两项研究中血清脂质相对于基线的变化百分比以及血清脂质值超出正常范围的患者百分比。将乙酸炔诺酮添加到醋酸亮丙瑞林中以进行长效混悬液处理的主要影响是血清HDL胆固醇的降低和LDL / HDL比例的增加。
| *毫克/分升 †比率 | ||||||
| 表3.血脂:治疗第24周时与基线值相比的平均百分比变化 | ||||||
| 醋酸亮丙瑞林3.75毫克 | 醋酸亮丙瑞林用于仓库悬浮液3.75 mg + 乙酸炔诺酮每天5毫克 | |||||
| 对照研究 (n = 39) | 对照研究 (n = 41) | 开放标签研究 (n = 117) | ||||
| 基准线 值* | 周24 变化百分比 | 基准线 值* | 周24 变化百分比 | 基准线 值* | 周24 变化百分比 | |
| 总胆固醇 | 170.5 | 9.2% | 179.3 | 0.2% | 181.2 | 2.8% |
| 高密度脂蛋白胆固醇 | 52.4 | 7.4% | 51.8 | -18.8% | 51.0 | -14.6% |
| 低密度脂蛋白胆固醇 | 96.6 | 10.9% | 101.5 | 14.1% | 109.1 | 13.1% |
| LDL / HDL比 | 2.0† | 5.0% | 2.1† | 43.4% | 2.3† | 39.4% |
| 甘油三酸酯 | 107.8 | 17.5% | 130.2 | 9.5% | 105.4 | 13.8% |
在第52周时,自基线的变化趋于更大。治疗后,具有随访数据的患者(158名患者中的105名)的平均血脂水平恢复到治疗前的水平。
| *包括所有患者,无论基线值如何。 | ||||
| 表4.血脂值超出正常范围的患者百分比 | ||||
| 醋酸亮丙瑞林用于仓库悬浮液3.75 mg 加醋酸炔诺酮5毫克每天 | ||||
| 对照研究 (n = 41) | 开放标签研究 (n = 117) | |||
| 基准线 | 24周* | 基准线 | 24周* | |
| 总胆固醇(> 240 mg / dL) | 15% | 20% | 6% | 7% |
| HDL胆固醇(<40 mg / dL) | 15% | 44% | 15% | 41% |
| 低密度脂蛋白胆固醇(> 160 mg / dL) | 5% | 7% | 9% | 11% |
| LDL / HDL比(> 4.0) | 2% | 15% | 7% | 21% |
| 甘油三酸酯(> 200 mg / dL) | 12% | 10% | 5% | 9% |
上市后经验
在醋酸亮丙瑞林用于仓库混悬液或醋酸炔诺酮的批准后使用过程中,已经确认了以下不良反应。由于这些反应是从不确定大小的人群中自愿报告的,因此并非总是能够可靠地估计其发生频率或建立与药物暴露的因果关系。
醋酸亮丙瑞林用于仓库的悬浮
在使用相同或不同人群的其他剂型的上市后监测期间,报告了以下不良反应:
- 过敏反应(过敏,皮疹,荨麻疹和光敏反应)
- 情绪波动,包括抑郁
- 自杀念头和企图
- 与过敏样或哮喘过程一致的症状
- 注射部位的硬结和脓肿等局部反应
- 与纤维肌痛一致的症状(例如,关节和肌肉疼痛,头痛,睡眠障碍,胃肠道不适和呼吸急促)
报告的其他不良反应包括:
肝胆疾病-严重肝损伤
伤害,中毒和手术并发症-脊柱骨折
调查-白血球数量减少
肌肉骨骼和结缔组织疾病-腱鞘炎样症状
神经系统疾病-惊厥,周围神经病,瘫痪
血管疾病-低血压,高血压
严重的静脉和动脉血栓形成和血栓栓塞事件,包括深静脉血栓形成,肺栓塞,心肌梗塞,中风和短暂性脑缺血发作
垂体中风
在上市后监测期间,已报告了醋酸亮丙瑞林和其他GnRH激动剂给药后垂体中风(垂体梗死继发的临床综合征)病例。在大多数这些病例中,诊断为垂体腺瘤,大多数垂体中风病例在首次给药后2周内发生,有些在第一小时内发生。在这些情况下,垂体中风表现为突然的头痛,呕吐,视觉改变,眼肌麻痹,精神状态改变,有时甚至是心血管衰竭。需要立即就医。
药物相互作用
7.1药物相互作用
醋酸亮丙瑞林用于仓库的悬浮
尚未使用醋酸亮丙瑞林进行储库悬浮液的药代动力学研究。但是,与细胞色素P-450酶或蛋白质结合相关的药物相互作用不会发生[见临床药理学(12.3) ] 。
醋酸炔诺酮
尚未进行任何药代动力学药物相互作用研究,以研究乙酸炔诺酮与任何药物之间的相互作用。诱导或抑制某些酶(包括CYP3A4)的药物或草药产品可能会降低或增加炔诺酮的血清浓度。
药物/实验室测试的相互作用
醋酸亮丙瑞林用于仓库的悬浮
以治疗剂量施用醋酸亮丙瑞林用于贮库悬浮液可抑制垂体-性腺系统。通常在停药后三个月内恢复正常功能。因此,可能会影响在治疗期间以及停用醋酸亮丙瑞林用于停药后三个月内进行的垂体促性腺激素和性腺功能的诊断测试。
在特定人群中的使用
怀孕
怀孕类别X – [参见禁忌症(4) ]
致畸作用
Lupaneta Pack禁忌在接受药物治疗的孕妇中或可能怀孕[请参见禁忌症(4) ] 。在开始使用醋酸亮丙瑞林进行储库悬架治疗之前和治疗期间,请确定患者是否怀孕。用于储存库悬浮液的乙酸亮丙瑞林不是避孕药。对于具有生殖能力的妇女,应使用非激素避孕方法[见警告和注意事项(5.4) ] 。
给孕妇服用时,醋酸亮丙瑞林用于仓库的悬浮液可能会对胎儿造成伤害。
当在妊娠第6天以0.00024、0.0024和0.024 mg / kg(人类剂量的1/300至1/3)的测试剂量向兔子给药时,用于储存悬浮液的醋酸亮丙瑞林导致主要胎儿的剂量相关增加异常。在大鼠中进行的类似研究未能证明胎儿畸形的增加。在兔子中使用两种较高剂量的醋酸亮丙瑞林用于仓库悬浮,在大鼠中使用最高剂量(0.024 mg / kg),可以增加胎儿死亡率,减少胎儿体重。
护理母亲
请勿在哺乳期母亲中使用Lupaneta Pack,因为尚未确定醋酸亮丙瑞林用于停药对哺乳期和/或母乳喂养孩子的影响。
尚不知道用于乳状液悬浮液的醋酸亮丙瑞林是否会在人乳中排泄。
已在接受母乳的母亲的牛奶中发现了可检测量的孕激素[见禁忌症(4) ] 。
儿科用
Lupaneta Pack未在初潮前的青少年中使用。尚未在儿科患者中建立Lupaneta Pack的安全性和有效性。 Lupaneta Pack治疗子宫内膜异位症的经验仅限于18岁以上的女性。
老人用
绝经后女性未使用Lupaneta Pack,65岁以上的女性尚未进行过研究。
Lupaneta包装说明
Lupaneta Pack(醋酸亮丙瑞林用于仓库混悬液;醋酸炔诺酮片)3个月装有一个双腔注射器,其中醋酸亮丙瑞林用于仓库混悬液11.25 mg和醋酸炔诺酮片剂USP:5 mg(每瓶90片)。
醋酸亮丙瑞林用于仓库的悬浮
用于仓库悬浮液的乙酸亮丙瑞林是促性腺激素释放激素(GnRH或LH-RH)(一种GnRH激动剂)的合成九肽类似物。化学名称为5-氧代-L-脯氨酰-L-组氨酸-L-色氨酸-L-丝氨酰-L-酪氨酰基-D-亮氨酰-L-亮氨酰-L-精氨酰基-N-乙基-L-脯氨酰胺乙酸盐(盐)具有以下结构式:

用于贮库悬浮液的乙酸亮丙瑞林11.25 mg可在装有无菌冻干微球的预装双腔注射器中获得,该微球与稀释剂混合后成为旨在用作肌肉注射的悬浮液。
用于贮存悬浮液的醋酸亮丙瑞林的前室11.25 mg,用于3个月给药的预填充双腔注射器,包含用于贮存悬浮液的醋酸亮丙瑞林(11.25 mg),聚乳酸(99.3 mg)和D-甘露醇(19.45 mg)。第二腔稀释液包含羧甲基纤维素钠(7.5毫克),D-甘露醇(75毫克),聚山梨酯80(1.5毫克),注射用水USP和冰醋酸USP以控制pH。
在制备用于仓库悬浮液的乙酸亮丙瑞林期间,乙酸损失掉,留下了肽。
醋酸炔诺酮
醋酸炔诺酮片USP-5毫克口服片。
乙酸炔诺酮USP(17-羟基-19-nor-17α-pregn-4-en-20-yn-3-one乙酸酯)是一种合成的口服活性孕激素,是炔诺酮的乙酸酯。它是白色或乳白色结晶粉末。

醋酸炔诺酮片剂USP,5 mg包含以下非活性成分:胶体二氧化硅,乳糖一水合物,硬脂酸镁,微晶纤维素和滑石粉。
Lupaneta Pack-临床药理学
12.1行动机制
醋酸亮丙瑞林用于仓库的悬浮
用于仓库悬浮液的乙酸亮丙瑞林是一种长效的GnRH类似物。一次注射醋酸亮丙瑞林用于贮库混悬液会导致初始升高,然后长时间抑制垂体促性腺激素。每隔季度重复给药会导致性腺类固醇分泌减少;因此,依赖性腺类固醇维持其功能的组织和功能变得静止。停止药物治疗后这种作用是可逆的。
口服醋酸亮丙瑞林无效。
醋酸炔诺酮
乙酸炔诺酮可在雌激素启动的子宫内膜中引起分泌变化。
药效学
在健康女性受试者(N = 20)中进行3个月的醋酸亮丙瑞林11.25 mg的药代动力学/药效学研究时,在给药后第4天至第4周之间观察到了个体受试者雌二醇抑制作用的开始。注射后第三周,雌二醇的平均浓度(8 pg / mL)处于绝经范围。在整个给药期的剩余时间内,平均血清雌二醇水平从绝经到早期卵泡期不等。
在四周内所有受试者的血清雌二醇均被抑制至≤20pg / mL,并在80%的受试者中保持抑制(≤40pg / mL),直到12周用药间隔结束时,此时这些受试者中的两名值在40至50 pg / mL之间。在12周的给药间隔中,另外四名受试者的雌二醇水平至少连续两次升高(范围43-240 pg / mL),但是在此期间没有任何受试者的黄体功能指标。
药代动力学
吸收性
醋酸亮丙瑞林用于仓库的悬浮
单次注射三个月的醋酸亮丙瑞林制剂(11.25 mg)用于女性受试者的储库悬浮液后,在4小时时观察到平均血浆亮丙瑞林浓度为36.3 ng / mL。在给药后第三周稳态水平发作后,亮丙瑞林似乎以恒定的速率释放,然后平均水平在12周后逐渐下降至检测下限附近。 3至12周的平均亮丙瑞林浓度(±标准偏差)为0.23±0.09 ng / mL。但是,完整的亮丙瑞林和无活性的主要代谢产物不能通过研究中的检测方法来区分。最初的爆发,然后迅速下降至稳态水平,类似于月度制剂的释放模式。
醋酸炔诺酮
乙酸炔诺酮口服给药后被脱乙酰基为炔诺酮,乙酸炔诺酮的处置与口服炔诺酮的处置没有区别。乙酸炔诺酮是从乙酸炔诺酮片剂中吸收的,炔诺酮的最大血浆浓度通常发生在给药后约2小时(见图8)。表5总结了在29名健康女性志愿者中,空腹条件下口服5 mg乙酸炔诺酮后,炔诺酮的药代动力学参数。
| AUC =曲线下面积, C max =最大血浆浓度, t max =最大血浆浓度下的时间, t 1/2 =半衰期, SD =标准偏差 | |
| 表5.健康妇女单剂量乙酸炔诺酮后的药代动力学参数 | |
| 醋酸炔诺酮(n = 29) | 算术平均值±SD |
| 炔诺酮 | |
| AUC(0-inf)(ng / ml * h) | 166.90±56.28 |
| 最高C(ng / ml) | 26.19±6.19 |
| 最大t(h) | 1.83±0.58 |
| t 1/2 (小时) | 8.51±2.19 |
图8.空腹条件下,对29名健康女性志愿者单剂5 mg醋酸炔诺酮的平均剂量后,平均炔诺酮血浆浓度曲线

食物的功效:
尚未研究食物施用对乙酸炔诺酮的药代动力学的影响。
分配
醋酸亮丙瑞林用于仓库的悬浮
静脉推注健康男性志愿者后,亮丙瑞林的平均稳态分布体积为27L。与人血浆蛋白的体外结合范围为43%至49%。
醋酸炔诺酮
炔诺酮与性激素结合球蛋白(SHBG)结合的比例为36%,与白蛋白结合的比例为61%。炔诺酮的分配量约为4 L / kg。
代谢
醋酸亮丙瑞林用于仓库的悬浮
在健康的男性志愿者中,静脉内施用1 mg大剂量的亮丙瑞林显示,平均全身清除率为7.6 L / h,基于两室模型,最终消除半衰期约为3小时。
在大鼠和狗中,施用14 C标记的亮丙瑞林显示被代谢为较小的无活性肽,五肽(代谢物I),三肽(代谢物II和III)和二肽(代谢物IV)。这些片段可以进一步分解代谢。
在子宫内膜异位症患者的药代动力学/药效学研究中,每12周肌注一次11.25 mg醋酸亮丙瑞林(n = 19),每4周肌注3.75 mg醋酸亮丙瑞德(n = 15)每24周一次,持续24周。在两个治疗组之间,血清雌二醇浓度相对于基线的变化没有统计学上的显着差异。
在5位前列腺癌患者中测得的MI血浆浓度在给药后2至6小时达到最大浓度,约为母体药物峰值的6%。给药一周后,平均血浆MI浓度约为亮丙瑞林平均浓度的20%。
醋酸炔诺酮
炔诺酮主要通过还原进行广泛的生物转化,然后进行硫酸盐和葡萄糖醛酸苷的缀合。循环中的大部分代谢物是硫酸盐,其中葡萄糖醛酸占大多数尿代谢物。
排泄
醋酸亮丙瑞林用于仓库的悬浮
在对3名患者给药1个月给药后,醋酸亮丙瑞德用于仓库悬浮液3.75 mg给药后,作为母体和MI代谢物在尿液中的回收率不足5%。
醋酸炔诺酮
炔诺酮的血浆清除率值约为0.4 L / hr / kg。炔诺酮通过尿液和粪便排出体外,主要以代谢产物的形式排出。单剂量服用醋酸炔诺酮后,炔诺酮的平均终末消除半衰期约为9小时。
特定人群
肝功能不全
醋酸炔诺酮给药后,肝脏疾病对炔诺酮处置的影响尚未评估。然而,乙酸炔诺酮是禁忌的肝功能或肝病的明显受损[见禁忌症(4) ] 。
尚未确定乙酸亮丙瑞林在肝功能不全患者中用于储库混悬液的药代动力学。
肾功能不全
尚未评估服用乙酸去甲炔诺酮后肾脏疾病对去甲炔诺酮处置的影响。在接受腹膜透析的多次剂量的含有乙炔雌二醇和炔诺酮的口服避孕药的绝经前慢性肾衰竭妇女中,血浆炔诺酮的浓度与具有正常肾功能的绝经前妇女相比没有变化。
尚未确定乙酸亮丙瑞林在肾脏功能不全患者中用于储库混悬液的药代动力学。
种族
醋酸炔诺酮给药后种族对炔诺酮处置的影响尚未评估。
药物相互作用
醋酸亮丙瑞林用于仓库的悬浮
用于储存库悬浮液的醋酸亮丙瑞林是一种主要由肽酶而不是细胞色素P-450酶降解的肽,如特定研究中所述,该药物仅与血浆蛋白结合约46%,预计不会发生药物相互作用。
非临床毒理学
致癌,诱变,生育力受损
醋酸亮丙瑞林用于仓库的悬浮
在大鼠和小鼠中进行了为期两年的致癌性研究。在大鼠中,当以每日高剂量(0.6至4 mg / kg)皮下给药时,在24个月时发现了与垂体良性垂体增生和垂体良性腺瘤有关的剂量相关性增加。女性胰腺胰岛细胞腺瘤和男性睾丸间质细胞腺瘤显着增加,但与剂量无关(低剂量组发病率最高)。在小鼠中,两年内未观察到醋酸亮丙瑞林引起的肿瘤或垂体异常,剂量高达60 mg / kg。患者已接受醋酸亮丙瑞林治疗长达3年,剂量高达10 mg /天,两年治疗,剂量高达20 mg /天,没有明显的垂体异常。
已经使用细菌和哺乳动物系统对乙酸亮丙瑞林进行了致突变性研究。这些研究没有提供诱变潜力的证据。
在成人(> 18岁)中使用醋酸亮丙瑞林和类似类似物进行的临床和药理研究表明,连续给药长达24周后停药,生育抑制的可逆性。尽管尚未在儿童中完成任何临床研究来评估生育抑制的完全可逆性,但醋酸醋酸亮丙瑞林和其他GnRH类似物的动物研究(青春期前和成年大鼠和猴子)已显示出功能恢复。
临床研究
醋酸亮丙瑞林用于仓库的悬浮
醋酸亮丙瑞林用于贮库混悬液的初始子宫内膜异位功效数据基于每月一次给予的3.75 mg剂量。
一项对41位女性的药代动力学/药效学研究包括每月一次3.75 mg剂量和每三个月一次11.25 mg剂量的使用,均未显示出在减少子宫内膜异位症的痛苦症状或减少子宫内膜异位症的程度方面的临床意义上的显着差异。与醋酸亮丙瑞林相关的骨矿物质密度(BMD)。
仓库悬浮液使用醋酸亮丙瑞林和醋酸炔诺酮
进行了两项临床研究,治疗期为12个月,以评估醋酸亮丙瑞林用于储库混悬液和醋酸炔诺酮的共同给药对与醋酸亮丙瑞林用于储库悬液相关的骨矿物质密度(BMD)损失以及醋酸亮丙立普通的疗效的影响用于减轻子宫内膜异位症的症状。 (这些研究中的所有患者均接受了1000 mg元素钙的钙补充)。总共242名妇女每月接受3.75 mg醋酸亮丙瑞林(13次注射)和5 mg醋酸炔诺酮的治疗。人口年龄范围为17-43岁。大多数患者是白种人(87%)。
一项共同管理的研究是一项对照,随机,双盲研究,其中包括51名每月单独接受醋酸亮丙瑞林治疗的妇女(分别用于长效药房混悬液治疗)和55名每月单独服用醋酸亮丙瑞林治疗的妇女,大剂量混悬液治疗。在完成了一年的治疗后,该试验中的妇女接受了长达24个月的随访。另一项研究是一项开放标签的单臂临床研究,该研究针对136名用醋酸亮丙瑞林用于贮库混悬液和醋酸炔诺酮的妇女治疗一年,完成治疗后长达12个月的随访。
第二项研究是一项开放标签,单臂研究,其中每月用醋酸亮丙瑞林进行口服混悬液加醋酸去氧炔诺酮治疗136名妇女,并在完成治疗后长达12个月进行随访。
疗效评估基于研究者或患者每月对子宫内膜异位症的五种体征或症状(痛经,骨盆痛,深度性交往困难,骨盆压痛和骨盆硬结)的评估。
下表6提供了根据醋酸亮丙瑞林和醋酸炔诺酮共同给药的两项研究,有关缓解子宫内膜异位症症状的详细疗效数据。
| * LA =醋酸亮丙瑞林3.75 mg评估 † LA/N = leuprolide acetate 3.75 mg plus norethindrone acetate 5 mg 1 Number of patients that were included in the assessment 2 Percentage of patients with the symptom/sign 3 Value description: 1=none; 2= mild; 3= moderate; 4= severe | ||||||||||||
| Table 6. Percentages of Patients with Symptoms of Endometriosis and Mean Clinical Severity Scores | ||||||||||||
| Percent of Patients with Symptom | Clinical Pain Severity Score | |||||||||||
| Baseline | Final | Baseline | Final | |||||||||
| 变量 | Study | 组 | N 1 | (%) 2 已知共有401种药物与Lupaneta Pack(亮丙瑞林/炔诺酮)相互作用。
检查互动最常检查的互动查看Lupaneta Pack(亮丙瑞林/炔诺酮)与下列药物的相互作用报告。
Lupaneta Pack(亮丙瑞林/炔诺酮)酒精/食物相互作用与Lupaneta Pack(白兰地内酯/炔诺酮)有5种酒精/食物相互作用 卢帕内塔Pack(亮丙瑞林/炔诺酮)疾病相互作用与Lupaneta Pack(亮丙瑞林/炔诺酮)有17种疾病相互作用,包括:
药物相互作用分类
药物状态
美国日本医生 Heather Benjamin MD经验:11-20年  Heather Miske DO经验:11-20年  Bert Hepner DO经验:11-20年  Steven Paterno MD经验:11-20年  Gregory Aaen MD经验:11-20年  渡邊剛经验:21年以上  宮崎総一郎 中部大学特聘教授经验:21年以上  百村伸一 教授经验:21年以上  村上和成 教授经验:21年以上  中山秀章 教授经验:21年以上 临床试验
| ||||||||













