获取国外Caverject药品价格,使用等信息,最快 24 小时回馈
Caverject
Caverject
Caverject的用途:
- 它用于治疗勃起功能障碍(ED)。
- 它可能由于其他原因而提供给您。与医生交谈。
服用Caverject之前我需要告诉我的医生什么?
- 如果您对前列地尔或Caverject的任何其他部位过敏(前列地尔注射液)。
- 如果您对Caverject过敏(前列地尔注射液); Caverject的任何部位(前列地尔注射液);或任何其他药物,食物或物质。告诉您的医生有关过敏以及您有什么症状。
- 如果被告知您不健康,无法做爱。
- 如果您的阴茎变形,阴茎植入物或其他阴茎问题。
- 如果您有以下任何健康问题:红细胞增多症或血小板增多症。
- 如果您有以下任何健康问题:白血病,多发性骨髓瘤,镰状细胞性贫血或其他可能引起勃起疼痛(硬阴茎)或勃起持续超过4小时的健康问题。询问您的医生是否不确定。
- 如果你是女人。该药未获准用于女性。
这不是与Caverject(前列地尔注射液)相互作用的所有药物或健康问题的列表。
告诉您的医生和药剂师您所有的药物(处方药或非处方药,天然产品,维生素)和健康问题。您必须检查以确保服用Caverject(前列地尔注射液)对您所有的药物和健康问题都是安全的。未经医生许可,请勿开始,停止或更改任何药物的剂量。
服用Caverject时我需要了解或做什么?
- 告诉您所有的医疗保健提供者您都服用了Caverject(前列地尔注射液)。这包括您的医生,护士,药剂师和牙医。
- 在看到Caverject(前列地尔注射液)对您的影响之前,请避免驾驶和执行其他需要提醒您注意的任务或动作。
- 为了减少头晕或晕眩的机会,如果您一直坐着或躺着,请慢慢抬起。小心上下楼梯。
- 喝酒之前,先与您的医生交谈。
- 这种药物不能阻止通过血液或性行为传播的艾滋病毒或肝炎等疾病。不使用乳胶或聚氨酯安全套就不要做任何事情。不要共用针头或其他东西,例如牙刷或剃刀。
- 使用注射剂时可能会断针。针已经断裂,部分针仍在阴茎中。如果针头断裂,您可以抓住断裂的一端,将其取出并打电话给医生。如果您无法抓住折断的一端,请立即致电您的医生。
- 这种药物中含有苯甲醇。苄醇可能对新生儿或婴儿造成非常严重的副作用,有时甚至是致命的副作用。该药物未获批准用于儿童。与医生交谈。
如何最好地服用这种药物(Caverject)?
按照医生的指示使用Caverject(前列地尔注射液)。阅读提供给您的所有信息。请严格按照所有说明进行操作。
- 您的医生将教您如何服用Caverject(前列地尔注射液)。
- 使用前后请洗手。
- 不要摇晃。
- 每次服药前都要装新针。
- 请勿使用弯针。不要试图拉直弯曲的针头。它可能更容易破裂。
- 给药后,在注射部位轻压,以防止瘀伤。这样做5分钟,直到出血停止。
- 将针头丢入针头/锋利的处理盒中。请勿重复使用针头或其他物品。盒子装满后,请遵守所有当地规定以摆脱它。如有任何疑问,请与医生或药剂师联系。
- 如果溶液混浊,泄漏或有颗粒,请勿使用。
- 如果溶液变色,请勿使用。
- 切换阴茎的侧面,并在每次使用Caverject(阿前列地尔注射液)的情况下给予Caverject(阿前列地尔注射液)。
如果我错过了剂量怎么办?
- 该药物根据需要使用。不要使用超出医生指示的频率。
我需要马上打电话给我的医生什么副作用?
警告/警告:尽管这种情况很少见,但有些人在服药时可能会有非常严重的副作用,有时甚至是致命的副作用。如果您有以下任何与严重不良副作用相关的症状或体征,请立即告诉医生或寻求医疗帮助:
- 过敏反应的迹象,如皮疹;麻疹;瘙痒;发红或发烧的皮肤发红,肿胀,起泡或脱皮;喘息胸部或喉咙发紧;呼吸,吞咽或说话困难;异常嘶哑或嘴,脸,嘴唇,舌头或喉咙肿胀。
- 勃起(阴茎硬)发红,肿块,肿胀,压痛或弯曲。
- 给予Caverject(前列地尔注射液)的刺激。
- 胸痛或压力或心跳加快。
- 头晕或昏倒。
- 头疼得厉害。
- 气促。
- 任何无法解释的瘀伤或出血。
- 腿静脉肿胀。
- 如果勃起疼痛(阴茎硬)或勃起持续时间超过4小时,请立即致电医生。即使没有性行为,也可能发生这种情况。如果不立即治疗,可能会导致持久的性问题,并且您可能无法做爱。
Caverject还有哪些其他副作用?
所有药物都可能引起副作用。但是,许多人没有副作用,或者只有很小的副作用。如果这些副作用或任何其他副作用困扰您或不消失,请致电您的医生或获得医疗帮助:
- 阴茎疼痛。
这些并非所有可能发生的副作用。如果您对副作用有疑问,请致电您的医生。打电话给您的医生,征求有关副作用的医疗建议。
您可以致电1-800-332-1088向FDA报告副作用。您也可以在https://www.fda.gov/medwatch报告副作用。
如果怀疑OVERDOSE:
如果您认为服药过量,请致电毒物控制中心或立即就医。准备好告诉或显示采取了什么,采取了多少,何时发生。
如何存储和/或丢弃Caverject?
- 按照医生的指示存放。
- 将所有药物放在安全的地方。将所有毒品放在儿童和宠物够不到的地方。
- 扔掉未使用或过期的药物。除非被告知,否则不要冲厕所或倒水。如果您对扔出药物的最佳方法有疑问,请咨询您的药剂师。您所在地区可能有毒品回收计划。
消费者信息使用
- 如果症状或健康问题没有好转或恶化,请致电医生。
- 不要与他人共享您的药物,也不要服用他人的药物。
- 有些药物可能还有另一份患者信息单张。请咨询您的药剂师。如果您对Caverject(前列地尔注射液)有任何疑问,请与您的医生,护士,药剂师或其他医疗保健提供者联系。
- 如果您认为服药过量,请致电毒物控制中心或立即就医。准备好告诉或显示采取了什么,采取了多少,何时发生。
注意:本文档包含有关前列地尔的副作用信息。此页面上列出的某些剂型可能不适用于品牌名称Caverject。
对于消费者
适用于前列地尔:海绵体腔内溶液,海绵体内溶液
其他剂型:
- 静脉内溶液
- 尿道栓
需要立即就医的副作用
除前者所需要的作用外,前列地尔(Caverject中所含的活性成分)可能会引起一些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
服用前列地尔时,如果有下列任何副作用,请立即咨询医生:
罕见
- 勃起过程中阴茎弯曲并伴有疼痛
- 勃起持续4至6小时
- 勃起持续超过6小时,伴有严重且持续的阴茎疼痛
- 睾丸肿胀或疼痛
不需要立即就医的副作用
前列地尔可能会发生一些副作用,通常不需要医疗。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。
请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
比较普遍;普遍上
- 注射部位的出血和疼痛(短期)
- 痛苦的勃起
罕见
- 注射部位阴茎上瘀伤或凝结的血液,通常是由于注射不正确造成的
对于医疗保健专业人员
适用于前列地尔:复方散剂,注射剂,注射剂,注射液,经尿栓
一般
最常见的副作用是阴茎痛,局部出血,发烧,尿道痛,尿道灼热,呼吸暂停和潮红。 [参考]
泌尿生殖
非常常见(10%或更多):阴茎痛(高达36%),尿道痛(13%),尿道灼热(12%)
常见(1%至10%):勃起时间超过4小时,阴茎成角,阴茎纤维化,海绵体纤维化,佩罗尼氏病,阴茎疾病,前列腺疾病,睾丸疼痛,尿道出血/斑点和其他轻微尿道擦伤,阴道灼热/瘙痒
罕见(0.1%至1%):精神异常,阴囊红斑,排尿困难,血尿,尿频,排尿急症,尿道出血,龟头炎,包茎,射精障碍,阴囊紊乱,阴囊痛,睾丸肿胀,睾丸浮肿,阴囊浮肿,阴囊水肿睾丸疾病,睾丸肿块,阴茎含铁血黄素沉淀,上皮或龟头肿胀,会阴部疼痛,勃起疼痛
罕见(少于0.1%):尿路感染
未报告频率:无尿,射精异常,阴茎偏离,阴茎温暖,尿频/尿急/排尿障碍[参考]
心血管的
很常见(10%或更多):冲洗(10.1%)
常见(1%至10%):心动过缓,低血压,心动过速,心脏骤停,水肿,血肿,高血压,心肌梗塞,心电图异常
罕见(0.1%至1%):血管脆性,室上收缩前期,静脉疾病,血管舒张,外周血管疾病,外周水肿,腿静脉肿胀
未报告频率:充血性心力衰竭,充血,二级心脏传导阻滞,休克,右心室漏斗痉挛,室上性心动过速,心室纤维性颤动,快速脉搏,气腹,心室肥厚,心动过速,速动性,动脉导管未闭,组织改变,静脉渗漏,心律失常,姿势性低血压,血压变化,迷走神经休克,血管迷走神经反应,心肌缺血[参考]
本地
很常见(10%或更多):局部出血(15%)
常见(1%至10%):注射部位血肿,注射部位灼痛,阴茎紧张感,注射部位疼痛
罕见(0.1%至1%):注射部位出血,注射部位浮肿,注射部位发炎,注射部位肿块,注射部位瘙痒,注射部位肿胀和发红,注射部位刺激,注射部位麻醉,注射部位发热
未报告频率:局部疼痛[参考]
呼吸道
非常常见(10%或更多):呼吸暂停(12%)
常见(1%至10%):上呼吸道感染,鼻窦炎,鼻炎
未报告频率:呼吸短促,支气管哮喘,高碳酸血症,呼吸抑制,呼吸窘迫,呼吸急促,肺发育不良,气胸[参考]
其他
很常见(10%或更多):发烧(14%)
常见(1%至10%):败血症,流感样症状,疼痛,意外伤害
罕见(0.1%至1%):乏力
稀有(少于0.1%):眩晕
未报告的频率:体温过低,紧张不安,全身无力[参考]
肌肉骨骼
常见(1%至10%):背痛,腿痛,骨盆痛,肌肉痉挛
罕见(0.1%至1%):骨外生
未报告频率:颈部过度伸展,僵硬,长骨皮质增生,小头畸形,腿抽筋[参考]
新陈代谢
常见(1%至10%):低钾血症,高甘油三酯血症,高胆固醇血症,高血糖
未报告频率:低血糖,高钾血症[参考]
神经系统
常见(1%至10%):癫痫发作,头痛,头晕
罕见(0.1%至1%):晕厥,感觉不足,感觉异常,晕厥前
未报告频率:脑出血,嗜睡,麻木,虚脱,健忘症,脑血管意外[参考]
皮肤科的
常见(1%至10%):瘀斑,红斑,皮肤病
罕见(0.1%至1%):皮疹,瘙痒,多汗症
稀有(少于0.1%):荨麻疹
未报告频率:汗液,敏感性,刺激性,非应用部位瘙痒[参考]
胃肠道
常见(1%至10%):腹泻,腹股沟疝
罕见(0.1%至1%):胃梗阻,胃粘膜肥大,恶心,口干
未报告频率:胃返流,腹膜炎[参考]
免疫学的
常见(1%至10%):感染
罕见(0.1%至1%):真菌感染,普通感冒
罕见(小于0.1%):过敏/类过敏反应[参考]
血液学
常见(1%至10%):弥散性血管内凝血
罕见(0.1%至1%):血肌酐升高
非常罕见(少于0.01%):血小板减少
未报告频率:贫血,出血,低铬性贫血[参考]
眼科
常见(1%至10%):视力异常
罕见(0.1%至1%):瞳孔散大[Ref]
肝的
未报告频率:高胆红素血症,胆道闭锁[参考]
肾的
未报告频率:多囊肾,肾衰竭[参考]
精神科
未报告频率:过敏性[参考]
参考文献
1.“产品信息。Caverjet无菌粉末(alprostadil)” Pharmacia和Upjohn,密西根州卡拉马祖。
2.“产品信息。Edex(alprostadil)。”威斯康星州马奎恩市的Schwarz Pharma。
3.“产品信息。缪斯(alprostadil)”,加利福尼亚州Menlo Park的VivusInc。
4. Cerner Multum,Inc.“澳大利亚产品信息”。 00
5. Cerner Multum,Inc.“英国产品特性摘要”。 00
6.“产品信息。ProstinVR儿科无菌溶液(alprostadil)” Pharmacia和Upjohn,密西根州卡拉马祖。
某些副作用可能没有报道。您可以将其报告给FDA。
单纯神经源性病因的勃起功能障碍(例如脊髓损伤)。
- 用1.25 mcg前列地尔开始给药。
- 如果有部分反应,剂量可在1小时内增加到2.5 mcg。每剂量的CAVERJECT使用一个新的小瓶。
- 在滴定过程中,在24小时内不应超过2剂。
- 最佳剂量应产生适合性交的勃起,持续时间不超过1小时。
- 患者必须留在医师办公室,直到完全消肿。
如果需要额外的滴定,则在接下来的24小时内可给予5 mcg的剂量。此后,可以间隔至少24小时给予5 mcg的增量剂量,直到达到最佳剂量为止。不建议剂量大于60 mcg。
患者家庭使用的维护剂量
- 一旦在医生办公室确定了CAVERJECT的剂量,在咨询医生后可能需要进行其他剂量调整。根据上述滴定准则调整剂量。
- 推荐的注射频率每周不超过3次,每次给药之间至少间隔24小时。
- 定期(每3个月或在临床上适当)重新评估患者,并确定是否需要调整剂量。
准备说明
CAVERJECT所需且未提供的耗材
- 1 mL稀释剂(注射用抑菌水,用0.945%w / v的苄醇保存)
- 1 mL至3 mL注射器,取决于滴定剂量
- 21至27号针头用于复原
- 29或30号半英寸注射针
- 酒精棉签
重组说明
- CAVERJECT小瓶:使用包含20 mcg或40 mcg CAVERJECT的正确强度的小瓶,使用1 mL至3 mL注射器,21至27号针头和1 mL稀释剂(注射用抑菌水,用苄醇保存0.945%w / v)进行复原。重构导致CAVERJECT为20 mcg / mL或40 mcg / mL。
- 目视检查小瓶中的溶液是否有颗粒物和变色。如果溶液浑浊,有色或有颗粒,请勿使用。
| 20 mcg小瓶 | 40 mcg小瓶 | ||
|---|---|---|---|
| 剂量 | 注射量 | 剂量 | 注射量 |
| 1.25微克 | 0.06毫升 | 1.25微克 | --- |
| 2.5微克 | 0.125毫升 | 2.5微克 | --- |
| 5微克 | 0.25毫升 | 5微克 | 0.125毫升 |
| 10微克 | 0.5毫升 | 10微克 | 0.25毫升 |
| 15微克 | 0.75毫升 | 15微克 | 0.375毫升 |
| 20微克 | 1毫升 | 20微克 | 0.5毫升 |
| 25微克 | --- | 25微克 | 0.625毫升 |
| 30微克 | --- | 30微克 | 0.75毫升 |
| 40微克 | --- | 40微克 | 1毫升 |
- 将CAVERJECT的剂量吸入注射器。
- 注射前,用29或30号规格的半英寸针头替换用于重建的针头。
- 当储存在25°C(77°F)或更低的温度下时,应在24小时内使用重新配制的溶液。
有关重构和针头准备步骤的完整详细说明,请参阅FDA批准的患者标签中的患者信息和使用说明。
管理说明
- 使用29号或30号规格的半英寸针头注射每剂。
- 注射剂量时,患者应处于坐姿或稍微斜躺的姿势。
- 收回未割包皮患者的包皮。
- 用拇指和食指抓住阴茎的头部,沿着大腿纵向拉伸。
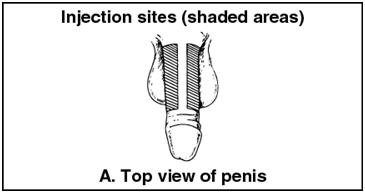
- 注射部位是右或左外侧阴茎。参见下面的图A和B。
|
|
| 图A | 图B |
- 注射前用酒精棉签擦拭预定的注射部位。
- 垂直于阴茎近端的长阴茎外侧轴插入针。避免注射器成角度,并且不要弯曲针头。
- 注射时避免可见的静脉。
- 每次使用CAVERJECT时,交替注射阴茎的一侧。
- 用酒精棉签或无菌纱布压缩注射部位5分钟。
- CAVERJECT仅适合单人使用,使用后应丢弃。
辅助勃起功能障碍的诊断
作为勃起功能障碍的辅助诊断,腔内注射CAVERJECT并监测患者勃起的发生。该测试的扩展是将CAVERJECT用作实验室研究的辅助手段,例如双工或多普勒超声成像。对于这些测试中的任何一项,请使用单剂量的CAVERJECT来诱发刚性勃起。
CaverJect的适应症和用法
勃起功能障碍
CaverJect适用于勃起功能障碍的治疗。
勃起功能障碍的诊断测试
CaverJect在勃起功能障碍的诊断中可作为其他诊断测试的辅助手段。
CaverJect剂量和管理
重要剂量和管理说明
- CaverJect可在含有20 mcg或40 mcg前列地尔的单剂量小瓶中使用。确保为每个患者剂量制剂使用新的正确强度的CaverJect小瓶。
- CaverJect的首次注射应由经过医学培训的人员在医师办公室内进行。
- 小心地将每位患者的CaverJect剂量滴定至最低有效剂量。
- 在开始家庭使用之前,指导患者正确使用并评估他们是否接受过自我注射技术方面的培训。建议患者阅读并认真遵守患者信息和使用说明。
勃起功能障碍的推荐剂量
血管性,精神性或混合病因的勃起功能障碍
- 用2.5 mcg前列地尔开始给药。
- 如果在2.5 mcg时有部分反应,则剂量可在1小时内增加到5 mcg。每个剂量的CaverJect使用新的小瓶。
- 在滴定过程中,在24小时内不应超过2剂。
- 最佳剂量应产生适合性交的勃起,持续时间不超过1小时。
- 患者必须留在医师办公室,直到完全消肿。
如果需要额外的滴定,可以至少间隔24小时以5到10 mcg的增量递增剂量。根据需要重复滴定,直到达到最佳剂量。不建议剂量大于60 mcg。
单纯神经源性病因的勃起功能障碍(例如脊髓损伤)。
- 用1.25 mcg前列地尔开始给药。
- 如果有部分反应,剂量可在1小时内增加到2.5 mcg。每个剂量的CaverJect使用新的小瓶。
- 在滴定过程中,在24小时内不应超过2剂。
- 最佳剂量应产生适合性交的勃起,持续时间不超过1小时。
- 患者必须留在医师办公室,直到完全消肿。
如果需要额外的滴定,则在接下来的24小时内可给予5 mcg的剂量。此后,可以间隔至少24小时给予5 mcg的增量剂量,直到达到最佳剂量为止。不建议剂量大于60 mcg。
患者家庭使用的维护剂量
- 一旦在医生办公室确定了CaverJect的剂量,在咨询医生后可能需要进行其他剂量调整。根据上述滴定准则调整剂量。
- 推荐的注射频率每周不超过3次,每次给药之间至少间隔24小时。
- 定期(每3个月或在临床上适当)重新评估患者,并确定是否需要调整剂量。
准备说明
CaverJect需要和不提供的耗材
- 1 mL稀释剂(注射用抑菌水,用0.945%w / v的苄醇保存)
- 1 mL至3 mL注射器,取决于滴定剂量
- 21至27号针头用于复原
- 29或30号半英寸注射针
- 酒精棉签
重组说明
- CaverJect小瓶:使用包含20 mcg或40 mcg CaverJect的正确强度的小瓶,使用1 mL至3 mL注射器,21至27号针头和1 mL稀释剂(注射用抑菌水,用苄醇保存0.945%w / v)进行复原。重建结果为CaverJect 20 mcg / mL或40 mcg / mL。
- 目视检查小瓶中的溶液是否有颗粒物和变色。如果溶液浑浊,有色或有颗粒,请勿使用。
| 20 mcg小瓶 | 40 mcg小瓶 | ||
|---|---|---|---|
| 剂量 | 注射量 | 剂量 | 注射量 |
| 1.25微克 | 0.06毫升 | 1.25微克 | --- |
| 2.5微克 | 0.125毫升 | 2.5微克 | --- |
| 5微克 | 0.25毫升 | 5微克 | 0.125毫升 |
| 10微克 | 0.5毫升 | 10微克 | 0.25毫升 |
| 15微克 | 0.75毫升 | 15微克 | 0.375毫升 |
| 20微克 | 1毫升 | 20微克 | 0.5毫升 |
| 25微克 | --- | 25微克 | 0.625毫升 |
| 30微克 | --- | 30微克 | 0.75毫升 |
| 40微克 | --- | 40微克 | 1毫升 |
- 将CaverJect的剂量吸入注射器。
- 注射前,用29或30号规格的半英寸针头替换用于重建的针头。
- 当储存在25°C(77°F)或更低的温度下时,应在24小时内使用重新配制的溶液。
有关重构和针头准备步骤的完整详细说明,请参阅FDA批准的患者标签中的患者信息和使用说明。
管理说明
- 使用29号或30号规格的半英寸针头注射每剂。
- 注射剂量时,患者应处于坐姿或稍微斜躺的姿势。
- 收回未割包皮患者的包皮。
- 用拇指和食指抓住阴茎的头部,沿着大腿纵向拉伸。
- 注射部位是右或左外侧阴茎。参见下面的图A和B。
|
|
| 图A | 图B |
- 注射前用酒精棉签擦拭预定的注射部位。
- 垂直于阴茎近端的长阴茎外侧轴插入针。避免注射器成角度,并且不要弯曲针头。
- 注射时避免可见的静脉。
- 每次使用CaverJect时,交替注射阴茎的一侧。
- 用酒精棉签或无菌纱布压缩注射部位5分钟。
- CaverJect仅供单个患者使用,使用后应丢弃。
辅助勃起功能障碍的诊断
作为诊断勃起功能障碍的辅助手段,腔内注射CaverJect并监测患者勃起的发生。该测试的扩展是将CaverJect用作实验室研究的辅助手段,例如双工或多普勒超声成像。对于这些测试中的任何一个,请使用单剂量的CaverJect进行刚性勃起。
剂型和优势
注射:在单剂量小瓶中装入20 mcg和40 mcg冻干粉进行复溶。
禁忌症
CaverJect是禁忌的:
- 已知对该药有超敏反应的男性[见不良反应(6.1) ]
- 患有镰刀状细胞性贫血或镰刀状细胞性状,多发性骨髓瘤或白血病等易患易感症的男性[请参阅警告和注意事项(5.1) ]
- 用于治疗阴茎纤维化疾病的男性勃起功能障碍,例如解剖变形,成角度,海绵体纤维化或佩罗尼氏病[请参阅警告和注意事项(5.2) ]
- 阴茎植入的男性。
警告和注意事项
长时间的勃起和狂热
延长勃起定义为持续持续4至6个小时的勃起,持续时间为4到6个小时,在CaverJect研究中,有18%的患者接受治疗的18个月中有4%。阴茎异常勃勃(勃起持续时间超过6小时)的发生率为0.4%。如果勃起持续超过4小时,患者应立即寻求医疗救助。如果不立即治疗阴茎异常勃勃,可能会导致阴茎组织损伤和永久性丧失效能。
为了最大程度地减少长时间勃起或阴茎异常勃起的机会,应将CaverJect缓慢滴定至最低有效剂量[参见剂量和用法(2.1) ]。另外,对于患有镰状细胞性贫血或镰状细胞性状,多发性骨髓瘤或白血病等易患易感症的患者,请勿使用CaverJect [请参阅禁忌症(4) ] 。
阴茎纤维化
在CaverJect的临床研究中,阴茎纤维化的总发生率为3%。在一项使用时间长达18个月的自我注射临床研究中,阴茎纤维化的发生率为7.8%。
阴茎的身体检查应该定期进行,以检测阴茎纤维化的体征。发生阴茎弯角或海绵体纤维化的患者应停止使用CaverJect治疗。
低血压
腔内注射CaverJect会增加前列地尔的外周血水平,这可能导致低血压。避免在已知海绵体静脉渗漏的患者中使用CaverJect。
与抗凝剂一起使用时,注射部位出血
服用华法林或肝素等抗凝剂的患者在腔内注射CaverJect后可能会增加注射部位出血的倾向。用酒精棉签或无菌纱布压缩注射部位5分钟。
与基本医疗状况有关的心血管风险
已有心血管疾病的患者有发生性活动的心脏风险。因此,勃起功能障碍的治疗方法(包括CaverJect)通常不应用于因其潜在的心血管状况而不宜进行性活动的男性。此外,勃起功能障碍的评估应包括确定潜在的潜在原因,并在进行完整的医学评估后确定适当的治疗方法。
与腔内注射其他血管活性药物联合使用的风险
在临床研究中尚未确定CaverJect与其他经腔海绵体内注射的血管活性剂联合使用的安全性和有效性。长时间勃起,阴茎异常勃勃和低血压的风险可能会增加。
断针
应使用单独的针头进行重组和给药。 CaverJect使用超细针头进行给药。与所有超细针头一样,存在断针的可能性。据报道,断针,而一部分针仍留在阴茎中,在某些情况下,需要住院治疗和手术切除。在正确的患者处理和注射技术上进行仔细的指导可能会将针头断裂的可能性降到最低[参见剂量和用法(2.3)和不良反应(6.2) ] 。
苄醇防腐剂可能导致婴儿发生严重不良反应的风险
使用推荐的稀释剂复溶时,溶液中含有苯甲醇。在含CaverJect的输注溶液中,使用苯甲醇保存的制剂治疗的新生儿和低出生体重的婴儿可能发生严重的致命不良反应,包括“喘气综合征”。 “喘气综合征”的特征在于中枢神经系统抑制,代谢性酸中毒和喘气。 CaverJect不适用于新生儿或婴儿。
咨询患者性传播疾病
CaverJect的使用不能防止性传播疾病。建议患者就预防性传播疾病(包括人类免疫缺陷病毒(HIV))所必需的保护措施进行咨询。
不良反应
标签中其他地方描述了以下内容:
- 长时间的勃起和阴茎勃勃[请参阅警告和注意事项(5.1) ]
- 阴茎纤维化[见警告和注意事项(5.2) ]
临床试验经验
由于临床试验是在广泛不同的条件下进行的,因此不能将在一种药物的临床试验中观察到的不良反应率直接与另一种药物在临床试验中观察到的不良反应率进行比较,并且可能无法反映在临床实践中观察到的不良反应率。
局部不良反应:表2显示了CaverJect临床研究中来自1861名患者的局部不良反应,包括一项为期18个月的开放标签研究。
| |
| 阴茎痛 | 37% |
| 长时间勃起 | 4% |
| 阴茎纤维化 | 3% |
| 注射部位血肿 | 3% |
| 阴茎疾病* | 3% |
| 注射部位瘀斑 | 2% |
| 阴茎皮疹 | 1% |
| 阴茎水肿 | 1% |
在<1%的患者中报告了以下局部不良反应:注射部位出血,注射部位发炎,注射部位瘙痒,注射部位肿胀,注射部位浮肿,尿道出血,阴茎温暖,麻木,刺激,敏感性,瘙痒,红斑,痛苦的勃起和射精异常。
在这些研究中,除阴茎痛(2%)外,在294例接受安慰剂的患者中未报告局部不良反应。
阴茎疼痛:在大多数情况下,阴茎疼痛的强度为轻度或中度。 3%的患者因阴茎痛而中止治疗
长期勃起/阴茎勃勃:长时间勃起被定义为持续4到6个小时的勃起;阴茎异常勃起被定义为持续了6个小时或更长时间的勃起。在临床研究中,在腔内给药CaverJect后长时间勃起的频率为4%,而阴茎异常勃勃的频率为0.4% [请参阅警告和注意事项(5.1) ] 。
阴茎血肿/瘀斑:在临床研究中,阴茎血肿和瘀斑的发生率分别为3%和2%。
全身不良反应: CaverJect临床研究中≥1%的受试者报告的全身不良反应包括:头晕(1%)。
在<1%的患者中报告了以下全身不良反应:睾丸痛,阴囊水肿,血尿,盆腔痛,低血压,血管舒张,血管迷走神经反应,发汗,皮疹和非应用性瘙痒。 3例(0.2%)因症状性低血压而停药。
294例接受安慰剂的患者未报告全身不良反应。
除了CaverJect观察到的不良反应外,CaverJect IMPULSE的临床研究还报告了以下不良反应:
在一项为期6周的开放标签交叉研究中,对87位患者的CaverJect IMPULSE进行了评估,该研究比较了CaverJect IMPULSE中包含的注射用前列地尔制剂与CaverJect中包含的制剂。在这项研究中使用的剂量范围从2.5 mcg到20 mcg。据报道,CaverJect IMPULSE制剂的不良反应包括:阴茎疾病(4.6%),勃起时间长(1.1%),注射部位红斑(1.1%),皮疹(1.1%),头晕(1.1%)和血精(1.1%) 。阴茎疾病包括阴茎疼痛,注射后疼痛和勃起疼痛。
在单剂量,双盲,交叉研究中对63位患者进行了CaverJect IMPULSE评估,该研究将CaverJect IMPULSE与CaverJect进行了比较。在这项研究中使用的剂量范围从2.5 mcg到20 mcg。据报道,CaverJect IMPULSE制剂的不良反应包括:阴茎痛(1.6%)和瘙痒症(1.6%)。
上市后经验
在批准使用CaverJect的过程中,已经确认了以下不良反应:
已有报道在使用CaverJect期间出现断针现象。在某些情况下,需要手术摘除针头。
药物相互作用
尚未正式研究前列地尔与口服或海绵体内给药的其他药物之间药代动力学药物-药物相互作用的潜力[见警告和注意事项(5.6) ] 。
在特定人群中的使用
怀孕
CaverJect不适用于女性。
哺乳期
CaverJect不适用于女性。
儿科用
尚未在儿科患者中确立安全性和有效性[见警告和注意事项(5.8) ] 。
老人用
临床研究中共有341名受试者,年龄在65岁以上。在这些受试者和较年轻的受试者之间未观察到安全性和有效性的总体差异,其他报告的临床经验也未发现老年和较年轻患者的反应差异。
过量
在CaverJect的临床试验中未观察到过量。如果发生海绵体内过量的CaverJect,则患者应接受医学监督,直到全身作用消失和/或发生阴茎消肿为止。任何全身症状(例如低血压)的治疗都是合适的。
CaverJect说明
CaverJect包含前列地尔的一种前列腺素E 1 (PGE 1 )的合成形式,化学名称为(11α,13E,15S)-11,15-二羟基-9-氧代前列腺素-13-en-1-oic酸。分子量为354.49。
前列地尔为白色至类白色结晶粉末,熔点在115°C至116°C之间。CaverJect可以作为无菌冷冻干燥粉末,用于海绵体内使用,大小:每瓶20 mcg和40 mcg。当用1mL的抑菌水按照指示进行重构时,用0.945%w / v的苯甲醇保存,得到1.13mL的重构溶液。每毫升CaverJect包含20.5 mcg或41.1 mcg前列地尔,具体取决于小瓶强度,172 mg乳糖,47 mcg柠檬酸钠和8.4 mg苄醇。前列地尔的可递送量为每毫升20 mcg或40 mcg,因为20 mcg强度的约0.5 mcg和40 mcg强度的约1.1 mcg由于吸附到小瓶和注射器而损失。在制造过程中,冻干前用盐酸和/或氢氧化钠调节注射用前列地尔的pH。
前列地尔的结构式如下所示:

CaverJect-临床药理学
作用机理
前列地尔(PGE1)是一种前列腺素,具有多种药理作用,包括血管舒张和抑制血小板聚集。前列地尔通过小梁平滑肌的松弛和海绵体动脉的扩张来诱导勃起,该扩张是通过结合至其受体并通过调节腺苷酸环化酶来增加细胞内环状单磷酸腺苷(cAMP)水平。通过挤压小静脉抵靠白膜膜,这会导致腔隙的扩大和血液的滞留,这一过程被称为体静脉阻塞机制。前列地尔还减弱海绵体中突触前去甲肾上腺素的释放。
体外研究表明,前列地尔简化了人海绵体和海绵体的分离制剂,以及去甲肾上腺素或PGF2α收缩的海绵状动脉节段。在猪尾猴( Macaca nemestrina )中,前列地尔在体内以剂量依赖性方式增加海绵状动脉血流量。
药代动力学
吸收:为了治疗勃起功能障碍,前列地尔通过注射入海绵体而给药。前列地尔的绝对生物利用度尚未确定。
分布:在腔内注射20 mcg前列地尔后,注射前30和60分钟时前列地尔的平均外周血药浓度(分别为89皮克/毫升和102皮克/毫升)不明显高于内源性前列地尔的基线水平(96皮克/毫升)。前列地尔的血浆水平采用放射免疫法测定。前列地尔在血浆中主要与白蛋白结合(结合率为81%),在较小程度上与α-球蛋白IV-4结合(结合率为55%)。没有观察到与红细胞或白细胞的显着结合。
代谢:前列地尔被转化为在排泄前会进一步代谢的化合物。静脉内给药后,约80%的循环前列地尔一次通过肺部代谢,主要是通过β-氧化和ω-氧化。在腔内注射20 mcg前列地尔后,主要循环代谢物13、14-dihydro-15-oxo-PGE 1的外周水平在注射后30分钟达到峰值,并在注射后60分钟恢复到给药前水平。 。
排泄:前列地尔的代谢产物主要通过肾脏排泄,在给药后24小时内,几乎90%的静脉注射剂量通过尿液排泄。其余剂量从粪便中排出。没有证据表明静脉注射后前列地尔或其代谢物会保留组织。
特定人群的药代动力学
老年:尚未正式评估年龄对前列地尔药代动力学的潜在影响。
种族:种族对前列地尔的药代动力学的潜在影响尚未得到正式评估。
肾和肝功能不全:尚未对肾上或肝功能不全患者的前列地尔的药代动力学进行正式研究。
非临床毒理学
致癌,诱变,生育力受损
致癌作用
尚未进行长期致癌性研究。
诱变
前列地尔在细菌突变(Ames),碱性洗脱,大鼠微核,姐妹染色单体交换,CHO / HGPRT哺乳动物细胞正向基因突变和计划外DNA合成(UDS)分析中呈阴性。
生育能力受损
大鼠生殖研究表明,前列地尔的最高剂量为0.2 mg / kg /天不会对大鼠的精子发生产生不利影响或产生影响。这些剂量比基于人体表面积的最大建议人类剂量(MRHD)40 µg高约48倍。
临床研究
在两项双盲安慰剂对照研究(研究1和研究2)和一项为期6个月的开放性双盲研究中,研究了CaverJect在因精神病,血管生成,神经病和/或混合病因导致勃起功能障碍的男性中的疗效。标签研究(研究3)。在临床研究(研究1和研究3)中,海绵体腔内注射CaverJect后超过80%的患者经历了足以进行性交的勃起。
研究1:共有153名ED男性患者,平均年龄为53岁(23-69岁)。该研究分为三个阶段:一个为期2.5周,随机,双盲,安慰剂对照的交叉阶段,其中每个人在办公室内注射安慰剂或2.5 mcg,5 mcg,7.5 mcg或10 mcg CaverJect;为期2周的开放标签的办公室剂量滴定阶段,以确定最佳的家用剂量(后一剂量定义为诱导勃起足以进行性交且持续≤60分钟的剂量);以及为期4周的开放标签在家阶段。在双盲安慰剂对照的交叉阶段,通过临床评估(“完全阴茎刚度”)和RigiScan标准(≥70%的坚挺度,至少10分钟),每剂CaverJect均明显优于安慰剂。安慰剂无反应。响应者的百分比随CaverJect剂量的增加而增加。根据临床评估,交叉和剂量滴定阶段的总体缓解率为76%(117/153),按照RigiScan标准为51%(78/152)。在居家阶段使用CaverJect的102名男性中有73%的注射达到了令人满意的性交。在居家阶段使用CaverJect的男性中,有75%仍处于剂量滴定阶段对他们最合适的剂量;分别有17%和8%的男性减少或增加剂量。每次注射的平均勃起时间为70.8分钟。
研究2:共有296名平均年龄为54岁(21-74岁)的ED男性参加了这项双盲,安慰剂对照,平行臂设计研究。这些人被随机分配到五组中的一组,并接受单剂量的安慰剂,2.5 mcg,5 mcg,10 mcg或20 mcg CaverJect。没有患者对安慰剂有反应。 CaverJect和安慰剂各剂量之间的临床反应和RigiScan评估的反应率差异具有统计学意义。随着CaverJect剂量增加(10 mcg剂量除外),临床反应率和RigiScan反应率也具有统计学意义的剂量反应关系。注射后的平均勃起时间为2.5 mcg剂量后的12分钟到20 mcg剂量后的44分钟,其关系是线性的( p = .025,线性回归分析)。
研究3:在一项为期6个月的开放标签在家研究中,对683名平均年龄为58岁(20-79岁)的ED男性进行了进一步的评估,评估了CaverJect的疗效。通过对89%的男性进行滴定确定了CaverJect的最佳剂量(606/683)。共有471/683名男性(占69%)完成了为期6个月的研究。注射的13762次CaverJect注射液中有87%产生了令人满意的性活动。平均勃起时间为67.5分钟。
在一项单盲,交叉研究中,将CaverJect IMPULSE中包含的前列地尔的配方与CaverJect在87例ED男性中进行了比较。研究中患者使用的剂量范围从2.5 mcg到20 mcg,并且两种制剂的剂量均相同。根据国际勃起功能指数(IIEF)的30分勃起功能(EF)域评分和勃起反应的医师评估评分,两种制剂的疗效均具有可比性。 CaverJect和CaverJect中包含的配方的平均EF域得分分别为26.6(SD = 5.3)和27.6(SD = 3.8)。基于从0(无肿块)到3(完全僵硬)的等级,CaverJect和CaverJect IMPULSE中包含的制剂的平均医师评估得分分别为2.6(SD = 0.6)和2.7(SD = 0.5)。
供应/存储和处理方式
CaverJect是冻干粉,装在小瓶中,含有23.2或46.4 mcg前列地尔,用于海绵体内给药。当用1毫升注射用抑菌水(用0.945%w / v的苄醇保存)重新配制时,前列地尔的递送量为20 mcg或40 mcg。
在20°C至25°C(68°F至77°F)之间存储20 mcg小瓶的CaverJect。当在25°C(77°F)或更低的温度下存放且未冷藏或冷冻时,重构后的溶液应在24小时内使用。
将CaverJect 40 mcg小瓶在2°C至8°C(36°至46°F)之间保存,直至分液。分配后,小瓶应在25°C(77°F)或更低的温度下保存3个月或直至失效日期,以先到者为准。当在25°C(77°F)或更低的温度下存放且未冷藏或冷冻时,重构后的溶液应在24小时内使用。
当重组并按指示使用时,前列地尔的可递送量分别为20微克或40微克。重组CaverJect时,仅可使用注射用抑菌水并用0.945%w / v的苄醇保存。
CaverJect在以下软件包中可用:
| 六个20 mcg小瓶的包装 | NDC 0009-3701-05 |
| 六个40 mcg小瓶的包装 | NDC 0009-7686-04 |
注射需要以下耗材,而CaverJect不提供以下耗材:
- 1 mL稀释剂(注射用抑菌水,用0.945%w / v的苄醇保存)
- 1 mL至3 mL注射器,取决于滴定剂量
- 21至27号针头用于复原
- 29或30号半英寸注射针
- 酒精棉签
病人咨询信息
建议患者阅读FDA批准的患者标签(患者信息和使用说明)。
剂量和自我管理
为确保安全有效地使用CaverJect,请在患者开始在家中使用CaverJect进行海绵体腔内治疗之前,对患者进行自我注射技术的指导和培训。告知患者初始剂量给药和剂量滴定将在医师办公室进行[参见剂量和给药方法(2.1) ] 。
一旦确定了CaverJect的家庭剂量,便指示患者在没有咨询医生的情况下不要更改剂量。
患者可能期望勃起发生在5分钟到20分钟之内,并且持续时间不超过1小时。 CaverJect每周应使用不超过3次,每次使用之间至少间隔24小时[请参阅剂量和用法(2.2) ] 。
告知患者他们必须前往医师办公室进行定期检查,以评估使用CaverJect的治疗益处和安全性。
当自我给药时,应指导患者[参见剂量和给药方法( 2.2,2.3) ] :
- 丢弃任何有沉淀或变色的复溶溶液
- 沿着阴茎近端三分之一的背外侧进行注射
- 注射前用酒精棉签擦拭预定的注射部位
- 注射时避免可见的静脉
- 交替注射阴茎的一侧和注射部位
- 用酒精棉签或无菌纱布压缩注射部位5分钟
- 每个CaverJect样品瓶只能使用一次,使用后应丢弃。每个剂量使用一个新的小瓶CaverJect。
- 请勿使用弯曲的针头进行重组或注射。请勿试图拉直弯曲的针头。从注射器上取下针头,将其丢弃,然后将新的未使用的无菌针头连接到注射器上。
- 不要重复使用或共用针头,使用后要正确丢弃
断针
告知患者,CaverJect自我注射过程中发生了断针。建议患者垂直于阴茎的长距离插入针头,以免针头弯曲或折断[见剂量和用法(2.4) ,警告和注意事项(5.7)和不良反应(6.2) ] 。
阴茎痛
告知患者最常见的副作用是注射后的阴茎痛,严重程度通常为轻度至中度[见不良反应(6.1) ] 。
独裁者
CaverJect的腔内治疗可能引起的严重不良反应是阴茎异常勃起。如果勃起持续时间超过4小时,则指示患者立即寻求医疗救助[请参阅警告和注意事项(5.1) ] 。
阴茎纤维化
在CaverJect的临床研究中已经报道了阴茎纤维化。建议患者尽快向医生报告以前没有出现过的阴茎疼痛或强度增加的阴茎疼痛,以及阴茎中结节或硬组织的出现或勃起的阴茎弯曲的情况。 [参见警告和注意事项(5.2) ] 。
注射部位反应
告知患者,注射CaverJect会在注射部位引起少量出血,并且可能发生血肿和瘀斑。劝告患者报告任何持续的发红,压痛或肿胀[见警告和注意事项(5.4) ] 。
性病
海绵体内CaverJect的使用不能防止性传播疾病的传播。向患者提供有关预防性传播疾病(包括人类免疫缺陷病毒(HIV))传播所必需的保护措施的建议[请参阅警告和注意事项(5.9) ] 。

LAB-0764-3.0
患者信息
CaverJect [KAV-er-jeckt] ®
(前列地尔)
用于注射,用于海绵体内
在开始使用CaverJect时以及每次获得笔芯时,请阅读此患者信息。可能有新的信息。此信息不能代替您与医疗保健提供者谈论您的医疗状况或治疗方法。
什么是CaverJect?
CaverJect是一种处方药,用于:
- 治疗勃起功能障碍(ED)。
- 结合其他医学检查诊断ED。
CaverJect不适用于女性或儿童。
如果您执行以下操作,请勿使用CaverJect:
- 对前列地尔或CaverJect中的任何成分过敏。有关CaverJect中成分的完整列表,请参见本传单的末尾。
- 患有某些医学问题,可能会导致勃起持续超过4小时,例如镰状细胞性贫血,镰状细胞性状,多发性骨髓瘤,白血病。
- 阴茎变形
- 阴茎植入
使用CaverJect之前,请告知您的医疗保健提供者所有其他医疗状况,尤其是如果您:
- 勃起持续了四个多小时
- 有镰状细胞性状或镰状细胞性贫血
- 患有或曾经患有称为多发性骨髓瘤或白血病的血细胞癌
- 阴茎变形
- 阴茎植入
- 血压低(低血压)
- 有出血问题
- 患有或曾经患有心脏病,例如心脏病发作,心律不齐,心绞痛,胸痛,主动脉瓣狭窄或心力衰竭
告诉您的医护人员您服用的所有药物,包括处方药和非处方药,维生素和草药补品。
CaverJect可能会影响其他药物的工作方式,而其他药物可能会影响CaverJect的工作方式并导致副作用。
尤其要告知您的医疗保健提供者,如果您服用其他任何可治疗ED的药物,其他注射到阴茎(鼻腔)的药物,或某些称为抗凝药物的药物(例如肝素或华法林)。
如果您不确定,请向您的医疗保健提供者或药剂师索要这些药物的清单。
知道你吃的药。保留一份清单,以便在您购买新药时向您的医疗保健提供者和药剂师显示。
我应该如何使用CaverJect?
- 有关如何以正确方式准备和注入CaverJect的信息,请参见CaverJect随附的详细使用说明。
- 您应该在医疗服务提供者的办公室接受第一剂CaverJect。
- 完全按照医疗保健提供者的指示使用CaverJect。
- 您的医疗保健提供者会告诉您要使用多少CaverJect以及何时使用它。
- 您的医疗保健提供者可能会根据需要更改您的剂量。在没有事先与您的医疗服务提供者交谈之前,请勿更改您的CaverJect剂量。
- 您的医疗保健提供者应在首次注射之前向您展示如何正确准备和注射CaverJect。
- CaverJect每周不应使用超过3次。
- 每24小时CaverJect的使用次数不得超过1次。
- 每次使用时,更改注射CaverJect的阴茎的确切位置和侧面。
- CaverJect只能使用1次,每次使用后应正确丢弃。
您应该每3个月向您的医疗保健提供者进行一次检查,以确保CaverJect的工作方式正确,并在需要时更改CaverJect的剂量。
CaverJect可能会有哪些副作用?
CaverJect可能会导致严重的副作用,包括:
- 不会消失的勃起(独身主义)。如果勃起持续超过4小时,请立即寻求医疗帮助。如果不立即治疗,这种情况可能会永久损坏您的阴茎。
- 阴茎变形(阴茎纤维化)。您的医疗保健提供者应定期检查您的阴茎是否有阴茎纤维化的迹象。如果发生阴茎纤维化,则不应继续使用CaverJect。
- 血压低(低血压)。
- 注射部位出血。服用某些称为抗凝剂的药物(例如肝素或华法林)的人可能有注射部位出血增加的风险。
- 增加患心脏病的风险。性活动会给您的心脏造成额外的负担,尤其是如果您的心脏因心脏病发作或心脏病而虚弱时。询问您的医疗保健提供者,您的心脏是否足够健康,以应对额外的性生活压力。如果您遇到心脏病的症状,例如胸痛,头晕或恶心,请停止性活动并立即寻求医疗帮助。
- 断针。使用CaverJect可能会断针。为了最大程度地避免折断针头,您应特别注意医疗保健提供者的说明,并尝试正确处理注射器和针头。如果针头在注射过程中断裂,并且您能够看到并抓住断裂的末端,则应将其取下并与您的医疗保健提供者联系。如果看不到或无法抓住折断的一端,则应立即联系您的医疗保健提供者。
- 苯甲醇毒性。苄醇是混合时存在于CaverJect中的防腐剂。 Benzyl alcohol has caused serious side effects, including death, in children, especially premature and low-birth weight infants, who have received the preservative benzyl alcohol. CaverJect is not meant for use in children.
CaverJect does not protect you or your partner from getting sexually transmitted infections , including HIV-the virus that causes AIDS.
The most common side effect of CaverJect is penile pain
These are not all the possible side effects of CaverJect.
打电话给您的医生,征求有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。
General information about the safe and effective use of CaverJect
有时出于患者信息手册中列出的目的以外的目的开出药物。 Do not use CaverJect for a condition for which it was not prescribed. Do not give CaverJect to other people even if they have the same symptoms that you have.可能会伤害他们。
You can ask your pharmacist or healthcare provider for information about CaverJect that is written for health professionals.
What are the Ingredients in CaverJect?
Active ingredient: alprostadil
Inactive ingredients: alpha cyclodextrin, lactose, sodium citrate, benzyl alcohol (contained in the final solution) and hydrochloric acid and/or sodium hydroxide for pH adjustment.

LAB-1045-1.0
Revised: December 2017
使用说明
CaverJect [KAV-er-jeckt]®
(alprostadil)
for injection, for intracavernosal use
Your healthcare provider should show you how to prepare and inject CaverJect the right way before you inject it for the first time. Do not try to inject yourself until you have been shown the right way to give your injections by your healthcare provider.
Information about how to safely inject CaverJect:
- Read and follow these instructions so that you inject CaverJect the right way. Call your healthcare provider if you have any questions about the right way to inject CaverJect.
- Separate needles should be used for reconstitution and administration. Do not use damaged or bent needles to inject CaverJect.
- If you accidentally bend a needle, do not attempt to straighten it.
- Using bent or re-straightened needles may cause part of the needle to break off and remain in the penis. Some people have reported needle breakage in their penis during the injection and, in some cases, had to go to hospital for surgery to remove the needle.
- If you accidentally bend the needle while preparing your CaverJect injection, remove it from the syringe, throw it away, and attach a new, needle to the syringe as described under "Prepare the Dose" below. ( See "Dispose of your used CaverJect syringe and needle" at the end of these Instructions).
- Do not share your needles or syringes with other people, even if the needle has been changed. You may give other people a serious infection, or get a serious infection from them.
- Use the needles, syringe, alcohol swabs, and vials only 1 time then safely throw away the supplies and any unused solution in a puncture resistant container (See "Dispose of your used CaverJect syringe and needle" at the end of these instructions). Ask your healthcare provider or pharmacist where you can get a puncture resistant or sharps container.
Supplies you will need to give your CaverJect injection (Figure A)
| Figure A: Supplies you will need for your Injection.  |
| Follow the instructions below to prepare and give your injection. Figure B explains the parts of the needle and syringe that are referred to in the instructions. | Figure B: Parts of the needle and syringe  |
CaverJect comes in 20 mcg or 40 mcg strengths. Make sure you have the right strength vial of CaverJect that your healthcare provider prescribed for you.
Prepare the Syringe
| Step 1 . | |||||||||
| Wash your hands thoroughly, and dry them with a clean towel. | |||||||||
| Step 2 . | |||||||||
Assemble the needle and syringe as follows:
| Figure C: Remove the syringe
| ||||||||
| Figure D: Open the needle wrapper
| ||||||||
| Step 3 . | |||||||||
| Keeping hold of the needle assembly, remove the plastic syringe cap from the syringe tip (Figure E). Do not touch the syringe tip. | Figure E: Remove the syringe cap
| ||||||||
| Step 4 . | |||||||||
Hold the needle assembly (still in the paper wrapper). Firmly attach the needle to the syringe tip. Turn it clockwise, like tightening a screw to lock it in place (Figure F).
| Figure F: Attach the needle to the syringe
| ||||||||
| Mixing the powder and liquid to prepare the dose | |||||||||
| Step 5 . | |||||||||
| Remove the plastic cap from the vial of CaverJect and remove any cover from the diluent (Figure G). | Figure G: Remove the vial cap  | ||||||||
| Step 6 . | |||||||||
| Wipe the rubber stoppers on the vials of CaverJect and diluent with 1 alcohol swab. Throw away the alcohol swab. | |||||||||
| Step 7 . | |||||||||
Carefully hold the syringe by the barrel and remove the needle cover (Figure H).
| Figure H: Remove the needle cover
| ||||||||
| Step 8 . | |||||||||
| Hold the syringe with the needle attached and push the needle through the center of the diluent vial's rubber stopper (Figure I). Be careful not to bend the needle. | Figure I: Push the needle into the diluent vial
| ||||||||
| Figure J: Remove the liquid from the vial
| ||||||||
| Step 9 . | |||||||||
| Push the syringe plunger to the 1mL mark on the syringe. This will remove air and extra liquid back into vial. Grasp the side of the syringe barrel (not the plunger) and pull the needle from the diluent vial in a straight line to avoid bending the needle (Figure K). | Figure K: Adjust the amount of liquid in the syringe
| ||||||||
| Step 10 . | |||||||||
Holding the syringe with the needle attached in a straight line with the vial of CaverJect, push the needle through the center of the rubber stopper of the vial of CaverJect. Be careful not to bend the needle .
| Figure L: Push the needle into the CaverJect vial
| ||||||||
| Step 11 . | |||||||||
| Without removing the needle or touching the needle or stopper, gently swirl (do not shake) the vial until all the powder is dissolved in the liquid. Then turn the vial and needle/syringe upside down and gently swirl the vial to dissolve any powder in the neck of the vial. Do not use the solution if it is cloudy, colored, or contains particles. | |||||||||
| Step 12 . | |||||||||
Keeping the needle in the vial, firmly hold the vial and syringe upside down in one hand.
| Figure M: Remove the liquid from the vial
| ||||||||
| Step 13 . | |||||||||
If there are air bubbles, gently tap the syringe barrel until the bubbles float to the top of the liquid (see Figure N ).
| Figure N: Tap the syringe barrel to remove air bubbles
| ||||||||
| Step 14 . | |||||||||
| Carefully replace the needle used to mix th 已知共有28种药物与Caverject(alprostadil)相互作用。
检查互动最常检查的互动查看Caverject(前列地尔)与下列药物的相互作用报告。
卡维妥(前列地尔)疾病相互作用与Caverject(alprostadil)有3种疾病相互作用,包括:
药物相互作用分类
药物状态
美国日本医生 Gregory Aaen MD经验:11-20年  Brian Aalbers DO经验:11-20年  Glen Scott DO经验:21年以上  Cecile Becker MD经验:11-20年  Shruti Badhwar DO经验:11-20年  渡邊剛经验:21年以上  村上和成 教授经验:21年以上  中山秀章 教授经验:21年以上  村田朗经验:21年以上  溝上裕士 医院教授经验:21年以上 临床试验
| |||||||||