获取国外Zyprexa Relprevv(注射)药品价格,使用等信息,最快 24 小时回馈
Zyprexa Relprevv(注射)
什么是Zyprexa Relprevv?
Zyprexa Relprevv是含有奥氮平的长效注射剂,奥氮平是一种抗精神病药物,会影响大脑中的化学物质。
Zyprexa Relprevv用于治疗由于精神分裂症或双相情感障碍(躁狂抑郁症)而处于躁动状态的成年人。这种注射剂并非每天用于治疗任何精神病。
Zyprexa Relprevv仅在特殊程序下可用。您必须先注册该程序,并了解服用该药物的风险和益处。
重要信息
Zyprexa Relprevv可能会导致ir妄症状(突然的严重混乱,迷失方向,躁动,言语或行走问题)或嗜睡,足以使您陷入昏迷状态。注射后至少三个小时将密切注视您,并且您在一天的剩余时间内都不应开车。
收到Zyprexa Relprevv之前,请告诉医生您是否患有心脏病,充血性心力衰竭,心律失常,心脏病发作或中风的病史,或者是否还使用了安定性药物(例如Valium)。
在紧急情况下,可能无法在接受治疗之前告知您的监护人您的健康状况或您是否怀孕或母乳喂养。确保以后有任何照顾您的医生知道您已收到该药。
奥氮平可能会损害您的思维或反应。如果您开车或做任何需要提醒您注意的事情,请当心。
Zyprexa Relprevv未被批准用于患有痴呆症相关精神病的老年人。
在服药之前
如果您对奥氮平过敏,则不应接受Zyprexa。
Zyprexa可能会增加患有痴呆症相关精神病的老年人的死亡风险,因此未经批准。
如果可能,在收到Zyprexa Relprevv之前,请告诉您的医生是否曾经:
自杀念头或行为;
肝病;
心脏病,高血压或高血压;
高胆固醇或甘油三酸酯;
中风,包括“中风”;
乳腺癌;
癫痫发作;
阿尔茨海默氏病;
糖尿病或高血糖;
前列腺肿大;
肠问题;要么
窄角型青光眼。
告诉医生您是否怀孕。在怀孕的最后三个月使用抗精神病药可能会导致新生儿呼吸困难,进食困难或戒断症状。
告诉医生您是否正在母乳喂养。奥氮平可进入母乳,并可能对哺乳婴儿产生副作用。
在紧急情况下,您可能无法告知护理人员您是孕妇还是母乳喂养。确保有任何照顾您怀孕的医生,或者您的宝宝知道您收到了这种药。
Zyprexa Relprevv未被18岁以下的任何人使用。
Zyprexa Relprevv如何服用?
Zyprexa Relprevv被注射到肌肉中。您将在诊所或医院接受注射。
Zyprexa Relprevv通常只给出一次。如果2小时后您仍然有症状,您的看护人可能会使用第二或第三剂。
Zyprexa Relprevv可能会导致ir妄症状(突然的严重混乱,迷失方向,躁动,言语或行走问题)或嗜睡,足以使您陷入昏迷状态。注射后至少三个小时将密切注视您。
如果我错过剂量怎么办?
由于Zyprexa Relprevv是在紧急情况下由医护人员提供的,因此您不太可能会错过剂量。
如果我服药过量怎么办?
由于这种药物是由医疗专业人员在医疗环境中服用的,因此服用过量的可能性不大。
收到Zyprexa Relprevv后应该避免什么?
避免喝酒。可能发生危险的副作用。
奥氮平会引起严重的嗜睡,并可能损害您的思维或反应。注射后,您必须在医疗机构停留至少3个小时,并且一天中其余时间都不应开车。
避免从坐着或躺着的姿势站起来太快,否则您可能会感到头晕。头晕或严重嗜睡会导致跌倒,骨折或其他伤害。
Zyprexa Relprevv副作用
如果您对Zyprexa有过敏反应迹象,请寻求紧急医疗帮助。呼吸困难;脸,嘴唇,舌头或喉咙肿胀。
如果您有严重的药物反应会影响身体的许多部位,请寻求治疗。症状可能包括:皮疹,发烧,腺体肿胀,流感样症状,肌肉酸痛,严重虚弱,异常瘀青或皮肤或眼睛发黄。
如果药物进入您的血液中的速度太快,Zyprexa Relprevv可能会导致严重的症状。注射后的前三个小时内,您将被观察到以下症状:
严重头晕,嗜睡或虚弱;
混乱,焦虑,生气或敌对;
感到紧张或动摇;
走路或说话有麻烦;
癫痫发作(抽搐);要么
一种轻松的感觉,就像你可能昏倒了一样。
如果您有以下情况,请立即致电您的医生:
眼睛,嘴唇,舌头,脸,手臂或腿的抽搐或无法控制的运动;
说话或吞咽困难;
脱水的迹象-如果您感到非常口渴或发烧,无法排尿,出汗过多或皮肤又干又热;
高血糖-口渴,排尿增加,饥饿,口干,果味气息;要么
严重的神经系统反应-肌肉非常僵硬(僵硬),发烧,出汗,精神错乱,心律快速或不均匀,震颤。
常见的Zyprexa副作用可能包括:
头痛,背痛;
体重增加(青少年更有可能),食欲增加;
睡意;
口干,恶心,呕吐,腹泻;
鼻窦疼痛,流鼻涕或鼻塞,咳嗽;要么
注射疼痛。
这不是副作用的完整列表,并且可能会发生其他副作用。打电话给您的医生,征求有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。
还有哪些其他药物会影响Zyprexa Relprevv?
将Zyprexa与其他使您困倦或呼吸缓慢的药物一起使用可能会导致危险或威胁生命的副作用。在使用阿片类药物,安眠药,肌肉松弛药或抗焦虑药或癫痫药之前,请先咨询医生。
其他药物可能会与奥氮平发生相互作用,包括处方药和非处方药,维生素和草药产品。告诉您的医生您目前所有的药物以及您开始或停止使用的任何药物。
版权所有1996-2020 Cerner Multum,Inc.版本:4.01。
注意:本文档包含有关奥氮平的副作用信息。此页面上列出的某些剂型可能不适用于Zyprexa Relprevv品牌。
对于消费者
适用于奥氮平:口服片剂,口服片剂崩解
其他剂型:
- 肌内粉剂溶液,肌内粉剂悬液缓释
警告
口服途径(片剂;片剂,崩解)
用抗精神病药治疗的老年痴呆症相关精神病患者的死亡风险增加。尽管临床试验中的死亡原因多种多样,但大多数死亡似乎是自然界的心血管疾病(例如,心力衰竭,猝死)或传染性疾病(例如,肺炎)。观察性研究表明,抗精神病药可能会增加死亡率。从这些研究中尚不清楚死亡率发现在多大程度上可归因于抗精神病药而不是患者的特征。奥氮平未被批准用于治疗与痴呆相关的精神病患者。
需要立即就医的副作用
奥氮平(Zyprexa Relprevv中包含的活性成分)及其所需的作用可能会引起某些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
服用奥氮平时,如果有下列任何副作用,请立即咨询医生:
比较普遍;普遍上
- 脸,手臂,手,小腿或脚肿胀或肿胀
- 模糊的视野
- 视力改变
- 步行和平衡变化
- 笨拙或不稳定
- 说话困难
- 吞咽困难
- 流口水
- 视力受损
- 无法坐下来
- 失去平衡控制
- 面具般的脸
- 肌肉颤抖,抽搐或僵硬
- 需要继续前进
- 体重快速增加
- 躁动
- 洗牌走
- 动作缓慢
- 言语不清
- 手臂和腿部的僵硬
- 头部,脸部,嘴部和颈部的抽动状运动
- 手或脚刺痛
- 手指,手,脚,腿或手臂发抖或颤抖
- 身体的扭曲运动
- 不受控制的运动,尤其是脸部,颈部和背部的运动
- 体重异常增加或减少
不常见
- 膀胱疼痛
- 血尿或浑浊
- 瘀血
- 燃烧,爬行,发痒,麻木,刺,“针刺”或刺痛感
- 胸痛
- 呼吸困难或劳累
- 排尿困难,灼热或疼痛
- 头晕
- 肌肉过度紧张
- 尿频
- 头痛
- 无法移动眼睛
- 眨眼或眼睑痉挛增加
- 阴道或生殖器部位瘙痒
- 缺乏协调
- 皮肤上的大块,扁平,蓝色或紫色的斑块
- 失去膀胱控制
- 记忆力减退
- 下背部或侧面疼痛
- 肌肉紧张或紧绷
- 紧张
- 性交时的疼痛
- 敲打耳朵
- 记忆问题
- 肌肉的节奏运动
- 缓慢,快速,剧烈或不规则的心跳或脉搏
- 说话比平常不太清晰
- 伸出舌头
- 白带厚实,白带,无异味或有轻微气味
- 胸闷
- 抽搐
- 颈部,躯干,手臂或腿部的不受控制的扭曲运动
- 身体或面部动作异常或不完整
- 胳膊和腿无力
不需要立即就医的副作用
奥氮平可能会出现一些通常不需要医疗的副作用。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。
请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
比较普遍;普遍上
- 胃酸或酸
- 背疼
- ching
- 性格改变
- 排便困难(凳子)
- 灰心
- 感到悲伤或空虚
- 发热
- 胃灼热
- 食欲增加
- 咳嗽加剧
- 消化不良
- 食欲不振
- 力量不足或丧失
- 失去兴趣或愉悦
- 流鼻涕
- 打喷嚏
- 胃部不适,不适或疼痛
- 鼻塞
- 口渴
- 睡眠困难
- 注意力不集中
- 浇水
不常见
- 皮肤上有瑕疵
- 身体疼痛或疼痛
- 发冷
- 冷汗
- 拥塞
- 咳嗽
- 皮肤干燥
- 喉咙干燥或酸痛
- 错误或异常的幸福感
- 月经大量出血(经期)
- 嘶哑
- 关节痛
- 缺乏感觉或情感
- 腿抽筋
- 手臂或腿部疼痛
- 青春痘
- 出汗
- 脖子上的腺体肿胀
- 漠不关心的感觉
- 声音变化
- 呕吐
对于医疗保健专业人员
适用于奥氮平:注射用肌肉粉,缓释注射用肌肉粉,口服片剂,口服片剂崩解
神经系统
注射后del妄/镇静综合症后,曾报道过与过量注射IM悬液注射后过量服用奥氮平(Zyprexa Relprevv中包含的活性成分)一致的体征和症状。在不到46%的时间内,事件发生率不到0.1%,约有2%的患者接受过事件。事件的发生范围从注射后不久到超过3小时不等。大多数患者住院,并且需要一些支持治疗,包括插管。据报道,在接受适当剂量的缓释IM悬液后3至4天有2人死亡。在这些患者中,死亡后报告奥氮平血药浓度很高。为确定这2例死亡中药物水平升高的原因而进行的研究提供了不确定的结果。正如美国食品药品监督管理局(FDA)在2015年3月23日发布的药物安全通讯中所报道的那样,对动物的一项研究发现,死亡后许多药物水平的升高可能已经发生,但是死亡的原因可能是快速,但是不能排除药物延迟进入血流的情况。
静坐不全最常见于口服剂量为15毫克/天;静坐事件包括静坐和运动亢进。
运动障碍事件包括颊舌综合症,舞蹈性运动症,运动障碍和迟发性运动障碍。
肌张力障碍事件包括肌张力障碍,全身性痉挛,颈部僵硬,眼科疾病,阿司匹林和斜颈。
帕金森病/帕金森病事件最常发生在口服剂量为15 mg / day的情况下,包括运动障碍,钝齿轮僵硬,锥体外系综合征,肌张力亢进,运动不足,掩盖相和震颤。
镇静最常见于青春期患者,三周内口服剂量至少2.5 mg /天;镇静包括失眠,嗜睡,镇静和嗜睡。
嗜睡和震颤最常见于口服锂或丙戊酸盐时。 [参考]
口服配方:
非常常见(10%或更多):嗜睡(最高52%),镇静(最高48%),静坐/静坐事件(最高27%),震颤(最高23%),帕金森综合症/帕金森综合症(最高至20%),头晕(至多18%),头痛(至多17%),任何锥体外系事件(至多10%)
常见(1%至10%):步态异常,健忘症,关节运动障碍,运动障碍/运动障碍事件,肌张力障碍/肌张力障碍事件,肌张力亢进,不协调,轻度/暂时性抗胆碱作用,感觉异常,言语障碍
罕见(0.1%至1%):共济失调,脑血管意外,构音障碍,不安腿综合征,癫痫发作,木僵,迟发性运动障碍
罕见(0.01%至0.1%):昏迷,宿醉效应,抗精神病药物恶性综合症
未报告的频率:运动障碍,舞蹈性运动症,齿轮僵直,运动障碍,肌张力障碍,锥体束外异常,全身性痉挛,失眠,运动减退,掩盖相,运动障碍,肌阵挛,视神经痛,迟发性运动障碍,抽搐
上市后报告:糖尿病昏迷
立即释放IM注入:
非常常见(10%或更高):镇静剂(最高44.1%)
常见(1%到10%):步态异常,静坐/静坐事件,锥体外系事件,头晕,帕金森/帕金森病,嗜睡,语言障碍,震颤
罕见(0.1%至1%):健忘症,不安腿综合征,晕厥
未报告的频率:运动障碍,舞蹈性运动症,齿轮僵硬,运动障碍,运动障碍事件,肌张力障碍,肌张力障碍事件,锥体外系疾病,全身性痉挛,运动亢进,失眠,肌张力亢进,运动障碍,掩盖相,运动障碍,肌阵挛,轻度脊柱炎
上市后报告:糖尿病昏迷,抗精神病药物恶性综合症,惊厥
扩展发行的IM注入:
非常常见(10%或更多):头痛/紧张性头痛(高达18%),镇静/嗜睡(高达13%)
常见(1%至10%):运动障碍,头晕,构音障碍,运动障碍,失眠,轻度/暂时性抗胆碱能作用,帕金森氏症,震颤
罕见(0.1%至1%):健忘症,肌张力障碍,癫痫发作,腿不安综合征,迟发性运动障碍
稀有(0.01%至0.1%):抗精神病药恶性综合症
未报告频率:步态异常,共济失调,脑血管不良反应,昏迷,惊厥,肌张力障碍,锥体外系症状,语言障碍,迟发性锥体外系综合征
上市后报告:糖尿病昏迷[参考]
心血管的
从17项安慰剂对照临床研究(n = 5106)中收集的涉及非典型抗精神病药(包括奥氮平(Zyprexa Relprevv中的活性成分)的使用)的治疗性治疗的老年痴呆症患者的行为发生风险药物治疗患者的死亡率是安慰剂治疗患者的1.6至1.7倍。试验的平均持续时间为10周,在大多数情况下(虽然不是全部),死因被报告为自然界中的心血管疾病(例如,心力衰竭,猝死)或传染性疾病(例如,肺炎)。 Olanzapine未获FDA批准用于治疗老年痴呆症患者的行为障碍。 [参考]
口服配方:
常见(1%至10%):胸痛,水肿,高血压,周围性水肿,体位/体位性低血压,心动过速
罕见(0.1%至1%):心动过缓,深静脉血栓形成,QT延长,血管舒张
罕见(0.01%至0.1%):室性心动过速/纤颤
上市后报告:心脏骤停,足尖扭转,静脉血栓栓塞事件,静脉血栓栓塞,室性心律失常
立即释放IM注入:
常见(1%至10%):心动过缓,低血压,周围性水肿,体位/体位性低血压,心动过速
罕见(0.1%至1%):光敏反应
售后报告:深静脉血栓形成,心脏骤停,QT延长,足尖扭转症,静脉血栓栓塞事件,静脉血栓栓塞,室性心律失常
扩展发行的IM注入:
常见(1%至10%):心律失常伴/不伴低血压/晕厥,水肿,经心电图QT校正的间隔时间延长,高血压,低血压,体位性低血压,周围性水肿,心动过速
罕见(0.1%至1%):深静脉血栓形成,血栓栓塞
罕见(0.01%至0.1%):室性心动过速/纤颤
上市后报告:心脏骤停,深静脉血栓形成,尖尖扭转型动脉瘤,静脉血栓栓塞事件/静脉血栓栓塞[参考]
新陈代谢
口服配方:
非常常见(10%或更多):体重增加/体重增加大于/等于基线体重的7%(高达89.4%),对高甘油三酸酯禁食(至59.5%),对高总胆固醇禁食(最高38.9%),食欲增加(最高29%),正常至高甘油三酸酯禁食(最高26.9%),禁食至高葡萄糖(最高14.3%)口渴(最高10%)
常见(1%至10%):空腹至高血糖,空腹至高总胆固醇,高尿酸,高血糖,碱性磷酸酶增加,甘油三酸酯水平增加,体重增加大于/等于基线体重的15%
罕见(0.1%至1%):伴或不伴酮症酸中毒或昏迷(有时是致命的)的糖尿病发展/加重
上市后报告:糖尿病酮症酸中毒,高甘油三酯血症,随机胆固醇水平为240 mg / dL或更高,随机甘油三酸酯水平为1000 mg / dL或更高
立即释放IM注入:
非常常见(10%或更多):体重增加/体重增加/等于基线体重的7%(最高89.4%),禁忌高甘油三酸酯/高甘油三酯血症(最高70.7%),禁食至高甘油三酸酯总胆固醇/高胆固醇血症(最高55.2%),高血糖/高血糖(最高26%)禁食
普通(1%至10%):食欲增加,体重增加大于/等于基线体重的15%
上市后报告:糖尿病酮症酸中毒,先前存在的糖尿病加重,随机胆固醇水平为240 mg / dL或更高,随机甘油三酸酯水平为1000 mg / dL或更高
扩展发行的IM注入:
非常常见(10%或更多):体重增加/体重增加大于/等于基线体重的7%(高达64.4%)
常见(1%到10%):对高胆固醇/葡萄糖/甘油三酸酯的禁食临界,对高胆固醇/甘油三酸酯/葡萄糖的正常禁食,高尿酸,碱性磷酸酶增加,食欲增加,体重增加大于/等于15%基线体重
罕见(0.1%至1%):伴或不伴酮症酸中毒或昏迷(有时是致命的)的糖尿病发展/加重
未报告频率:胆固醇/低密度脂蛋白/甘油三酸酯/钠的变化
上市后报告:糖尿病性酮症酸中毒,高血糖症,随机胆固醇水平为6.21 mmol / L或更高,随机甘油三酸酯水平为11.29 mmol / L或更高[参考]
与其他一些非典型抗精神病药相比,奥氮平在增加葡萄糖水平方面似乎具有更大的关联性。据报道,平均增加量高达15 mg / dL。在基线时有葡萄糖失调迹象的患者中,平均血糖变化差异更大。在对完成9到12个月治疗的患者进行的分析中,大约6个月后,平均血糖升高的速度减慢了。
已经观察到脂质的临床显着改变,包括血清甘油三酸酯升高超过500 mg / dL。在成人至少48周的长期研究中,平均空腹胆固醇,LDL,甘油三酸酯分别比基线增加了5.6 mg / dL,2.5 mg / dL和18.7 mg / dL。在基线时没有脂质失调迹象的患者中,空腹血脂值(总胆固醇,LDL和甘油三酸酯)的平均增加幅度更大。
在13个安慰剂对照的单一疗法试验中,奥氮平治疗的患者平均增加2.6千克,而安慰剂患者的平均减轻0.3千克。 22.5%的人至少增加了其基线重量的7%,4.2%的患者至少增加了基线的15%(而安慰剂组分别为3%和0.3%)。在所有基线BMI上均观察到临床上体重显着增加。长期暴露(至少24周)后,体重增加7%,15%或25%或更高,分别为89.4%,55.3%和29.1%。据报道,在短期治疗(约22天)中,接受这种药物的青少年体重增加和食欲增加的比例分别为40.6%,7.1%和2.5%。 [参考]
胃肠道
腹痛包括腹痛,下腹痛和上腹痛。
据报道,恶心和口干与剂量有关。口服锂或丙戊酸盐时口干比较常见。 [参考]
口服配方:
非常常见(10%或更多):口干(最高32%),便秘(最高11%),消化不良(最高11%)
常见(1%至10%):腹痛,腹泻,消化不良,流涎增加,恶心,呕吐
罕见(0.1%至1%):腹胀,舌头浮肿
罕见(0.01%至0.1%):肠梗阻,肠梗阻,胰腺炎
未报告频率:颊舌综合征,下/上腹痛
立即释放IM注入:
常见(1%至10%):便秘,口干
罕见(0.1%至1%):腹胀,恶心
未报告频率:颊舌综合征
上市后报告:胰腺炎,呕吐
扩展发行的IM注入:
常见(1%至10%):腹痛/上腹痛,便秘,腹泻,口干,肠胃气胀,恶心,牙痛,牙齿感染/脓肿,呕吐
罕见(0.1%至1%):腹胀
稀有(0.01%至0.1%):胰腺炎[参考]
肝的
肝转氨酶的短暂,无症状升高是常见现象,尤其是在治疗初期。 [参考]
口服配方:
非常常见(10%或更高):AST升高(最高27.6%),总胆红素降低(最高22.1%),ALT正常水平上限的3倍(3 x ULN)(最高12.1%)
常见(1%至10%):无症状肝酶升高(ALT,AST),高γ-谷氨酰转移酶(GGT)
罕见(0.1%至1%):胆红素血症/总胆红素增加
稀有(0.01%至0.1%):脂肪肝沉积
未报告频率:肝炎,肝细胞/胆汁淤积性肝炎,混合性肝损伤
上市后报告:黄疸
立即释放IM注入:
非常常见(10%或更高):AST升高(高达27.6%),总胆红素降低(高达22.1%),ALT 3 x ULN(高达12.1%)
上市后报告:胆汁淤积性/混合性肝损伤,黄疸,总胆红素增加
扩展发行的IM注入:
常见(1%至10%):ALT 3 x ULN,高GGT水平,无症状肝酶升高(ALT,AST),肝酶升高(AST,ALT,GGT),总胆红素低
罕见(0.1%至1%):ALT升高大于200国际单位/ L,总胆红素增加
罕见(0.01%至0.1%):肝细胞/胆汁淤积性肝炎,混合性肝损伤
未报告频率:直接胆红素/ GGT改变
上市后报告:黄疸[参考]
呼吸道
口服配方:
常见(1%至10%):呼吸困难,咳嗽加剧,鼻咽炎,咽炎,呼吸道感染,鼻炎,鼻窦炎
罕见(0.1%至1%):鼻出血,肺栓塞
罕见(0.01%至0.1%):肺水肿
未报告频率:下呼吸道感染,肺炎,上呼吸道感染,病毒性呼吸道感染,病毒性上呼吸道感染
立即释放IM注入:
常见(1%至10%):肺炎
罕见(0.1%至1%)::光
上市后报告:肺栓塞
扩展发行的IM注入:
常见(1%至10%):咳嗽,鼻/窦充血,鼻咽炎,咽喉痛,打喷嚏,上呼吸道感染
罕见(0.1%至1%):鼻出血,肺栓塞
稀有(0.01%至0.1%):
未报告频率:肺炎[参考]
内分泌
在临床研究中,发现催乳素水平的变化在统计学上基于剂量存在显着差异,较高的剂量与较高的催乳激素水平相关。在长达12周的研究中,约30%基线泌乳素基线值正常的患者的血浆泌乳素浓度超过了正常上限(ULN)。这些升高大多数是轻微的,并保持在2倍ULN以下。
与成人相比,大约47%的治疗青少年患者的催乳素水平明显更高。 [参考]
口服配方:
非常常见(10%或更高):催乳素水平升高(高达47.4%)
罕见(0.1%至1%):男性乳房发育症/男性乳房增大
立即释放IM注入:
非常常见(10%或更多):催乳素增加(高达47.4%)
罕见(0.1%至1%):男性乳房发育症/男性乳房增大
扩展发行的IM注入:
非常常见(10%或更多):血浆催乳素水平升高(高达30%)
罕见(0.1%至1%):男性乳房发育症/男性乳房增大[参考]
血液学
口服配方:
常见(1%至10%):嗜酸性粒细胞增多,白细胞减少,中性粒细胞减少
罕见(0.1%至1%):血小板减少症,血栓栓塞
立即释放IM注入:
常见(1%至10%):嗜酸性粒细胞增多,白细胞减少,中性粒细胞减少
上市后报告:血小板减少
扩展发行的IM注入:
常见(1%至10%):嗜酸性粒细胞增多,白细胞减少,中性粒细胞减少
稀有(0.01%至0.1%):血小板减少
未报告频率:单核细胞/嗜酸性粒细胞变化,白细胞计数高,治疗后血小板计数低[参考]
眼科
口服配方:
常见(1%至10%):弱视,视力异常
罕见(0.1%至1%):适应异常,干眼,眼科
稀有(0.01%至0.1%):瞳孔散大
未报告频率:眼科危机
立即释放IM注入:
未报告频率:眼科危机
扩展发行的IM注入:
罕见(0.1%至1%):排卵[参考]
其他
口服配方:
非常常见(10%或更多):虚弱(最高20%),疲劳(最高14%),意外伤害(最高12%)
常见(1%至10%):发烧/发热,肢体疼痛(关节除外),嗜睡,残余事件,非特异性事件
罕见(0.1%至1%):寒冷
稀有(0.01%至0.1%):寒冷和发烧,体温过低,猝死/无法解释的猝死
未报告频率:跌倒,体温升高,新生儿停药综合征
立即释放IM注入:
常见(1%至10%):乏力,疲劳,发热,残留事件
不报告频率:跌倒,嗜睡
上市后报告:突然的无法解释的死亡
扩展发行的IM注入:
常见(1%至10%):乏力,耳痛,疲劳,发烧/发热,用药过量,疼痛,程序性疼痛
稀有(0.01%至0.1%):体温过低
未报告的频率:死亡,跌倒,体温升高,嗜睡,新生儿停药综合征,突然死亡/无法解释的死亡,无力[参考]
乏力最常见于口服剂量为15毫克/天。
残留事件包括运动障碍,肌阵挛和抽搐。 [参考]
过敏症
口服配方:
罕见(0.1%至1%):过敏
上市后报告:过敏反应,类过敏反应,血管性水肿
立即释放IM注入:
上市后报告:过敏反应,类过敏反应,血管性水肿
扩展发行的IM注入:
罕见(0.1%至1%):过敏
上市后报告:过敏反应,类过敏反应,血管性水肿[参考]
泌尿生殖
口服配方:
常见(1%至10%):痛经,勃起功能障碍,糖尿,尿失禁,尿路感染,阴道炎
少见(0.1%至1%):闭经,乳房增大/疼痛,月经减少,溢乳,排尿障碍,阳imp,月经增加,月经过多,出血,多尿,尿频,尿频,尿s,尿retention留,尿急
稀有(0.01%至0.1%):狂妄
立即释放IM注入:
常见(1%至10%):勃起功能障碍,尿失禁
罕见(0.1%至1%):闭经,乳房增大,溢乳
上市后报告:精神分裂症,犹豫,尿retention留
扩展发行的IM注入:
常见(1%至10%):勃起功能障碍,白带
罕见(0.1%至1%):闭经,乳房增大,溢乳,尿,、尿失禁,尿retention留
稀有(0.01%至0.1%):狂妄[参考]
肌肉骨骼
口服配方:
常见(1%至10%):关节痛,背痛,肌酸/肌酸酐磷酸激酶高,关节痛,肌肉骨骼僵硬
稀有(0.01%至0.1%):骨质疏松,横纹肌溶解
未报告频率:颈部僵硬,斜颈
立即释放IM注入:
常见(1%至10%):关节痛
罕见(0.1%至1%):肌酸酐磷酸激酶升高
稀有(0.01%至0.1%):肌酸激酶水平升高
未报告频率:颈部僵硬,斜颈
上市后报告:横纹肌溶解
扩展发行的IM注入:
常见(1%至10%):关节痛,背痛,肌酸磷酸激酶高,肌肉痉挛,肌肉骨骼痉挛
稀有(0.01%至0.1%):横纹肌溶解[参考]
皮肤科
口服配方:
常见(1%至10%):痤疮,皮肤干燥,瘀斑,皮疹,出汗/发汗
罕见(0.1%至1%):脱发,面部浮肿,光敏反应
未报告频率:药物反应与嗜酸性粒细胞增多和全身症状(DRESS),红斑,瘙痒,荨麻疹
立即释放IM注入:
上市后报告:脱发,嗜酸性粒细胞增多和全身症状(DRESS)的药物反应,瘙痒,皮疹,出汗/发汗,荨麻疹
扩展发行的IM注入:
常见(1%至10%):痤疮,皮疹
罕见(0.1%至1%):脱发,光敏反应
频率未报告:出汗/出汗,红斑
上市后报告:药物反应与嗜酸性粒细胞增多和全身症状(DRESS),瘙痒,荨麻疹[参考]
精神科
为了收集不良反应,使用人格障碍一词来收集有关非攻击性不良行为的数据。
抑郁症最常见的是口服锂或丙戊酸盐。 [参考]
口服配方:
非常常见(10%或更多):抑郁症(高达18%),失眠(高达12%)
常见(1%至10%):冷漠,困惑,性欲降低,欣快,人格障碍,躁动不安
罕见(0.1%至1%):自杀未遂
稀有(0.01%至0.1%):停药症状
未报告频率:焦虑,视觉幻觉/幻觉
上市后报告:停产反应
立即释放IM注入:
普通(1%至10%):性欲降低
未报告频率:幻觉
上市后报告:焦虑,停药反应,失眠
扩展发行的IM注入:
常见(1%至10%):异常的梦想,异常的思维,听觉幻觉,性欲下降,躁动不安,睡眠障碍
稀有(0.01%至0.1%):停药反应/症状
未报告的频率:攻击性,躁动,焦虑,意识错乱,ir妄,幻觉,失眠,其他认知障碍,视觉幻觉[参考]
本地
立即释放IM注入:
常见(1%至10%):注射部位疼痛
扩展发行的IM注入:
常见(1%至10%):麻醉,淤青,臀部疼痛,出血,硬结,注射部位硬结/肿块/疼痛,刺激
罕见(0.01%至0.1%):注射部位脓肿需要/不需要手术干预
未报告频率:水肿型反应,红斑型反应,结节型反应,非特异性注射部位反应[参考]
免疫学的
扩展发行的IM注入:
常见(1%至10%):病毒感染[参考]
肾的
口服配方:
常见(1%至10%):糖尿
立即释放IM注入:
常见(1%至10%):糖尿
扩展发行的IM注入:
常见(1%至10%):糖尿症[参考]
参考文献
1. FDA。美国食品药品监督管理局“ Zyprexa Relprevv(奥氮平)”:药物安全通讯-FDA的研究回顾揭示了与可注射的精神分裂症药物相关的两例死亡。 MedWatch / SafetyInformation / SafetyAlertsforHu”([2015年3月23日]):
2.“产品信息。Zyprexa(奥氮平)。”印第安纳州印第安纳波利斯的礼来公司和礼来公司。
3.“产品信息。ZyPREXA Relprevv(奥氮平)。”印第安纳州印第安纳波利斯的礼来公司和礼来公司。
4. Cerner Multum,Inc.“澳大利亚产品信息”。 00
5. Cerner Multum,Inc.“英国产品特性摘要”。 00
某些副作用可能没有报道。您可以将其报告给FDA。
维持治疗—尽管尚未进行任何对照研究来确定应使用ZYPREXA RELPREVV治疗多长时间,但已在稳定的精神分裂症患者的24周内证明了疗效。此外,长期服用ZYPREXA可以有效地维持精神分裂症的治疗反应。应该定期对患者进行重新评估,以确定是否需要继续治疗。
从其他抗精神病药物转换—没有系统收集的数据来具体说明如何将精神分裂症患者从其他抗精神病药物转换为ZYPREXA RELPREVV。
重组和管理ZYPREXA RELPREVV的说明
仅用于深层肌内注射。不要静脉内或皮下注射。
只要溶液和容器允许,在给药前应目视检查肠胃外药品是否有颗粒物质和变色。
步骤1:准备材料
便利套件包括:
- 小瓶ZYPREXA RELPREVV粉
- 3 mL稀释液瓶
- 一个3毫升的注射器与预先连接的19号,1.5英寸(38 MM)注射针-PRO®与针头保护装置针
- 两根19号1.5英寸(38毫米)皮下注射针-带针头保护装置
- —对于肥胖患者,可以使用2英寸(50毫米),19规格或更大的针头(不包括在便利工具包中)进行给药。
ZYPREXA RELPREVV必须仅使用便利工具包中提供的稀释剂来悬挂。
建议在重构时使用手套,因为ZYPREXA RELPREVV可能会刺激皮肤。如果与皮肤接触,请用水冲洗。
有关安全有效地使用Hypodermic Needle-Pro注射器和针头的更多信息,请参见标题为“重组和管理ZYPREXA RELPREVV的说明”的附加插页。
步骤2:确定复原量
请参考下表以确定稀释到每种粉末强度中要添加到粉末中的稀释剂的量。
重要的是要注意,小瓶中的稀释剂多于重构所需的稀释剂。
| 剂量 | 样品瓶强度 | 稀释剂添加 |
| 150毫克 | 210毫克 | 1.3毫升 |
| 210毫克 | 210毫克 | 1.3毫升 |
| 300毫克 | 300毫克 | 1.8毫升 |
| 405毫克 | 405毫克 | 2.3毫升 |
步骤3:重构ZYPREXA RELPREVV
在继续进行步骤3之前,请阅读《皮下注射针-Pro使用说明》。不遵守这些说明可能会导致针刺受伤。
轻拍小瓶以松开粉末。
打开预先包装的皮下注射针-Pro注射器和带针头保护装置的针头。
将预定的稀释剂体积(步骤2)抽入注射器中。
将稀释剂注入粉末瓶中。
稍微向后拉注射器中的柱塞,抽出空气以平衡小瓶中的压力。
从样品瓶中取出针头,将样品瓶直立以防止材料损失。
接合针头安全装置(请参阅完整的《皮下注射针-Pro使用说明》)。
垫硬表面以缓冲冲击力(请参见图1)。用力地反复轻敲小瓶的表面,直到看不到粉末为止。
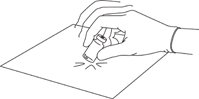 |
| 图1:用力敲打混合。 |
目视检查小瓶是否结块。未悬浮的粉末显示为黄色,干燥的团块,粘在小瓶上。如果大的团块保持附加攻丝可能需要(参见图2)。
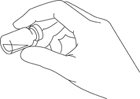 |
| 图2:检查未悬浮的粉末,并在需要时重复轻拍。 |
剧烈摇动小瓶,直到悬浮液看起来光滑且颜色和质地一致为止。悬浮的产品将为黄色且不透明(请参见图3)。
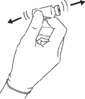 |
| 图3:剧烈摇动小瓶。 |
如果形成泡沫,则让小瓶直立以使泡沫消散。
如果不立即使用产品,则应大力摇晃以重新悬浮。重构后的ZYPREXA RELPREVV在室温下可在小瓶中保持稳定长达24小时。
步骤4:注射ZYPREXA RELPREVV
在进行3个小时的观察期后,在进行注射之前,请确认会有人陪伴患者。如果无法确认,则不要注射。
请参阅下表确定要注入的最终体积。悬浮液浓度为150 mg / mL ZYPREXA RELPREVV。
| 剂量 | 最终注射量 |
| 150毫克 | 1毫升 |
| 210毫克 | 1.4毫升 |
| 300毫克 | 2毫升 |
| 405毫克 | 2.7毫升 |
将新的安全针连接到注射器上。
将所需的量缓慢地抽回注射器中。
一些多余的产品将保留在小瓶中。
接合针头安全装置,然后从注射器中取出针头。
要进行给药,请选择带有针头保护装置的19口径1.5英寸(38毫米)皮下注射针-Pro针头。对于肥胖患者,可以使用2英寸(50毫米),19规格或更大的针头(不包括在便利工具包中)。为防止堵塞,必须使用19号或更大号的针头。
注射前,将新的安全针连接到注射器上。从小瓶中取出悬浮液后,应立即注射。
仅用于深层肌内注射。不要静脉内或皮下注射。
选择并准备在臀区域注射的部位。
将针头插入肌肉后,抽吸数秒钟以确保没有血液出现。如果将任何血液吸入注射器,请丢弃注射器和该剂量,并从新的便利工具箱开始。注射应在稳定,连续的压力下进行。
不要按摩注射部位。
接合针头安全装置。
进样后,请妥善处理小瓶,针头和注射器。该小瓶仅供一次性使用。
注射后Deli妄/镇静综合症—注射Zyprexa Relprevv后,不良反应的体征和症状与奥氮平过量有关,特别是镇静(包括昏迷)和/或ir妄。 Zyprexa Relprevv必须在已注册的医疗机构中进行管理,并且可以随时使用紧急响应服务。每次注射后,医护人员必须在医疗机构对患者进行至少3个小时的观察。由于这种风险,接受Zyprexa Relprevv是只能通过所谓的接受Zyprexa Relprevv病人护理程序的限制分配方案,需要处方,医疗机构,患者和药店招生[见剂量和给药方法( 2.1 ),警告和注意事项( 5.1 , 5.2 ) ,过量( 10.2 )和患者咨询信息( 17 )] 。
老年痴呆症相关精神病患者的死亡率增加—用抗精神病药治疗的老年痴呆症相关精神病患者的死亡风险增加。十七项安慰剂对照试验(模式持续时间为10周)的分析(主要是在服用非典型抗精神病药的患者中)显示,接受药物治疗的患者的死亡风险是接受安慰剂治疗的患者死亡风险的1.6至1.7倍。在一个典型的10周对照试验过程中,药物治疗患者的死亡率约为4.5%,而安慰剂组的死亡率约为2.6%。尽管死亡原因多种多样,但大多数死亡似乎是自然界的心血管疾病(例如,心力衰竭,猝死)或传染性疾病(例如,肺炎)。观察性研究表明,与非典型抗精神病药类似,常规抗精神病药治疗可能会增加死亡率。尚不清楚观察性研究中死亡率增加的结果在多大程度上可归因于抗精神病药,而不是患者的某些特征。 Zyprexa Relprevv未被批准用于治疗与痴呆相关的精神病患者[请参阅警告和注意事项( 5.3 ),在特定人群中使用( 8.5 )和患者咨询信息( 17 )] 。
Zyprexa Relprevv的适应症和用法
Zyprexa Relprevv仅可通过受限制的分发程序获得(请参阅“警告和注意事项( 5.2 )”) 。 Zyprexa Relprevv不得直接分配给患者。为了使患者能够接受治疗,开药者,医疗机构,患者和药房都必须加入Zyprexa Relprevv患者护理计划。要注册,请致电1-877-772-9390。
精神分裂症
Zyprexa Relprevv适用于精神分裂症的治疗。在精神分裂症患者的两项临床试验中确定了疗效:一项在成人中进行的8周试验和一项在成年人中进行的维持试验[见临床研究( 14.1 )] 。
Zyprexa Relprevv剂量和用法
剂量
Zyprexa Relprevv仅用于肌肉内臀深部注射,不应静脉内或皮下给药。
请注意,有两种ZYPREXA肌内制剂的给药时间表不同。 ZYPREXA肌内注射剂(10 mg /小瓶)是短效制剂,请勿与Zyprexa Relprevv混淆。有关该产品的更多信息,请参考ZYPREXA IntraMuscular的包装说明书。
在开始治疗之前,先与口服奥氮平建立耐受性。
Zyprexa Relprevv应每2至4周由医疗专业人员使用19号1.5英寸针头进行深肌内臀肌注射来给药。将针头插入肌肉后,应保持抽吸几秒钟,以确保没有血液进入注射器。如果将任何血液吸入注射器,应将其丢弃,并应使用新的便利工具包准备新鲜药物。注射应在稳定,连续的压力下进行。不要按摩注射部位。
剂量选择-Zyprexa Relprevv的功效已证明在每2周施用150 mg至300 mg和每4周施用405 mg的范围内。表1列出了考虑口服ZYPREXA和Zyprexa Relprevv的剂量建议。
目标口服ZYPREXA剂量 | 前8周的Zyprexa Relprevv剂量 | Zyprexa Relprevv治疗8周后的维持剂量 |
| 10毫克/天 | 210 mg / 2周或 | 150 mg / 2周或 |
| 405毫克/ 4周 | 300毫克/ 4周 | |
| 15毫克/天 | 300毫克/ 2周 | 210 mg / 2周或 |
| 405毫克/ 4周 | ||
| 20毫克/天 | 300毫克/ 2周 | 300毫克/ 2周 |
Zyprexa Relprevv剂量每4周大于405 mg或每2周大于300 mg尚未在临床试验中进行评估。
注射后Deli妄/镇静综合症—在上市前临床研究中,据报道,Zyprexa Relprevv注射后的患者出现不良反应,其症状和体征与奥氮平过量有关,尤其是镇静(包括昏迷)和/或del妄[参见盒装警告,警告和注意事项( 5.1 )和过量( 10.1 )] 。应告知患者这种风险以及如何识别相关症状[参见患者咨询信息( 17 )] 。 Zyprexa Relprevv必须在已注册的医疗机构中进行管理,并且可以随时使用紧急响应服务。每次Zyprexa Relprevv注射后,医护人员必须在医疗机构连续观察患者至少3小时,观察是否出现与奥氮平用药过量相一致的症状,包括镇静(从轻度到昏迷不等)和/或including妄(包括意识错乱,迷失方向) ,躁动,焦虑和其他认知障碍)。注意到的其他症状包括锥体外系症状,构音障碍,共济失调,攻击性,头晕,虚弱,高血压和惊厥。在第一个小时内发生事件的可能性最大。大多数病例发生在注射后的前3小时内;但是,该事件已在3小时后发生。在3个小时的观察期之后,医护人员必须在释放前确认患者机敏,定向且没有注射后ir妄/镇静综合征的任何体征和症状。所有患者在离开医疗机构时必须陪伴其到达目的地。在每次注射的剩余时间内,患者不得驾驶或操作重型机械,并应建议患者警惕注射后del妄/镇静综合症的症状,并在需要时能够获得医疗救助。如果怀疑有注射后del妄/镇静综合症,应在能够进行复苏的设施中进行严密的医学监督和监视[见剂量过量( 10 )] 。
在特定人群中的剂量-在开始使用Zyprexa Relprevv治疗之前,应确定口服ZYPREXA的耐受性。对于患有虚弱,易患低血压反应的弱势患者,建议的起始剂量为Zyprexa Relprevv 150 mg / 4 wks,否则其综合因素可能导致奥氮平的代谢减慢(例如,≥65岁的非吸烟女性患者) (年龄),或者对奥氮平对药理学较敏感的人。在指示时,这些患者应谨慎进行剂量递增[参见警告和注意事项( 5.18 ),药物相互作用( 7 )和临床药理学( 12.3 )] 。
Zyprexa Relprevv尚未在18岁以下的受试者中进行过研究[请参阅警告和注意事项( 5.7 )] 。
维持治疗—尽管尚未进行任何对照研究来确定应使用Zyprexa Relprevv治疗多长时间,但已在稳定的精神分裂症患者的24周内证明了疗效。此外,长期服用ZYPREXA可以有效地维持精神分裂症的治疗反应。应该定期对患者进行重新评估,以确定是否需要继续治疗。
从其他抗精神病药物转换—没有系统收集的数据来具体说明如何将精神分裂症患者从其他抗精神病药物转换为Zyprexa Relprevv。
重组和管理Zyprexa Relprevv的说明
仅用于深层肌内注射。不要静脉内或皮下注射。
只要溶液和容器允许,在给药前应目视检查肠胃外药品是否有颗粒物质和变色。
步骤1:准备材料
便利套件包括:
- 小瓶Zyprexa Relprevv粉末
- 3 mL稀释液瓶
- 一个3毫升的注射器与预先连接的19号,1.5英寸(38 MM)注射针-PRO®与针头保护装置针
- 两根19号1.5英寸(38毫米)皮下注射针-带针头保护装置
- —对于肥胖患者,可以使用2英寸(50毫米),19规格或更大的针头(不包括在便利工具包中)进行给药。
Zyprexa Relprevv必须仅使用便利工具包中提供的稀释剂进行悬浮。
建议在重构时使用手套,因为Zyprexa Relprevv可能会刺激皮肤。如果与皮肤接触,请用水冲洗。
有关安全有效地使用Hypodermic Needle-Pro注射器和针头的更多信息,请参见标题为“重组和管理Zyprexa Relprevv的说明”的附加插页。
步骤2:确定复原量
请参考下表以确定稀释到每种粉末强度中要添加到粉末中的稀释剂的量。
重要的是要注意,小瓶中的稀释剂多于重构所需的稀释剂。
| 剂量 | 样品瓶强度 | 稀释剂添加 |
| 150毫克 | 210毫克 | 1.3毫升 |
| 210毫克 | 210毫克 | 1.3毫升 |
| 300毫克 | 300毫克 | 1.8毫升 |
| 405毫克 | 405毫克 | 2.3毫升 |
步骤3:重构Zyprexa Relprevv
在继续进行步骤3之前,请阅读《皮下注射针-Pro使用说明》。不遵守这些说明可能会导致针刺受伤。
轻拍小瓶以松开粉末。
打开预先包装的皮下注射针-Pro注射器和带针头保护装置的针头。
将预定的稀释剂体积(步骤2 )抽入注射器中。
将稀释剂注入粉末瓶中。
稍微向后拉注射器中的柱塞,抽出空气以平衡小瓶中的压力。
从样品瓶中取出针头,将样品瓶直立以防止材料损失。
接合针头安全装置(请参阅完整的《皮下注射针-Pro使用说明》)。
垫硬表面以缓冲冲击力(请参见图1 )。用力地反复轻敲小瓶的表面,直到看不到粉末为止。
 |
| 图1:用力敲打混合。 |
目视检查小瓶是否结块。未悬浮的粉末显示为黄色,干燥的团块,粘在小瓶上。如果大的团块保持附加攻丝可能需要(参见图2 )。
 |
| 图2:检查未悬浮的粉末,并在需要时重复轻拍。 |
剧烈摇动小瓶,直到悬浮液看起来光滑且颜色和质地一致为止。悬浮的产品将为黄色且不透明(请参见图3 )。
 |
| 图3:剧烈摇动小瓶。 |
如果形成泡沫,则让小瓶直立以使泡沫消散。
如果不立即使用产品,则应大力摇晃以重新悬浮。重构的Zyprexa Relprevv在室温下在小瓶中可保持稳定长达24小时。
步骤4:注入Zyprexa Relprevv
在进行3个小时的观察期后,在进行注射之前,请确认会有人陪伴患者。如果无法确认,则不要注射。
请参阅下表确定要注入的最终体积。悬浮液浓度为150 mg / mL Zyprexa Relprevv。
| 剂量 | 最终注射量 |
| 150毫克 | 1毫升 |
| 210毫克 | 1.4毫升 |
| 300毫克 | 2毫升 |
| 405毫克 | 2.7毫升 |
将新的安全针连接到注射器上。
将所需的量缓慢地抽回注射器中。
一些多余的产品将保留在小瓶中。
接合针头安全装置,然后从注射器中取出针头。
要进行给药,请选择带有针头保护装置的19口径1.5英寸(38毫米)皮下注射针-Pro针头。对于肥胖患者,可以使用2英寸(50毫米),19规格或更大的针头(不包括在便利工具包中)。为防止堵塞,必须使用19号或更大号的针头。
注射前,将新的安全针连接到注射器上。从小瓶中取出悬浮液后,应立即注射。
仅用于深层肌内注射。不要静脉内或皮下注射。
选择并准备在臀区域注射的部位。
将针头插入肌肉后,抽吸数秒钟以确保没有血液出现。如果将任何血液吸入注射器,请丢弃注射器和该剂量,并从新的便利工具箱开始。注射应在稳定,连续的压力下进行。
不要按摩注射部位。
接合针头安全装置。
进样后,请妥善处理小瓶,针头和注射器。该小瓶仅供一次性使用。
剂型和优势
Zyprexa Relprevv是仅用于肌内悬浮的粉末。 Zyprexa Relprevv以黄色固体形式存在于玻璃小瓶中,每瓶相当于210、300或405 mg奥氮平。稀释剂是在玻璃小瓶中的澄清,无色至微黄色溶液[请参见说明( 11 )和供应/储存和处理方式( 16 )] 。重新配制的悬浮液将是黄色且不透明的[见剂量和用法( 2.2 )] 。
禁忌症
没有。
警告和注意事项
注射后Deli妄/镇静综合症
在Zyprexa Relprevv的上市前临床研究中,据报道,注射Zyprexa Relprevv的患者出现不良反应,其症状和体征与奥氮平过量有关,特别是镇静(包括昏迷)和/或ir妄[请参阅带框警告和剂量]和管理( 2.1 )] 。这些事件发生在少于0.1%的注射剂中,大约2%的接受注射长达46个月的患者中。在某些情况下,这些事件与血清奥氮平浓度无意中迅速增加至治疗上范围有关。虽然在一些发生这些事件的患者中观察到血清奥氮平浓度迅速增加并超过了预期,但尚无确切的机制将药物无意地引入血流。临床体征和症状包括头晕,神志不清,神志不清,言语不清,步态改变,行走困难,虚弱,躁动,锥体外系症状,高血压,惊厥和意识水平降低,范围从轻度镇静到昏迷。注射后至事件发生的时间范围从注射后不久到注射后超过3小时不等。大多数患者住院,在某些情况下需要一些支持治疗,包括插管。到72小时,所有患者基本康复。每次注射的事件风险相同,因此每位患者的风险是累积的(即,随着注射次数的增加而增加) [请参见剂量过量( 10.1 )] 。
建议医护专业人员每次开处方和使用Zyprexa Relprevv时都要与患者讨论这种潜在风险[请参阅患者咨询信息( 17 )] 。
Zyprexa Relprevv的处方和分发程序
Zyprexa Relprevv仅可通过受限制的分发程序获得(请参阅盒装警告,适应症和用法( 1 )和患者咨询信息( 17 )) 。 Zyprexa Relprevv不得直接分配给患者。为了使患者能够接受治疗,开药者,医疗机构,患者和药房都必须加入Zyprexa Relprevv患者护理计划。要注册,请致电1-877-772-9390。
Zyprexa Relprevv必须在已注册的医疗保健机构(例如医院,诊所,住宅治疗中心或社区医疗保健中心)中进行管理,并且可以随时使用紧急响应服务。每次Zyprexa Relprevv注射后,医护人员必须在医疗机构连续观察患者至少3个小时,并且必须确认患者在注射前出现ir妄/镇静综合征的任何体征和症状之前保持警觉,定向并没有任何症状。被释放。所有患者在离开医疗机构时必须陪伴其到达目的地。在每次注射的剩余时间内,患者不应驾驶或操作重型机械,并应警惕注射后del妄/镇静综合征的症状,并在需要时能够获得医疗救助。如果怀疑有注射后del妄/镇静综合症,应在能够进行复苏的设施中进行严密的医学监督和监视[见剂量过量( 10 )] 。如果在注射后发生ir妄/镇静综合征时需要肠胃外苯二氮卓类药物进行患者管理,建议仔细评估过度镇静和心肺抑郁的临床状况。
老年痴呆症相关精神病患者
死亡率增加
接受抗精神病药治疗的老年痴呆症相关精神病患者的死亡风险增加。 Zyprexa Relprevv未获准用于治疗与痴呆相关的精神病患者[请参阅盒装警告,在特定人群中使用( 8.5 )和患者咨询信息( 17 )] 。
在老年痴呆症相关精神病患者的安慰剂对照口服奥氮平临床试验中,奥氮平治疗的患者的死亡发生率明显高于安慰剂治疗的患者(分别为3.5%和1.5%)。
脑血管不良事件(CVAE),包括中风
在老年痴呆症相关精神病患者的口服奥氮平试验中,报告了包括死亡在内的脑血管不良事件(例如中风,短暂性脑缺血发作)。在安慰剂对照试验中,口服奥氮平治疗的患者脑血管不良事件的发生率比安慰剂治疗的患者高得多。 Zyprexa Relprevv未被批准用于治疗与痴呆相关的精神病患者[请参阅带框警告和患者咨询信息( 17 )] 。
自杀
精神分裂症固有的自杀企图,高危患者应密切监督药物治疗。
抗精神病药恶性综合症(NMS)
据报道,与包括奥氮平在内的抗精神病药物的给药有关,一种潜在的致命症状复合物有时被称为神经安定性恶性综合症(NMS)。 NMS的临床表现为高热,肌肉僵硬,精神状态改变和自主神经不稳定(脉搏或血压异常,心动过速,发汗和心律不齐)。其他体征可能包括肌酐磷酸激酶升高,肌红蛋白尿(横纹肌溶解)和急性肾衰竭。
该综合征患者的诊断评估很复杂。在做出诊断时,重要的是要排除临床表现包括严重内科疾病(例如,肺炎,全身感染等)和未经治疗或未得到充分治疗的锥体外系体征和症状(EPS)的病例。鉴别诊断中的其他重要考虑因素包括中枢抗胆碱能毒性,中暑,药物热和原发性中枢神经系统病理。
NMS的管理应包括:1)立即停用抗精神病药和其他对并发治疗非必需的药物; 2)强化对症治疗和医学监测; 3)对任何伴随着严重的医学问题的治疗,只要有具体的治疗方法即可。关于NMS的具体药物治疗方案尚无普遍共识。
如果患者从NMS恢复后需要抗精神病药物治疗,应谨慎考虑可能重新引入药物治疗的情况,并在开始用Zyprexa Relprevv治疗之前确定口服奥氮平的耐受性[参见剂量和给药方法( 2.1 )] 。由于已经报告了NMS的复发,因此应仔细监测患者[参见患者咨询信息( 17 )] 。
嗜酸性粒细胞增多和全身症状的药物反应(DRESS)
据报道,与奥氮平接触会引起与嗜酸性粒细胞增多和全身症状的药物反应(DRESS)。 DRESS可能会出现皮肤反应(例如皮疹或剥脱性皮炎),嗜酸性粒细胞增多,发烧和/或淋巴结病,并伴有全身并发症,例如肝炎,肾炎,肺炎,心肌炎和/或心包炎。着装有时是致命的。如果怀疑有DRESS,请中止Zyprexa Relprevv [请参阅患者咨询信息( 17 )] 。
代谢变化
非典型抗精神病药已与代谢变化相关,包括高血糖,血脂异常和体重增加。代谢变化可能与心血管/脑血管风险增加有关。奥氮平的具体代谢特征如下。
高血糖和糖尿病
当确诊为糖尿病或血糖水平升高(空腹100-126 mg / dL,非空腹140-200 mg / dL)的患者开具奥氮平处方时,医疗保健提供者应考虑风险和收益。服用奥氮平的患者应定期进行监测,以防血糖控制恶化。开始使用奥氮平治疗的患者应在治疗开始时以及治疗期间定期进行空腹血糖测试。应监测任何接受非典型抗精神病药治疗的患者的高血糖症状,包括烦躁,多尿,多食和无力。在非典型抗精神病药治疗期间出现高血糖症状的患者应接受空腹血糖测试。在某些情况下,停用非典型抗精神病药后,高血糖症已缓解;然而,尽管中止了可疑药物的治疗,有些患者仍需要继续抗糖尿病治疗[见患者咨询信息( 17 )] 。
据报道,在非典型抗精神病药物包括奥氮平治疗的患者中,高血糖症在某些情况下是极端的,并与酮症酸中毒或高渗性昏迷或死亡有关。非典型抗精神病药使用与葡萄糖异常之间的关系的评估由于患有精神分裂症患者的糖尿病背景风险增加以及普通人群中糖尿病发生率增加的可能性而变得复杂。流行病学研究表明,使用非典型抗精神病药治疗的患者出现与治疗相关的高血糖相关不良反应的风险增加。尽管相对风险估计值不一致,但非典型抗精神病药与血糖水平升高之间的相关性似乎是连续的,奥氮平似乎比其他一些非典型抗精神病药具有更大的相关性。
临床干预措施(CATIE)的抗精神病临床试验的第一阶段中,已观察到奥氮平治疗的患者(中位暴露时间为9.2个月)的平均血糖升高。血清葡萄糖(空腹和非空腹样品)从基线到平均两个最高血清浓度的平均增加为15.0 mg / dL。
在对健康志愿者的研究中,接受奥氮平(N = 22)3周的受试者的空腹血糖水平较基线水平平均升高2.3 mg / dL。与基线相比,安慰剂治疗的受试者(N = 19)的空腹血糖平均增加了0.34 mg / dL。
成人奥氮平单药治疗—在对5项安慰剂对照的成人奥氮平单药治疗研究中进行分析,中位治疗时间约为3周,与安慰剂相比,奥氮平与空腹血糖水平的平均变化较大(2.76 mg / dL对0.17 mg / dL)。基线时有葡萄糖失调迹象的患者(诊断为糖尿病或相关不良反应的患者,接受抗糖尿病药治疗的患者,基线随机葡萄糖水平≥200mg /的患者,奥氮平和安慰剂之间的平均变化差异更大) dL和/或基线空腹血糖水平≥126mg / dL)。
与安慰剂治疗的受试者(中位数暴露17天)相比,奥氮平治疗的患者的平均HbA 1c较基线升高0.04%(中位暴露21天),而基线时平均HbA 1c降低0.06%。
在对8项安慰剂对照研究(中位治疗暴露4-5周)的分析中,奥氮平治疗的受试者(N = 855)有6.1%出现治疗性糖尿,而安慰剂治疗的受试者有2.8%(N = 599) 。表2显示了成人奥氮平单药研究的空腹血糖水平的短期和长期变化。
a不适用。 | ||||||
| 长达12周的曝光 | 至少接触48周 | |||||
| 实验室分析物 | 类别变更(至少一次) 从基线 | 治疗臂 | ñ | 耐心 | ñ | 耐心 |
| 正常到高 | 奥氮平 | 543 | 2.2% | 345 | 12.8% | |
| 禁食 | (<100 mg / dL至≥126mg / dL) | 安慰剂 | 293 | 3.4% | NA一 | NA一 |
| 葡萄糖 | 从高到低 | 奥氮平 | 178 | 17.4% | 127 | 26.0% |
| (≥100mg / dL和<126 mg / dL至≥126mg / dL) | 安慰剂 | 96 | 11.5% | NA一 | NA一 | |
暴露至少48周的患者的空腹血糖平均变化为4.2 mg / dL(N = 487)。在对完成了奥氮平治疗9-12个月的患者的分析中,空腹和非空腹血糖水平的平均变化随时间持续增加。
青少年使用奥氮平单药治疗–尚未确定Zyprexa Relprevv在18岁以下患者中的安全性和有效性。
在一项针对青春期患者(13至17岁)的3例安慰剂对照口服奥氮平单药治疗研究的分析中,包括患有精神分裂症(6周)或双相I型障碍(躁狂或混合发作)(3周)的患者,奥氮平与一种与安慰剂相比,空腹血糖水平从基线的平均变化更大(2.68 mg / dL对-2.59 mg / dL)。暴露至少24周的青少年的空腹血糖平均变化为3.1 mg / dL(N = 121)。表3显示了青少年口服奥氮平单药研究的空腹血糖的短期和长期变化。
a不适用。 | ||||||
| 长达12周的曝光 | 至少接触24周 | |||||
| 实验室分析物 | 类别变更(至少一次) 从基线 | 治疗臂 | ñ | 耐心 | ñ | 耐心 |
| 正常到高 | 奥氮平 | 124 | 0% | 108 | 0.9% | |
| 禁食 | (<100 mg / dL至≥126mg / dL) | 安慰剂 | 53 | 1.9% | NA一 | NA一 |
| 葡萄糖 | 从高到低 | 奥氮平 | 14 | 14.3% | 13 | 23.1% |
| (≥100mg / dL和<126 mg / dL至≥126mg / dL) | 安慰剂 | 13 | 0% | NA一 | NA一 | |
血脂异常
使用奥氮平已观察到脂质的不良变化。建议进行临床监测,包括对使用奥氮平的患者进行基线和定期随访脂质评估[请参见患者咨询信息( 17 )] 。
使用奥氮平可观察到临床上甘油三酸酯水平升高,有时甚至很高(> 500 mg / dL)。使用奥氮平还可以观察到总胆固醇的适度平均增加。
成人奥氮平单药治疗—在对5个安慰剂对照的奥氮平单药治疗研究中,治疗持续时间长达12周,分析显示,奥氮平治疗的患者的平均空腹总胆固醇,低密度脂蛋白胆固醇和甘油三酸酯的平均水平较基线增加5.3 mg / dL,3.0 mg / dL和20.8 mg / dL,与之相比,安慰剂治疗的患者的平均空腹总胆固醇,LDL胆固醇和甘油三酸酯的下降分别为6.1 mg / dL,4.3 mg / dL和10.7 mg / dL。对于空腹HDL胆固醇,在奥氮平治疗的患者和安慰剂治疗的患者之间未观察到临床上有意义的差异。在基线时没有脂质失调迹象的患者中,空腹血脂值(总胆固醇,LDL胆固醇和甘油三酸酯)的平均增加更大,其中脂质失调被定义为诊断为血脂异常或相关不良反应的患者,接受降脂剂治疗的患者,或基线血脂水平高的患者。
在长期研究(至少48周)中,患者的平均空腹总胆固醇,LDL胆固醇和甘油三酸酯的平均水平较基线分别增加了5.6 mg / dL,2.5 mg / dL和18.7 mg / dL,空腹HDL胆固醇降低0.16 mg / dL。在对完成12个月治疗的患者进行的分析中,约4-6个月后,平均非空腹总胆固醇没有进一步增加。
在长期研究中,总胆固醇,LDL胆固醇或甘油三酸酯的变化(至少一次)从正常或临界水平变为高水平,或HDL胆固醇的变化从正常或临界水平变为低水平的患者比例更高(至少48个)周)与短期研究相比。表4显示了空腹血脂值的分类变化。
a不适用。 | ||||||
| 长达12周的曝光 | 至少接触48周 | |||||
| 实验室分析物 | 类别变更(至少一次) 从基线 | 治疗臂 | ñ | 耐心 | ñ | 耐心 |
| 增加≥50mg / dL | 奥氮平 | 745 | 39.6% | 487 | 61.4% | |
| 安慰剂 | 402 | 26.1% | NA一 | NA一 | ||
| 禁食 | 正常到高 | 奥氮平 | 457 | 9.2% | 293 | 32.4% |
| 甘油三酸酯 | (<150 mg / dL至≥200mg / dL) | 安慰剂 | 251 | 4.4% | NA一 | NA一 |
| 从高到低 | 奥氮平 | 135 | 39.3% | 75 | 70.7% | |
| (≥150mg / dL和<200 mg / dL至≥200mg / dL) | 安慰剂 | 65岁 | 20.0% | NA一 | NA一 | |
| 增加≥40mg / dL | 奥氮平 | 745 | 21.6% | 489 | 32.9% | |
| 安慰剂 | 402 | 9.5% | NA一 | NA一 | ||
| 禁食总计 | 正常到高 | 奥氮平 | 392 | 2.8% | 283 | 14.8% |
| 胆固醇 | (<200 mg / dL至≥240mg / dL) | 安慰剂 | 207 | 2.4% | NA一 | NA一 |
| 从高到低 | 奥氮平 | 222 | 23.0% | 125 | 55.2% | |
| (≥200mg / dL和<240 mg / dL至≥240mg / dL) | 安慰剂 | 112 | 12.5% | NA一 | NA一 | |
| 增加≥30mg / dL | 奥氮平 | 536 | 23.7% | 483 | 39.8% | |
| 安慰剂 | 304 | 14.1% | NA一 | NA一 | ||
| 空腹低密度脂蛋白 | 正常到高 | 奥氮平 | 154 | 0% | 123 | 7.3% |
| 胆固醇 | (<100 mg / dL至≥160mg / dL) | 安慰剂 | 82 | 1.2% | NA一 | NA一 |
| 从高到低 | 奥氮平 | 302 | 10.6% | 284 | 31.0% | |
| (≥100mg / dL和<160 mg / dL至≥160mg / dL) | 安慰剂 | 173 | 8.1% | NA一 | NA一 | |
在临床抗精神病药物干预有效性试验(CATIE)的第一阶段中,在中位暴露9.2个月内,服用奥氮平的患者甘油三酸酯的平均增加量为40.5 mg / dL。在CATIE的第1阶段中,总胆固醇的平均增加量为9.4 mg / dL。
已经观察到关于禁食甘油三酸酯增加的剂量组差异。在一项用Zyprexa Relprevv进行的为期24周的随机,双盲,固定剂量研究中,已观察到空腹甘油三酯剂量组之间的统计学差异显着。在试验期间的任何时间,空腹甘油三酯从正常水平变化到高水平的发生率均表明最高剂量组(300 mg / 2周,24.5%[13/53])与较低剂量组(150 mg / 2)之间存在显着差异周,6.5%[4/62]; 405 mg / 4周,9.8%[13/133])。
已知共有594种药物与Zyprexa Relprevv(奥氮平)相互作用。
- 43种主要药物相互作用
- 541种中等程度的药物相互作用
- 10种次要药物相互作用
检查互动
最常检查的互动
查看Zyprexa Relprevv(奥氮平)与以下药物的相互作用报告。
- Abilify(阿立哌唑)
- Adderall(苯丙胺/右旋苯丙胺)
- AndroGel(睾丸激素)
- Chantix(瓦伦尼克林)
- 氯氮唑(氯氮平)
- mb(度洛西汀)
- Depakote(双丙戊酸钠)
- 立普妥(阿托伐他汀)
- Prilosec(奥美拉唑)
- Prolia(denosumab)
- 普萘洛尔
- Sabril(vigabatrin)
- Suboxone(丁丙诺啡/纳洛酮)
- 睾丸激素(睾丸激素)
- 沙洛米德(沙利度胺)
- Topamax(托吡酯)
- 曲马多
- 曲唑酮
- Truvada(恩曲他滨/替诺福韦)
- 威布霉素(强力霉素)
Zyprexa Relprevv(奥氮平)酒精/食物相互作用
Zyprexa Relprevv(olanzapine)与酒精/食物有4种相互作用
Zyprexa Relprevv(奥氮平)疾病相互作用
与Zyprexa Relprevv(奥氮平)有19种疾病相互作用,包括:
- 痴呆
- 急性酒精中毒
- 中枢神经系统抑郁症
- 网管系统
- 迟发性运动障碍
- 萧条
- 抱负
- 发作
- 血液学异常
- 高血糖/糖尿病
- 低血压
- 脂质改变
- 体重增加
- 抗胆碱作用
- 高泌乳素血症
- 肝病
- 帕金森症
- ALT升高
- 北大
药物相互作用分类
| 具有高度临床意义。避免组合;互动的风险大于收益。 | |
| 具有中等临床意义。通常避免组合;仅在特殊情况下使用。 | |
| 临床意义不大。降低风险;评估风险并考虑使用替代药物,采取措施规避相互作用风险和/或制定监测计划。 | |
| 没有可用的互动信息。 |
药物状态
- 可用性 仅处方
- 怀孕和哺乳 现有风险数据
- CSA时间表* 不是管制药物
- 审批历史 FDA的药物史
美国日本医生

Heather Benjamin MD

Heather Benjamin MD

Suzanne Reitz MD

Heather Miske DO

Heather Miske DO

渡邊剛

宮崎総一郎 中部大学特聘教授

百村伸一 教授

村上和成 教授

中山秀章 教授
临床试验
- 用于用一线osimertinib(LAT-Flosi)处理的少殖民NSCLC的LAT
- 针对口腔癌患者的个性化幸存者护理计划 - 对身体心理功能和重返工作
- 使用Tritanium®C前颈笼进行一或两层的前颈椎切除术和融合(Stryker)
- 躯干稳定练习对脑瘫生活质量和沟通的影响
- 食管测量和CT扫描测量的比较
- 可口的利多卡因凝胶对接受胃肠道上镜检查的患者的GAG反射作用
- 口咽运动和中风后阻塞性睡眠呼吸暂停
- 幽门螺杆菌幽门螺杆菌消除了不同的二氮四核治疗疗法
- 对青少年和成年人中的lanadelumab的研究,以防止与正常C1抑制剂(C1-INH)对非高 - 抗敏力血管性水肿的急性攻击
- TY-9591在晚期非小细胞肺癌(NSCLC)患者EGFR阳性突变患者中的研究