获取国外肉毒杆菌药品价格,使用等信息,最快 24 小时回馈
肉毒杆菌
什么是肉毒杆菌毒素?
肉毒杆菌毒素(onabotulinumtoxinA)是由引起肉毒杆菌中毒的细菌制成的。肉毒杆菌毒素会阻止肌肉中的神经活动。
肉毒杆菌毒素在成人中用于治疗宫颈肌张力障碍(头部位置异常和颈部疼痛)。
肉毒杆菌素还用于治疗2岁以上成人和儿童手臂,手,腿和脚的肌肉僵硬(痉挛)。
肉毒杆菌毒素用于治疗至少12岁的成年人和儿童的神经疾病引起的某些眼部肌肉疾病。这包括眼睑不受控制的眨眼或痉挛,以及眼睛未指向同一方向的情况(斜视)。
肉毒杆菌毒素在成人中用于治疗膀胱过度活动症和尿失禁(尿液渗漏),而其他药物则无济于事。肉毒杆菌毒素可用于治疗由神经疾病(如脊髓损伤或多发性硬化症)引起的失禁。
肉毒杆菌毒素在成人中用于预防每月超过15天且持续4小时或更长时间的慢性偏头痛。肉毒杆菌毒素不应该用于治疗普通的紧张性头痛。
肉毒杆菌毒素也用于治疗成年人的严重腋下出汗(多汗症)。
肉毒杆菌化妆品用于暂时减轻成人面部皱纹的出现。
重要信息
如果在将要注射药物的区域感染,则不应使用肉毒杆菌毒素。如果您当前患有膀胱感染或无法排尿(除非您通常使用导管),则不应使用这种药物来治疗膀胱过度活动或尿失禁。
肉毒杆菌毒素所含的肉毒杆菌毒素可以扩散到注射部位以外的其他身体部位。这可能会导致严重的威胁生命的副作用。
如果声音嘶哑,眼睑下垂,视力问题,严重的眼睛刺激感,严重的肌肉无力,膀胱失去控制或呼吸,说话或吞咽困难,请立即致电医生。
在服药之前
如果您对肉毒杆菌毒素过敏,或者患有以下疾病,则不应使用肉毒杆菌毒素治疗:
注射药物区域的感染;要么
(用于膀胱过度活动症和大小便失禁),如果您当前患有膀胱感染或无法排尿并且不定期使用导管。
为确保肉毒杆菌毒素对您安全,请告诉您的医生是否曾经:
其他肉毒杆菌毒素注射,例如Dysport或Myobloc(尤其是最近4个月内);
肌萎缩性侧索硬化症(ALS,或“卢格氏病”);
重症肌无力;
Lambert-Eaton综合征;
事先使用肉毒杆菌毒素后的副作用;
呼吸系统疾病,例如哮喘或肺气肿;
吞咽问题;
面部肌肉无力(眼睑下垂,前额无力,抬起眉毛有麻烦);
脸部正常外观的变化;
出血问题;要么
手术(尤其是脸部手术)。
肉毒杆菌毒素是由捐赠的人血浆制成的,可能含有病毒或其他传染因子。对捐赠的血浆进行了测试和处理,以减少污染的风险,但是仍然存在传播疾病的可能性很小。向您的医生询问任何可能的风险。
目前尚不清楚这种药物是否会伤害未出生的婴儿。告诉医生您是否怀孕或计划怀孕。
使用这种药物母乳喂养可能并不安全。向您的医生询问任何风险。
肉毒杆菌毒素如何服用?
肉毒杆菌毒素注射仅应由训练有素的医学专业人员进行,即使用于美容目的。
这种药物是由医护人员注射到肌肉中的。肉毒杆菌毒素注射间隔至少3个月。
视情况而定,一次可将肉毒杆菌毒素注射到一个以上的区域。
在接受针对眼部肌肉疾病的注射时,您可能需要使用滴眼剂,药膏,特殊的隐形眼镜或其他保护眼睛表面的装置。遵循医生的指示。
如果您因出汗过多而需要治疗,请在注射前约24小时刮除腋下。接受注射之前或之后的24小时内,请勿使用止汗剂或除臭剂。注射前30分钟内避免运动和热食或饮料。
注射后最多可能需要2周的时间,颈部肌肉痉挛症状才会开始改善。您可能会在6周后注意到最大的改善。
注射后可能只需要1-3天,眼肌痉挛症状就会开始改善。您可能会在2到6周后注意到最大的改善。
肉毒杆菌毒素注射的作用是暂时的。您的症状可能会在3个月内完全恢复。重复注射后,症状恢复所需的时间可能会越来越少,尤其是当您的身体对肉毒杆菌毒素产生抗体时。
请勿一次从多个医务人员处寻求肉毒杆菌毒素注射。如果您转用医疗保健提供者,请告诉您的新提供者距您上次注射肉毒杆菌毒素已有多长时间了。
比处方更频繁地使用这种药物不会使其更有效,并可能导致严重的副作用。
如果我错过剂量怎么办?
由于肉毒杆菌毒素具有暂时性作用,并且间隔很宽,因此不大可能不会造成伤害。
如果我服药过量怎么办?
寻求紧急医疗护理或致电1-800-222-1222,拨打毒药帮助热线。
服药过量的症状可能不会立即出现,但可能包括肌肉无力,吞咽困难以及呼吸弱或浅。
收到肉毒杆菌毒素后应该避免什么?
肉毒杆菌毒素可能会损害您的视力或深度感知。除非您知道这种药会如何影响您,否则请避免驾驶或危险活动。
避免在注射后过快地恢复正常的身体活动。
肉毒杆菌毒素的副作用
如果您对肉毒杆菌有过敏反应迹象,请寻求紧急医疗救助:荨麻疹,瘙痒,喘息,呼吸困难;感觉自己可能会昏倒;脸,嘴唇,舌头或喉咙肿胀。
肉毒杆菌毒素所含的肉毒杆菌毒素可以扩散到注射部位以外的其他身体部位。这在一些接受肉毒杆菌毒素注射的人中,甚至出于美容目的,已经造成严重的威胁生命的副作用。
如果您有以下任何一种副作用,请立即致电您的医生(注射后长达数小时或数周):
异常或严重的肌肉无力(尤其是在未注射药物的身体部位);
呼吸,说话或吞咽困难;
失去膀胱控制;
声音嘶哑,眼皮下垂;
视力变化,眼睛疼痛,严重干燥或眼睛不适(您的眼睛可能对光线更敏感);
胸痛或压力,疼痛蔓延到您的下巴或肩膀,不规则的心跳;
小便时疼痛或烧灼,排空膀胱有麻烦;
喉咙痛,咳嗽,胸闷,呼吸急促;要么
眼睑肿胀,结s或流眼,视力问题。
常见的肉毒杆菌毒素副作用可能包括:
注射药物附近的肌肉无力;
治疗后数月吞咽困难;
肌肉僵硬,颈部疼痛,手臂或腿部疼痛;
视力模糊,眼睑浮肿,眼睛干燥,眉毛下垂;
口干;
头痛,疲倦;
腋下以外区域的出汗增加;要么
注射部位有瘀伤,出血,疼痛,发红或肿胀。
这不是副作用的完整列表,并且可能会发生其他副作用。打电话给您的医生,征求有关副作用的医疗建议。您可以通过1-800-FDA-1088向FDA报告副作用。
还有哪些其他药物会影响肉毒杆菌毒素?
告诉您的医生您所有其他药物的信息,尤其是:
肌肉放松剂;
感冒或过敏药;
睡眠药
可注射的抗生素;要么
血液稀释剂-华法林,香豆素,扬托芬。
此列表不完整。其他药物可能会影响肉毒杆菌毒素,包括处方药和非处方药,维生素和草药产品。此处未列出所有可能的药物相互作用。
版权所有1996-2020 Cerner Multum,Inc.版本:7.01。
注意:本文档包含有关onabotulinumtoxinA的副作用信息。此页面上列出的某些剂型可能不适用于Botox品牌。
综上所述
肉毒杆菌毒素的常见副作用包括:抗体发展。有关不良影响的完整列表,请参见下文。
对于消费者
适用于肉毒杆菌毒素A:溶液粉
警告
注射途径(溶液粉)
毒素作用的远距离传播-肉毒杆菌毒素A和所有肉毒杆菌毒素产品的作用可能会从注射区域扩散,产生与肉毒杆菌毒素作用一致的症状。注射后数小时至数周已报告了这些症状。吞咽和呼吸困难可能会危及生命,并且已有死亡报告。在接受痉挛治疗的儿童中,症状的风险可能最大,但成人中也可能出现症状,尤其是那些患有潜在疾病的患者,这些疾病可能使他们容易出现这些症状。
需要立即就医的副作用
除其需要的作用外,肉毒杆菌毒素A(肉毒杆菌毒素中包含的活性成分)可能会引起一些不良作用。尽管并非所有这些副作用都可能发生,但如果确实发生了,则可能需要医疗护理。
服用肉毒杆菌毒素A时,如果有以下任何副作用,请立即与医生或护士联系:
比较普遍;普遍上
- 吞咽困难
罕见
- 呼吸或说话困难
- 肌肉无力
更常见-眼睑痉挛
- 眼睛干燥
- 无法完全闭上眼睑
较常见-上肢痉挛
- 身体酸痛或疼痛
- 发冷
- 咳嗽
- 耳部充血
- 发热
- 头痛
- 失去声音
- 流鼻涕或鼻塞
- 打喷嚏
- 咽喉痛
- 异常疲倦或虚弱
较常见-因膀胱过度活动引起的尿失禁
- 膀胱疼痛
- 血尿或浑浊
- 排尿困难,灼热或疼痛
- 尿频
- 下背部或侧面疼痛
不常见-眼睑痉挛
- 减少闪烁
- 刺激眼睛的角膜(有色部分)
- 从眼睑边缘向外或向内转动
不太常见-用于额头线
- 眉毛和上眼睑下垂
较不常见-用于睑缘线
- 上眼睑下垂
- 面部疼痛
- 肌肉无力
- 面部部分或轻微麻痹
较不常见-用于can侧线
- 眼睑肿胀
较不常见-上肢痉挛
- 咳嗽产生粘液
- 呼吸困难
- 肌肉无力
- 恶心
- 癫痫发作
- 胸闷
- 弱点
不需要立即就医的副作用
肉毒杆菌毒素A可能会发生一些副作用,通常不需要医治。随着身体对药物的适应,这些副作用可能会在治疗期间消失。另外,您的医疗保健专业人员可能会告诉您一些预防或减少这些副作用的方法。
请咨询您的医疗保健专业人员,是否持续存在以下不良反应或令人讨厌,或者是否对这些副作用有任何疑问:
更常见-眼睑痉挛
- 眼睑上有蓝色或紫色的瘀伤
- 上眼睑下垂
- 刺激眼睛或流泪
- 眼睛对光的敏感性
更常见-宫颈肌张力障碍
- 身体酸痛或疼痛
- 发冷
- 咳嗽
- 耳部充血
- 发热
- 头痛
- 失去声音
- 颈部疼痛
- 流鼻涕或鼻塞
- 打喷嚏
- 咽喉痛
- 异常疲倦或虚弱
更常见-慢性偏头痛
- 颈部疼痛
较常见-前额线
- 头痛
更常见-多汗症
- 身体酸痛或疼痛
- 发冷
- 拥塞
- 咳嗽
- 腹泻
- 喉咙干燥或酸痛
- 恐惧
- 发热
- 普遍感到不适或生病
- 头痛
- 拍摄地点流血严重
- 皮肤瘙痒
- 关节痛
- 食欲不振
- 恶心
- 紧张
- 排尿困难或困难
- 流鼻涕
- 发抖
- 出汗
- 脖子上的腺体肿胀
- 睡眠困难
- 吞咽麻烦
- 声音变化
- 呕吐
更常见的斜视
- 上眼睑下垂
- 眼睛向上或向下而不是笔直向前
较常见-上肢痉挛
- 手臂疼痛
不常见-眼睑痉挛
- 皮疹
- 眼睑皮肤肿胀
少见-慢性偏头痛
- 出血,起泡,灼热,寒冷,皮肤变色,压力感,荨麻疹,感染,炎症,瘙痒,肿块,麻木,疼痛,皮疹,发红,疤痕,酸痛,刺痛,肿胀,压痛,刺痛,溃疡或注射部位的温度
- 模糊的视野
- 身体疼痛或疼痛
- 咳嗽产生粘液
- 呼吸困难
- 头晕
- 上眼睑下垂
- 头痛
- 肌肉酸痛
- 紧张
- 敲打耳朵
- 缓慢或快速的心跳
- 胸闷
不太常见-用于额头线
- 皮肤紧致
少见-下肢痉挛
- 背疼
- 身体疼痛或疼痛
- 发冷
- 咳嗽
- 呼吸困难
- 耳部充血
- 发热
- 头痛
- 失去声音
- 打喷嚏
- 咽喉痛
- 鼻塞
- 异常疲倦或虚弱
不太常见-对于斜视
- 难以找到物体的位置
- 双重视野
对于医疗保健专业人员
适用于onabotulinumumxinA:注射剂
一般
较常见的不良反应包括局部疼痛和头痛,否则反应会根据所治疗的病情而变化。注射的肌肉的局部无力代表了预期的药理作用,而附近肌肉的无力也可能由于毒素的传播而发生。 [参考]
胃肠道
肉毒杆菌毒素导致死亡,是严重吞咽困难的并发症。在宫颈肌张力障碍患者中,有19%的患者出现吞咽困难。据报道大多数吞咽困难为轻度或中度,但是在这些病例中约有20%伴有呼吸困难。 [参考]
非常常见(10%或更多):吞咽困难(高达19%)
常见(1%至10%):便秘,恶心
罕见(0.1%至1%):口腔干燥
未报告频率:吞咽困难,下巴疼痛
上市后报告:腹痛,腹泻,口干,呕吐,厌食[参考]
呼吸道
与安慰剂组相比,在第1、6、12周时,基线时呼吸功能稳定,降低,呼吸功能降低的上肢痉挛试验患者的事件发生率变化更大(15%或更大或20%或更大的下降)。与安慰剂的这些差异在统计学上不显着,但值得注意。在患有神经肌肉病因性限制性肺疾病和与神经系统疾病相关的逼尿肌过度活动的患者中,与安慰剂相比,治疗患者的强迫肺活量(FVC)降低的发生率达15%或20%或更高。与安慰剂相比,治疗上肢痉挛的患者发生支气管炎的频率更高(3%比1%)。在接受上肢痉挛治疗的肺功能下降的患者中,与安慰剂相比,接受治疗的患者报告上呼吸道感染的频率更高(高达11%比6%)。在接受下肢痉挛治疗的患者中,与安慰剂相比,上呼吸道感染的发生率更高(2%比1%)。在接受上肢痉挛治疗的儿科患者中,上呼吸道感染的发生率比安慰剂高(17%[6单位/ kg]; 10%[3单位/ kg]; 9%[安慰剂])。 [参考]
非常常见(10%或更多):上呼吸道感染
常见(1%至10%):支气管炎,咳嗽,鼻炎,呼吸困难,咽炎,鼻漏,鼻充血
上市后报告:吸入性肺炎,呼吸抑制和/或呼吸衰竭[参考]
神经系统
常见(1%至10%):头痛,偏头痛恶化,面部轻瘫,头晕,高渗,语言障碍,癫痫发作
罕见(0.1%至1%):眩晕
未报告频率:VII神经障碍
上市后报告:臂丛神经病变,面神经麻痹,感觉不足,局部麻木,重症肌无力,感觉异常,周围神经病,神经根病,晕厥[参考]
泌尿生殖
非常常见(10%或更高):尿路感染(高达26%),尿retention留(高达17%)
常见(1%至10%):排尿困难,血尿,尿尿,残余尿量
在患有膀胱过度活动症(OAB)的患者中进行的试验中,在注射内脏肌注射后的最初12周内,最常见的不良反应是尿路感染(UTI; 18%),排尿困难(9%),尿retention留(6%),细菌尿(4%)和剩余尿量(3%)。与没有糖尿病的患者相比,糖尿病患者的尿路感染发生率更高(分别为31%和26%)。与PVR尿量为200 mL或更少的患者相比,注射后经历最大空洞残留(PVR)尿量超过200 mL的患者的UTI发生率增加(44%比23%)。
在逼尿肌过度活跃并伴有神经系统疾病的患者中,尿路感染和尿retention留分别发生在24%和17%。
肌肉骨骼
常见(1%至10%):肢体疼痛,肌肉无力,乏力,乏力,背痛,肌张力亢进,僵硬,跌倒,步态障碍,肌肉痉挛,颈部疼痛,肌肉骨骼僵硬,肌痛
罕见(0.1%至1%):下颚疼痛
上市后报告:失神经/肌肉萎缩,局部肌肉抽搐/不自主肌肉收缩,构音障碍, [参考]
心血管的
肉毒杆菌毒素:
常见(1%至10%):高血压
未报告频率:心律不齐,心肌梗塞(有时致命) [参考]
本地
常见(1%至10%):注射部位疼痛[参考]
眼科
非常常见(10%或更多):眼睑下垂(高达21%)
常见(1%至10%):眼睑下垂,眉毛下垂,浅点状角膜炎,干眼
罕见(0.1%至1%):眼睑浮肿,眼部感染,复视,眼球后出血
非常罕见(小于0.01%):角膜穿孔
未报告的频率:刺激眼睑,注射液,眼角膜炎,畏光,外翻,角膜炎,复视,眼睑注射后眼睑皮肤局部肿胀持续数天,眨眼减少(注射眼轮状肌肉可能导致严重的角膜暴露)持续性上皮缺损
上市后报告:视觉障碍,斜视,视力模糊[参考]
过敏症
据报致命的过敏反应。在这种情况下,使用利多卡因作为稀释剂,因此无法确定其原因。
未报告频率:过敏反应,血清病,荨麻疹,软组织水肿,呼吸困难
其他
常见(1%至10%):疲劳,虚弱,发烧,
未报告频率:局部面部麻痹,晕厥,重症肌无力加重
上市后报告:垂耳,感觉不足,不适,神经根病,耳鸣[参考]
皮肤科
常见(1%至10%):瘙痒,皮肤紧绷
未报告频率:弥漫性皮疹
上市后报告:脱发(包括疟疾),多汗症,瘙痒,皮疹,多形性红斑,牛皮癣性皮炎,牛皮癣性皮疹[参考]
免疫学的
常见(1%至10%):流感综合征,感染
未报告的频率:免疫原性(形成抗A型肉毒杆菌毒素的中和抗体,可能会降低治疗效果) [参考]
血液学
常见(1%至10%):出血[参考]
精神科
常见(1%至10%):焦虑[参考]
参考文献
1.“产品信息。肉毒杆菌化妆品(onabotulinumtoxinA)。”加利福尼亚州欧文市的Allergan Inc.
2.“产品信息。肉毒杆菌毒素(纳肉毒素)。”加利福尼亚州欧文市的Allergan Inc.
某些副作用可能没有报道。您可以将其报告给FDA。
2.3膀胱功能障碍
一般
患者在治疗时不得患有尿路感染(UTI)。除氨基糖苷类药物外,预防性抗生素[见药物相互作用( 7.1 )]应在治疗前1-3天,治疗当日和治疗后1-3天服用,以减少与手术相关的UTI的可能性。
患者应在注射程序前至少3天停止抗血小板治疗。需要对接受抗凝治疗的患者进行适当管理,以减少出血的风险。
进行膀胱镜检查时应格外小心。
膀胱过度活动症
根据局部部位的做法,可以在注射前使用稀释的局麻药在膀胱内滴注有或没有镇静剂。如果进行局部麻醉滴注,则应在注射前排干膀胱并用无菌盐水冲洗。
建议剂量为100单位BOTOX,是最大建议剂量。推荐的稀释度为100单位/ 10 mL,使用无防腐剂的0.9%氯化钠注射液,USP(参见表1)。处置任何未使用的盐水。
通过柔性或刚性膀胱镜将重组的BOTOX(100单位/ 10 mL)注射到逼尿肌中,避免使用三角骨。膀胱应注入足够的生理盐水,以使注射液具有足够的可视性,但应避免过度扩张。
开始注射之前(取决于针头的长度),应在注射针头中充满(灌注)约1 mL的BOTOX,以清除空气。
针头应插入逼尿肌约2毫米,每次注射20次,每次0.5毫升(总体积为10毫升),相隔约1厘米(见图1)。对于最后一次注射,应注射大约1 mL无菌生理盐水,以便将针头中剩余的BOTOX输送到膀胱。注射后,患者应在离开诊所之前表现出排尿能力。注射后应观察患者至少30分钟,直到出现自发性空洞。
当前一剂的临床疗效减弱时(在双盲,安慰剂对照临床研究中,有资格接受BOTOX二次治疗的患者的中位时间为169天[〜24周]),应考虑患者再次注射。从之前的膀胱注射开始早于12周。
图1 :用于治疗膀胱过度活动症和逼尿肌过度活动症A与神经系统疾病相关的Intrutrusor注射剂的注射模式
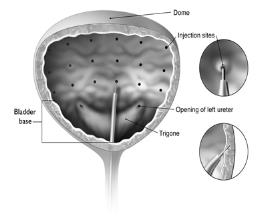
与神经系统疾病相关的逼尿肌过度活动
根据局部部位的实践,可以在注射前使用稀释的局麻药进行膀胱内滴注,有或没有镇静剂,或全身麻醉。如果进行局部麻醉滴注,则应在注射前排干膀胱并用无菌盐水冲洗。
推荐剂量为每次治疗200单位BOTOX,并且不得超过该剂量。
BOTOX的200单位瓶
- 用6 mL不含防腐剂的0.9%氯化钠注射液USP重构200单位的BOTOX小瓶,并轻轻混合。
- 从小瓶中抽取2 mL到三个10 mL注射器中的每一个中。
- 通过向10 mL注射器中的每一个中添加8 mL不含防腐剂的0.9%氯化钠注射液USP,完成重构。这将导致三个10 mL注射器,每个注射器包含10 mL(每个〜67单位),总共200单位的重组BOTOX。
- 重建注射器后立即使用。处理 任何未使用的盐水。
BOTOX的100单位瓶
- 重新配制两个100单位的BOTOX小瓶,每个小瓶均加入6 mL不含防腐剂的0.9%氯化钠注射液USP,并轻轻混合。
- 从每个小瓶中抽取4 mL到两个10 mL注射器中的每个中。将每个小瓶中剩余的2 mL吸到第三个10 mL注射器中,每个注射器中总共吸取4 mL。
- 通过向10 mL注射器中的每一个中添加6 mL不含防腐剂的0.9%氯化钠注射液USP,完成重构。这将导致三个10 mL注射器,每个注射器包含10 mL(每个〜67单位),总共200单位的重组BOTOX。
- 重建注射器后立即使用。处置任何未使用的盐水。
通过柔性或刚性膀胱镜将重建的BOTOX(200单位/ 30 mL)注射到逼尿肌中,避免使用三角骨。膀胱应注入足够的生理盐水,以使注射液具有足够的可视性,但应避免过度扩张。
开始注射之前(取决于针头的长度),应在注射针头中充满(灌注)约1 mL的BOTOX,以清除空气。
针头应插入逼尿肌约2毫米,每次进样30次,每次1 mL(〜6.7单位)(总体积为30 mL),彼此之间的距离应约1 cm(见图1)。对于最后一次注射,应注射约1 mL无菌生理盐水,以便将针头中剩余的BOTOX输送到膀胱。注射后,应排干用于膀胱壁显像的盐水。注射后应至少观察患者30分钟。
当先前注射的临床效果减弱时(双盲,安慰剂对照临床研究中达到重新治疗资格的中位时间为BOTOX的295-337天(42-48周)),应考虑重新注射患者200个单位),但距先前的膀胱注射不早于12周。
2.4慢性偏头痛
推荐的稀释度为200单位/ 4毫升或100单位/ 2毫升,最终浓度为每0.1毫升5单位(见表1)。推荐的治疗慢性偏头痛的剂量为155单位肌肉注射,使用无菌30号0.5英寸针头,每个部位注射0.1毫升(5单位)。注射应按照下图和表2的规定在7个特定的头/颈肌肉区域进行分配。对于颈部肌肉较厚的患者,可能在颈部区域需要一根一英寸的针头。除应在一个部位(中线)注射的前列腺肌外,所有肌肉均应在两侧注射,一半注射部位的数量应放在左侧,头颈部的一半。建议的重新治疗时间表是每12周一次。
图1-4:慢性偏头痛的推荐注射部位(A至G)
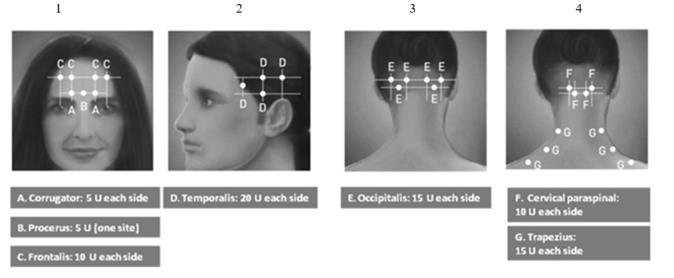
| 头/颈区域 | 推荐剂量(站点数a ) |
| 额叶b | 20个单位,分为4个站点 |
| 瓦楞纸箱b | 10个单位,分为2个站点 |
| Procerus | 1个地点5个单位 |
| 枕叶b | 30个单位,分为6个地点 |
| 颞叶b | 40个单位,分为8个站点 |
| 斜方肌b | 30个单位,分为6个地点 |
| 颈椎旁 肌肉群b | 20个单位,分为4个站点 |
| 总剂量: | 155个单位,分为31个站点 |
a每个IM注射部位= 0.1 mL = 5单位肉毒杆菌毒素
b双边剂量
2.5成人痉挛
一般
应根据个体的大小,所涉肌肉的数量和位置,痉挛的严重程度,局部肌肉无力的存在,患者对先前治疗的反应或BOTOX的不良事件史,针对个人量身定制初始和后续治疗的剂量。
推荐的稀释度为200单位/ 4 mL或100单位/ 2 mL,使用不含防腐剂的0.9%氯化钠注射液,USP(参见表1)。应使用推荐的最低起始剂量,每个部位通常不应超过50个单位。适当尺寸的针(例如25-30号针)可用于浅表肌肉,而较长的22号针可用于较深的肌肉组织。建议使用针状肌电图引导或神经刺激等技术对受累肌肉进行定位。
当前次注射的作用减弱时,可以重复进行BOTOX治疗,但通常不早于前次注射后12周。重新注射时肌肉痉挛的程度和方式可能需要改变BOTOX和注射肌肉的剂量。
成人上肢痉挛
在临床试验中,在给定的治疗疗程中,在选定的肌肉之间分配了75单位至400单位的剂量(参见表3和图2)。
| 肌肉 | 推荐剂量 总剂量(站点数) |
| 肱二头肌 | 100个单位-200个单位,分为4个站点 |
| 腕腕Car | 12.5个单位-1个站点中的50个单位 |
| 屈腕腕 | 12.5个单位-1个站点中的50个单位 |
| 屈指屈肌 | 1个地点30个单位-50个单位 |
| 屈指屈肌 | 1个地点30个单位-50个单位 |
| 内收肌 | 1个地点20个单位 |
| 屈肌腱 | 1个地点20个单位 |
图2:注射部位成人上肢痉挛
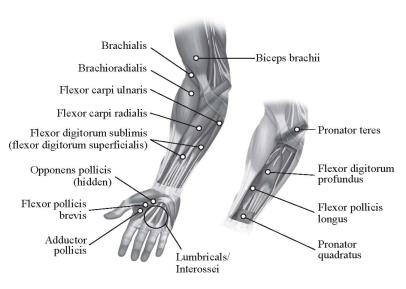
成人下肢痉挛
治疗成人下肢痉挛的推荐剂量为300单位至400单位,分为5块肌肉(腓肠肌,比目鱼肌,胫骨后缘,屈指幻肌和指屈屈肌)(参见表4和图3)。
| MUSCLè | 推荐Ëd 剂量 至T A L dØ年龄 (N个U MBER 的 S I TES) |
| 腓肠肌内侧头 | 75个单元,分为3个站点 |
| 腓肠肌外侧头 | 75个单元,分为3个站点 |
| Soleus | 75个单元,分为3个站点 |
| 胫骨后路 | 75个单元,分为3个站点 |
| 拇长屈肌 | 50个单位,分为2个站点 |
| 趾长屈肌 | 50个单位,分为2个站点 |
数字 3:已经来到Èction站点 对于 成人下肢 水疗式T孵化城
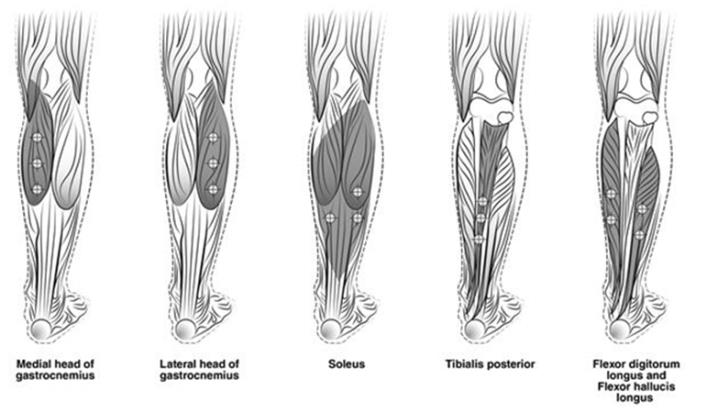
2.6小儿痉挛
一般
建议所涉及的肌肉有技术,如针肌电指导,神经刺激,或超声波的定位。当同时治疗下肢或上下肢时,总剂量不应超过10单位/ kg体重或340单位(以3个月为间隔)中的较低者(请参阅带框警告和警告和注意事项(5.1, 5.6)]。其他一般成人痉挛剂量信息也适用于小儿痉挛患者[参见剂量和给药方法( 2.5 )]。
小儿上肢痉挛
用于治疗小儿上肢痉挛推荐剂量为3个单位/ kg至6单位/公斤受影响的肌肉(参见表5和图4)之间划分。每次治疗中上肢BOTOX的总剂量不应超过6单位/千克或200单位,以较低者为准。
| 肌肉 | 推荐剂量和 网站数量 |
| 肱二头肌 | 1.5单位/千克至3单位/千克,分为4个站点 |
| 臂臂肌 | 1单位/千克至2单位/千克,分为2个站点 |
| 臂臂radi | 0.5单位/千克至1单位/千克分为2个站点 |
| 腕腕Car | 1单位/千克至2单位/千克,分为2个站点 |
| 屈腕腕 | 1单位/千克至2单位/千克,分为2个站点 |
| 屈指屈肌 | 0.5单位/千克至1单位/千克分为2个站点 |
| 屈指屈肌 | 0.5单位/千克至1单位/千克分为2个站点 |
图4:注射部位儿科上肢痉挛
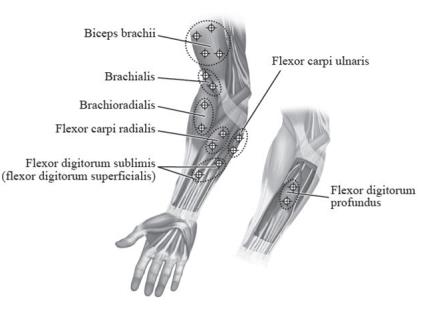
小儿下肢痉挛
用于治疗小儿下肢痉挛推荐剂量为4个单位/ kg至8单位/千克受影响的肌肉(参见表6和图5)之间进行分配。每次治疗下肢BOTOX的总剂量不应超过8单位/千克或300单位,以较低者为准。
表6:BOTOX给药通过肌肉儿科下肢痉挛
| MUSCLè | 推荐Ëd 剂量 总剂量(站点数) |
| 腓肠肌内侧头 | 1单位/千克至2单位/千克,分为2个站点 |
| 腓肠肌外侧头 | 1单位/千克至2单位/千克,分为2个站点 |
| Soleus | 1单位/千克至2单位/千克,分为2个站点 |
| 胫骨后路 | 1单位/千克至2单位/千克,分为2个站点 |
图5:注射部位小儿下肢痉挛
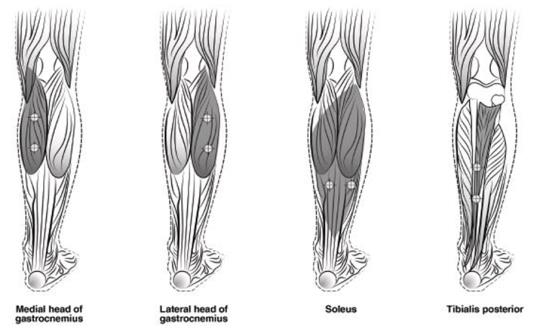
2. 7子宫颈肌张力障碍
一项双盲,安慰剂对照的研究招募了接受和耐受BOTOX注射剂具有悠久历史的患者,并事先进行了个体化剂量调整。在这项研究中,给予患者的平均BOTOX剂量为236单位(第198个单位至300个单位的第25至75个百分位数)。 BOTOX剂量在受影响的肌肉之间分配[请参阅临床研究( 14.6 )]。
应根据患者的头部和颈部位置,疼痛部位,肌肉肥大,患者反应和不良事件史来调整初始患者和序贯治疗的剂量。不事先使用BOTOX的患者的初始剂量应降低剂量,并根据个人反应调整后续剂量。限制注入胸锁乳突肌到100个单位或更小的总剂量可降低吞咽困难的发生[见警告和注意事项(5.1,5.5,5.6)]。
建议的稀释度为200单位/ 2 mL,200单位/ 4 mL,100单位/ 1 mL或100单位/ 2 mL,使用不含防腐剂的0.9%氯化钠注射液USP,具体取决于所需的注射部位的数量和数量。达到治疗目的(见表1)。通常,每个站点应使用适当长度的无菌针头(例如25-30号)来管理不超过50个单位。在肌电图引导下定位受累肌肉可能会有用。
通常在注射后的前两周内开始临床改善,在注射后约六周内可获得最大的临床收益。在双盲,安慰剂对照研究中,观察到大多数受试者在治疗后3个月已恢复到治疗前状态。
2. 8原发性腋窝多汗症
建议剂量为每个腋窝50单位。应使用标准染色技术(例如,Minor的碘-淀粉测试)定义要注射的多晶区域。推荐的稀释度为100单位/ 4 mL,使用无防腐剂的0.9%氯化钠注射液,USP(见表1)。使用无菌的30号针头,以0.1到0.2 mL的等分试样将50单位的BOTOX(2 mL)皮内注射到每个腋下,均匀分布在大约1-2 cm的多个位置(10-15)中。
当先前注射的临床效果减弱时,应重复注射多汗症。
未成年人的碘淀粉测试程序说明:
在测试前的24小时内,患者应刮除腋下并放弃使用非处方除臭剂或止汗剂。测试前,患者应舒适地休息,不要运动或喝热饮料约30分钟。擦干腋下区域,然后立即用碘溶液涂漆。让该区域干燥,然后在该区域轻轻撒上淀粉粉。轻轻吹掉多余的淀粉粉。多晶质区域将在大约10分钟内呈现深蓝黑色。
每个注射部位的作用环直径最大约为2厘米。为了最大程度地减少无效区域,注入位置应均匀分布,如图6所示。
数字 6 :原发性腋窝多汗症的注射方式
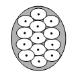
每次注射的深度约为2毫米,与皮肤表面成45°角,斜面朝上,以最大程度地减少泄漏并确保注射保持在皮内。如果在墨水中标记了注入部位,请勿直接通过墨水标记注入BOTOX,以免造成永久性的纹身效果。
2. 9眼睑痉挛
对于眼睑痉挛,使用无菌的27-30号针头在无肌电图引导的情况下注射重建的BOTOX。初始推荐剂量为1.25单位-2.5单位(每个部位的容积为0.05 mL至0.1 mL),分别注入上睑的内侧和外侧睑板球菌眼和下睑的外侧外侧睑板球菌眼。避免在上睑提肌附近注射可能会降低上睑的并发症。避免内侧下眼睑注射,从而减少向下斜肌的扩散,可以减少复视的并发症。在眼睑软组织中容易发生瘀斑。可以在注射后立即在注射部位施加压力来防止这种情况。
为达到1.25单位的推荐稀释度为100单位/ 8 mL; 2.5单位为100单位/ 4毫升(见表1)。
通常,注射的初始效果在三天内即可见到,并在治疗后一到两周达到峰值。每种治疗持续约三个月,此后可以重复该过程。在重复治疗中,如果最初治疗的反应被认为不足,则剂量可增加至两倍,通常定义为持续不超过两个月的作用。但是,每个站点注入5个以上的单位似乎几乎没有收益。如果使用BOTOX进行眼睑痉挛治疗的频率超过每三个月一次,则可能会发现一定的耐受性,而且这种效果很少能持久。
BOTOX治疗眼睑痉挛在30天内的累积剂量不应超过200单位。
2. 10斜视
BOTOX旨在利用从注射针头尖端记录的电活动作为眼内肌肉注射的指导。不应尝试在没有手术暴露或肌电图指导的情况下进行注射。医师应熟悉肌电图检查技术。
为了准备注射BOTOX的眼睛,建议在注射前几分钟服用几滴局部麻醉剂和眼充血剂。
用于治疗斜视的BOTOX量应在每只肌肉0.05-0.15 mL之间。
重组BOTOX的最初列出的剂量[参见剂量和用法( 2.2 )]通常会使注射后的肌肉麻痹,从注射后一到两天开始,并在第一周内强度增加。麻痹持续2-6周,并在相似的时间段内逐渐消退。持续六个月以上的过度校正很少见。由于肌肉对初始剂量的麻痹反应不足,或者由于机械因素(例如较大的偏差或限制),或者由于缺乏稳定双眼运动的双眼运动融合,大约一半的患者将需要后续剂量。
在单位初始d操作系统
使用列出的较低剂量来治疗小偏差。仅将较大剂量用于较大偏差。
- 对于垂直肌肉和少于20棱镜屈光度的水平斜视:任何一块肌肉中的1.25单位至2.5单位。
- 对于20棱镜屈光度到50棱镜屈光度的水平斜视:2.5单位-5单位在任何一块肌肉中。
- 对于持续一个月或更长时间的持续性VI神经麻痹:内直肌中1.25个单位-2.5个单位。
随后d操作系统对于R esidual或R ecurrent小号trabismus
- 建议每次注射后7-14天重新检查患者,以评估该剂量的效果。
- 出现需要随后注射的目标肌肉充分麻痹的患者,应接受与初始剂量相当的剂量。
- 与先前给药的剂量相比,针对目标肌肉不完全麻痹的患者的后续剂量可以增加多达两倍。
- 之前的剂量作用消失之前,不应再进行后续注射,这在被注射的肌肉和邻近肌肉中具有明显的功能。
- 对于任何一只肌肉,单次注射的最大建议剂量为25个单位。
为达到1.25单位的推荐稀释度为100单位/ 8 mL; 2.5单位为100单位/ 4毫升(见表1)。
上市后的报告表明,肉毒杆菌毒素和所有肉毒杆菌毒素产品的作用可能会从注射区域扩散,产生与肉毒杆菌毒素作用一致的症状。这些可能包括乏力,全身性肌无力,复视,上睑下垂,吞咽困难,声音障碍,构音障碍,尿失禁和呼吸困难。注射后数小时至数周已报告了这些症状。吞咽和呼吸困难可能会危及生命,并且已有死亡报告。在接受痉挛治疗的儿童中,症状的风险可能最大,但在进行了痉挛和其他疾病的成人中,也可能出现症状,特别是在那些具有潜在症状的儿童中。在未批准的用途和在批准的适应症,的效果扩散的情况下,已经报道了在剂量与那些用于治疗颈肌张力障碍和痉挛状态和以较低的剂量[秒EE警告和注意事项( 5.1 )]。
1适应症和用途
1.1膀胱功能障碍
膀胱过度活动症
肉毒杆菌 (onabotulinumtoxinA)注射液用于治疗抗胆碱能药物反应不足或不耐受的成年人,患有膀胱过度活动症,并伴有尿急,尿急和尿频。
与神经系统疾病相关的逼尿肌过度活动
肉毒杆菌 指示用于治疗因抗胆碱能药物反应不足或不耐受的成人与神经系统疾病(例如,SCI,MS)相关的逼尿肌过度活动所致的尿失禁。
1.2慢性偏头痛
肉毒杆菌毒素可预防成人偏头痛(每月≥15天,每天持续4小时或更长时间)的头痛。
使用限制
在七项安慰剂对照研究中,尚未确定预防发作性偏头痛(每月头痛14天或更少)的安全性和有效性。
1.3痉挛
肉毒杆菌毒素可用于2岁及2岁以上患者的痉挛治疗。
使用限制
尚未证明肉毒杆菌素可改善上肢功能能力或受固定挛缩影响的关节的活动范围。
1.4宫颈肌张力障碍
肉毒杆菌毒素可用于治疗成人颈肌张力障碍,以减轻与颈肌张力障碍有关的头部异常姿势和颈部疼痛的严重程度。
1.5原发性腋窝多汗症
肉毒杆菌毒素可用于治疗严重的原发性腋窝多汗症,而局部用药不足。
使用限制
尚未确定肉毒杆菌毒素在其他身体部位多汗症的安全性和有效性。接受肉毒杆菌毒素治疗的手掌多汗症和面部多汗症患者可能会分别出现手部肌肉无力和睑裂。应评估患者继发性多汗症的潜在原因(例如甲状腺功能亢进),以避免对多汗症进行对症治疗,而无需诊断和/或治疗基础疾病。
尚未确定肉毒杆菌毒素在18岁以下小儿腋窝多汗症中的安全性和有效性。
1.6眼睑痉挛和斜视
肉毒杆菌毒素可用于治疗与肌张力障碍相关的斜视和眼睑痉挛,包括对12岁以上的患者进行良性眼睑痉挛或VII神经疾病。
2剂量和给药
2.1安全使用说明
注射用肉毒杆菌毒素(onabotulinumtoxinA)的效用单位对所用的制备和测定方法具有特异性。它们不能与肉毒杆菌毒素产品的其他制剂互换使用,因此,肉毒杆菌的生物活性单位不能与通过任何其他特定测定方法评估的任何其他肉毒杆菌毒素产品的单位进行比较或转化为该单位[请参阅警告和注意事项( 5.2 )和说明( 11 )] 。
应遵循适应症的具体剂量和给药建议。开始治疗时,应使用最低推荐剂量。在对成年患者进行一种或多种适应症治疗时,每3个月间隔内最大累积剂量不应超过400单位。在儿科患者中,每3个月间隔一次总剂量不应超过10单位/千克体重或340单位中的较低者[请参阅剂量和用法( 2.6 )] 。
肉毒杆菌毒素的安全有效使用取决于产品的正确储存,正确剂量的选择以及正确的重构和给药技术。斜视,上肢或下肢痉挛的治疗也需要对标准肌电图技术的理解,并且对宫颈肌张力障碍的治疗可能有用。使用肉毒杆菌毒素的医师必须了解涉及区域的相关神经肌肉和结构解剖结构,以及由于先前的外科手术程序和疾病而造成的任何解剖结构变化,尤其是在肺部附近注射时。
如果发生以下情况,请勿使用肉毒杆菌毒素并与Allergan(1-800-890-4345)联系:
•纸箱标签上没有包含带有半透明Allergan银色徽标的完整封条(在纸箱的两端),或者封条上有一个带有对角线的黑色圆圈(即禁止标志),
•样品瓶标签不包含在彩虹色水平线内带有名称“ Allergan”的全息胶片,或
•药瓶标签和纸箱标签上没有美国许可证号1145 [请参阅如何提供/存储和处理( 16 )] 。
2.2制备与稀释技术
注射前,仅用无菌,不含防腐剂的0.9%氯化钠注射液(USP)重构肉毒杆菌毒素的每个真空干燥小瓶。在适当大小的注射器中吸取适量的稀释剂(请参阅表1,或针对与神经系统疾病相关的逼尿肌过度活动的具体说明,请参见第2.3节),然后将稀释剂缓慢注入小瓶中。如果真空没有将稀释剂拉入小瓶,则丢弃小瓶。轻轻混合肉毒杆菌 通过旋转小瓶来稀释。在标签的空白处记录重新配制的日期和时间。复原后24小时内应服用肉毒杆菌毒素。在这段时间内,未使用的重组肉毒杆菌应在冰箱(2°至8°C)中保存24小时,直至使用。肉毒杆菌毒素小瓶仅适用于单剂量。丢弃所有未使用的部分。
| 稀释剂*已添加到100单位瓶中 | 每0.1 mL的最终剂量单位 | 稀释剂*已添加至200单位样品瓶 | 每0.1 mL的最终剂量单位 |
| 1毫升 2毫升 4毫升 8毫升 10毫升 | 10伙 5伙 2.5伙 1.25伙 1个单位 | 1毫升 2毫升 4毫升 8毫升 10毫升 | 20伙 10伙 5伙 2.5单位 2伙 |
*不含防腐剂的0.9%氯化钠注射液,仅USP
**关于与神经系统疾病稀释相关的逼尿肌过度活动,请参见第2.3节
注意:这些稀释度是针对0.1 mL进样量计算的。通过施用较小或较大的注射体积(从0.05 mL(剂量减少50%)到0.15 mL(剂量增加50%)),也可以减少或增加肉毒杆菌毒素的剂量。
肉毒杆菌毒素的注射是通过将适当重构的毒素的量稍微大于预期剂量的量吸入适当大小的无菌注射器中来制备的。注射器针筒中的气泡被排出,并将注射器连接到适当的注射针上。应确认针头是否通畅。每次都应使用新的无菌针头和注射器进入小瓶以取出肉毒杆菌毒素。
重组肉毒杆菌应该透明,无色且无颗粒物质。给药前以及溶液和容器允许的情况下,应目视检查肠胃外药品是否有颗粒物和变色。
2.3膀胱功能障碍
一般
患者在治疗时不得患有尿路感染(UTI)。除氨基糖苷类药物外,预防性抗生素[见药物相互作用( 7.1 )]应在治疗前1-3天,治疗当日和治疗后1-3天服用,以减少与手术相关的UTI的可能性。
患者应在注射程序前至少3天停止抗血小板治疗。需要对接受抗凝治疗的患者进行适当管理,以减少出血的风险。
进行膀胱镜检查时应格外小心。
膀胱过度活动症
根据局部部位的做法,可以在注射前使用稀释的局麻药在膀胱内滴注有或没有镇静剂。如果进行局部麻醉滴注,则应在注射前排干膀胱并用无菌盐水冲洗。
推荐剂量是100单位肉毒杆菌素,是最大推荐剂量。推荐的稀释度为100单位/ 10 mL,使用无防腐剂的0.9%氯化钠注射液,USP(参见表1)。处置任何未使用的盐水。
通过柔性或刚性膀胱镜将重构的肉毒杆菌毒素(100单位/ 10 mL)注射到逼尿肌中,避免使用三角骨。膀胱应注入足够的生理盐水,以使注射液具有足够的可视性,但应避免过度扩张。
在开始注射之前(取决于针头的长度),应在注射针头中充满(灌注)约1 mL的肉毒杆菌素,以清除空气。
针头应插入逼尿肌约2毫米,每次注射20次,每次0.5毫升(总体积为10毫升),相隔约1厘米(见图1)。对于最后一次注射,应注射约1 mL无菌生理盐水,以便将针头中剩余的肉毒杆菌素递送至膀胱。注射后,患者应在离开诊所之前表现出排尿能力。注射后应观察患者至少30分钟,直到出现自发性空洞。
当前次注射的临床效果减弱时(在双盲,安慰剂对照临床研究中,有资格接受肉毒杆菌第二次治疗的患者的中位时间为169天[〜24周]),应考虑患者再次注射。从之前的膀胱注射开始早于12周。
图1 :用于治疗膀胱过度活动症和逼尿肌过度活动症A与神经系统疾病相关的Intrutrusor注射剂的注射模式

与神经系统疾病相关的逼尿肌过度活动
根据局部部位的实践,可以在注射前使用稀释的局麻药进行膀胱内滴注,有或没有镇静剂,或全身麻醉。如果进行局部麻醉滴注,则应在注射前排干膀胱并用无菌盐水冲洗。
推荐剂量是每次治疗200单位肉毒杆菌素,不应超过此剂量。
200单位肉毒杆菌素瓶
- 用6 mL不含防腐剂的0.9%氯化钠注射液USP重构200单位的肉毒杆菌素小瓶,并轻轻混合小瓶。
- 从小瓶中抽取2 mL到三个10 mL注射器中的每一个中。
- 通过向10 mL注射器中的每一个中添加8 mL不含防腐剂的0.9%氯化钠注射液USP,完成重构。这将导致三个10 mL注射器,每个注射器包含10 mL(每个〜67单位),总共200单位的重组肉毒杆菌毒素。
- 重建注射器后立即使用。处理 任何未使用的盐水。
100单位肉毒杆菌素瓶
- 重新配制两个100单位的肉毒杆菌素小瓶,每个小瓶分别加入6 mL不含防腐剂的0.9%氯化钠注射液USP,并轻轻混合。
- 从每个小瓶中抽取4 mL到两个10 mL注射器中的每个中。将每个小瓶中剩余的2 mL吸到第三个10 mL注射器中,每个注射器中总共吸取4 mL。
- 通过向10 mL注射器中的每一个中添加6 mL不含防腐剂的0.9%氯化钠注射液USP,完成重构。这将导致三个10 mL注射器,每个注射器包含10 mL(每个〜67单位),总共200单位的重组肉毒杆菌毒素。
- 重建注射器后立即使用。处置任何未使用的盐水。
通过柔性或刚性膀胱镜将重构的肉毒杆菌毒素(200单位/ 30 mL)注射到逼尿肌中,避免使用三角骨。膀胱应注入足够的生理盐水,以使注射液具有足够的可视性,但应避免过度扩张。
在开始注射之前(取决于针头的长度),应在注射针头中充满(灌注)约1 mL的肉毒杆菌素,以清除空气。
针头应插入逼尿肌约2毫米,每次进样30次,每次1 mL(〜6.7单位)(总体积为30 mL),彼此之间的距离应约1 cm(见图1)。对于最后一次注射,应注射约1 mL无菌生理盐水,以便将针头中剩余的肉毒杆菌素递送至膀胱。注射后,应排干用于膀胱壁显像的盐水。注射后应至少观察患者30分钟。
当先前注射的临床效果减弱时(双盲,安慰剂对照临床研究中达到重新治疗资格的中位时间为Botox的295-337天(42-48周)),应考虑重新注射患者200个单位),但距先前的膀胱注射不早于12周。
2.4慢性偏头痛
推荐的稀释度为200单位/ 4毫升或100单位/ 2毫升,最终浓度为每0.1毫升5单位(见表1)。推荐的治疗慢性偏头痛的剂量为155单位肌肉注射,使用无菌30号0.5英寸针头,每个部位注射0.1毫升(5单位)。注射应按照下图和表2的规定在7个特定的头/颈肌肉区域进行分配。对于颈部肌肉较厚的患者,可能在颈部区域需要一根一英寸的针头。除应在一个部位(中线)注射的前列腺肌外,所有肌肉均应在两侧注射,一半注射部位的数量应放在左侧,头颈部的一半。建议的重新治疗时间表是每12周一次。
图1-4:慢性偏头痛的推荐注射部位(A至G)

| 头/颈区域 | 推荐剂量(站点数a ) |
| 额叶b | 20个单位,分为4个站点 |
| 瓦楞纸箱b | 10个单位,分为2个站点 |
| Procerus | 1个地点5个单位 |
| 枕叶b | 30个单位,分为6个地点 |
| 颞叶b | 40个单位,分为8个站点 |
| 斜方肌b | 30个单位,分为6个地点 |
| 颈椎旁 肌肉群b | 20个单位,分为4个站点 |
| 总剂量: | 155个单位,分为31个站点 |
a每个IM注射部位= 0.1 mL = 5单位肉毒杆菌毒素
b双边剂量
2.5成人痉挛
一般
应根据个体的大小,涉及的肌肉的数量和位置,痉挛的严重程度,局部肌肉无力的存在,患者对先前治疗的反应或肉毒杆菌毒素的不良反应史,针对个人量身定制初始和后续治疗的剂量。
推荐的稀释度为200单位/ 4 mL或100单位/ 2 mL,使用不含防腐剂的0.9%氯化钠注射液,USP(参见表1)。应使用推荐的最低起始剂量,每个部位通常不应超过50个单位。适当尺寸的针(例如25-30号针)可用于浅表肌肉,而较长的22号针可用于较深的肌肉组织。建议使用针状肌电图引导或神经刺激等技术对受累肌肉进行定位。
当前次注射的作用减弱时,可以重复进行肉毒杆菌毒素治疗,但通常不早于前次注射后12周。重新注射时肌肉痉挛的程度和方式可能需要改变肉毒杆菌毒素和所注射肌肉的剂量。
成人上肢痉挛
在临床试验中,在给定的治疗疗程中,在选定的肌肉之间分配了75单位至400单位的剂量(参见表3和图2)。
| 肌肉 | 推荐剂量 总剂量(站点数) |
| 肱二头肌 | 100个单位-200个单位,分为4个站点 |
| 腕腕Car | 12.5个单位-1个站点中的50个单位 |
| 屈腕腕 | 12.5个单位-1个站点中的50个单位 |
| 屈指屈肌 | 1个地点30个单位-50个单位 |
| 屈指屈肌 | 1个地点30个单位-50个单位 |
| 内收肌 | 1个地点20个单位 |
| 屈肌腱 | 1个地点20个单位 |
图2:注射部位成人上肢痉挛

成人下肢痉挛
治疗成人下肢痉挛的推荐剂量为300单位至400单位,分为5块肌肉(腓肠肌,比目鱼肌,胫骨后缘,屈指幻肌和指屈屈肌)(参见表4和图3)。
| MUSCLè | 推荐Ëd 剂量 至T A L dØ年龄 (N个U MBER 的 S I TES) |
| 腓肠肌内侧头 | 75个单元,分为3个站点 |
| 腓肠肌外侧头 | 75个单元,分为3个站点 |
| Soleus | 75个单元,分为3个站点 |
| 胫骨后路 | 75个单元,分为3个站点 |
| 拇长屈肌 | 50个单位,分为2个站点 |
| 趾长屈肌 | 50个单位,分为2个站点 |
数字 3:已经来到Èction站点 对于 成人下肢 水疗式T孵化城

2.6小儿痉挛
一般
建议使用针状肌电图引导,神经刺激或超声等技术对受累肌肉进行定位。当同时治疗下肢或上下肢时,总剂量不应超过10单位/ kg体重或340单位(以3个月为间隔)中的较低者(请参阅带框警告和警告和注意事项( 5.1 , 5.6 )]。其他一般成人痉挛剂量信息也适用于小儿痉挛患者[参见剂量和给药方法( 2.5 )]。
儿科上肢痉挛
治疗小儿上肢痉挛的推荐剂量为3单位/千克至6单位/千克,分为受影响的肌肉(见表5和图4)。每次治疗中上肢施用肉毒杆菌毒素的总剂量不应超过6单位/千克或200单位,以较低者为准。
| 肌肉 | 推荐剂量和 网站数量 |
| 肱二头肌 | 1.5单位/千克至3单位/千克,分为4个站点 |
| 臂臂肌 | 1单位/千克至2单位/千克,分为2个站点 |
| 臂臂radi | 0.5单位/千克至1单位/千克分为2个站点 |
| 腕腕Car | 1单位/千克至2单位/千克,分为2个站点 |
| 屈腕腕 | 1单位/千克至2单位/千克,分为2个站点 |
| 屈指屈肌 | 0.5单位/千克至1单位/千克分为2个站点 |
| 屈指屈肌 | 0.5单位/千克至1单位/千克分为2个站点 |
图4:小儿上肢痉挛的注射部位

小儿下肢痉挛
治疗小儿下肢痉挛的推荐剂量为4单位/千克至8单位/千克,分配给受影响的肌肉(参见表6和图5)。下肢每次治疗中施用肉毒杆菌毒素的总剂量不应超过8单位/千克或300单位,以较低者为准。
表6:针对小儿下肢痉挛的肌肉肉毒杆菌毒素剂量
| MUSCLè | 推荐Ëd 剂量 总剂量(站点数) |
| 腓肠肌内侧头 | 1单位/千克至2单位/千克,分为2个站点 |
| 腓肠肌外侧头 | 1单位/千克至2单位/千克,分为2个站点 |
| Soleus | 1单位/千克至2单位/千克,分为2个站点 |
| 胫骨后路 | 1单位/千克至2单位/千克,分为2个站点 |
图5 :小儿下肢痉挛的注射部位

2.7宫颈肌张力障碍
一项双盲,安慰剂对照研究纳入了接受和耐受肉毒杆菌毒素注射有悠久历史的患者,并事先进行了个体化剂量调整。在这项研究中,向患者施用的肉毒杆菌毒素平均剂量为236单位(第198单位至300单位的第25至75个百分位数)。肉毒杆菌毒素剂量在受影响的肌肉之间分配[见临床研究( 14.6 )]。
应根据患者的头部和颈部位置,疼痛部位,肌肉肥大,患者反应和不良事件史来调整初始患者和序贯治疗的剂量。对于没有事先使用肉毒杆菌毒素的患者,初始剂量应较低,随后根据个人反应调整剂量。限制注入胸锁乳突肌到100个单位或更小的总剂量可降低吞咽困难的发生[见警告和注意事项( 5.1 , 5.5 , 5.6 )]。
建议的稀释度为200单位/ 2 mL,200单位/ 4 mL,100单位/ 1 mL或100单位/ 2 mL,使用不含防腐剂的0.9%氯化钠注射液USP,具体取决于所需的注射部位的数量和数量。达到治疗目的(见表1)。通常,每个站点应使用适当长度的无菌针头(例如25-30号)来管理不超过50个单位。在肌电图引导下定位受累肌肉可能会有用。
通常在注射后的前两周内开始临床改善,在注射后约六周内可获得最大的临床收益。在双盲,安慰剂对照研究中,观察到大多数受试者在治疗后3个月已恢复到治疗前状态。
2.8原发性腋窝多汗症
建议剂量为每个腋窝50单位。应使用标准染色技术(例如,Minor的碘-淀粉测试)定义要注射的多晶区域。推荐的稀释度为100单位/ 4 mL,使用无防腐剂的0.9%氯化钠注射液,USP(见表1)。使用无菌的30号针头,以0.1至0.2 mL的等分试样皮内注射50单位的肉毒杆菌毒素到每个腋下,均匀分布在大约1-2 cm的多个部位(10-15)中。
当先前注射的临床效果减弱时,应重复注射多汗症。
未成年人的碘淀粉测试程序说明:
在测试前的24小时内,患者应刮除腋下并放弃使用非处方除臭剂或止汗剂。测试前,患者应舒适地休息,不要运动或喝热饮料约30分钟。擦干腋下区域,然后立即用碘溶液涂漆。让该区域干燥,然后在该区域轻轻撒上淀粉粉。轻轻吹掉多余的淀粉粉。多晶质区域将在大约10分钟内呈现深蓝黑色。
每个注射部位的作用环直径最大约为2厘米。为了最大程度地减少无效区域,注入位置应均匀分布,如图6所示。
数字 6 :原发性腋窝多汗症的注射方式

每次注射的深度约为2毫米,与皮肤表面成45°角,斜面朝上,以最大程度地减少泄漏并确保注射保持在皮内。如果在墨水上标记了注射部位,请勿直接通过墨水标记注射肉毒杆菌毒素,以避免永久性的纹身效果。
2.9眼睑痉挛
对于眼睑痉挛,使用无菌的27-30号针头在没有肌电图引导的情况下注射重组肉毒杆菌毒素。初始推荐剂量为1.25单位-2.5单位(每个部位的容积为0.05 mL至0.1 mL),分别注入上睑的内侧和外侧睑板球菌眼和下睑的外侧外侧睑板球菌眼。避免在上睑提肌附近注射可能会降低上睑的并发症。避免内侧下眼睑注射,从而减少向下斜肌的扩散,可以减少复视的并发症。在眼睑软组织中容易发生瘀斑。可以在注射后立即在注射部位施加压力来防止这种情况。
为达到1.25单位的推荐稀释度为100单位/ 8 mL; 2.5单位为100单位/ 4毫升(见表1)。
通常,注射的初始效果在三天内即可见到,并在治疗后一到两周达到峰值。每种治疗持续约三个月,此后可以重复该过程。在重复治疗中,如果最初治疗的反应被认为不足,则剂量可增加至两倍,通常定义为持续不超过两个月的作用。但是,每个站点注入5个以上的单位似乎几乎没有收益。如果肉毒杆菌毒素治疗眼睑痉挛的频率大于每三个月一次,则可能会发现一定的耐受性,而且这种效果很难持久。
肉毒杆菌毒素在30天内的累积Botox治疗剂量不得超过200单位。
2.10斜视
肉毒杆菌毒素旨在利用从注射针头尖端记录的电活动作为眼内肌肉注射的指导。不应尝试在没有手术暴露或肌电图指导的情况下进行注射。医师应熟悉肌电图检查技术。
为了准备注射肉毒杆菌毒素的眼睛,建议在注射前几分钟给予几滴局部麻醉药和眼充血剂。
用于治疗斜视的肉毒杆菌注射量应在每只肌肉0.05-0.15 mL之间。
重组肉毒杆菌毒素的初始列出剂量[请参见剂量和给药方法( 2.2 )]通常会使注射后的肌肉麻痹,从注射后一到两天开始,并在第一周内强度增加。麻痹持续2-6周,并在相似的时间段内逐渐消退。持续六个月以上的过度校正很少见。由于肌肉对初始剂量的麻痹反应不足,或者由于机械因素(例如较大的偏差或限制),或者由于缺乏稳定双眼运动的双眼运动融合,大约一半的患者将需要后续剂量。
在单位初始d操作系统
使用列出的较低剂量来治疗小偏差。仅将较大剂量用于较大偏差。
- 对于垂直肌肉和少于20棱镜屈光度的水平斜视:任何一块肌肉中的1.25单位至2.5单位。
- 对于20棱镜屈光度到50棱镜屈光度的水平斜视:2.5单位-5单位在任何一块肌肉中。
- 对于持续一个月或更长时间的持续性VI神经麻痹:内直肌中1.25个单位-2.5个单位。
随后d操作系统对于R esidual或R ecurrent小号trabismus
- 建议每次注射后7-14天重新检查患者,以评估该剂量的效果。
- 出现需要随后注射的目标肌肉充分麻痹的患者,应接受与初始剂量相当的剂量。
- 与先前给药的剂量相比,针对目标肌肉不完全麻痹的患者的后续剂量可以增加多达两倍。
- 之前的剂量作用消失之前,不应再进行后续注射,这在被注射的肌肉和邻近肌肉中具有明显的功能。
- 对于任何一只肌肉,单次注射的最大建议剂量为25个单位。
为达到1.25单位的推荐稀释度为100单位/ 8 mL; 2.5单位为100单位/ 4毫升(见表1)。
3剂型和强度
注射:在单剂量小瓶中无菌100单位或200单位真空干燥的粉末,只能在注射前用无菌,无防腐剂的0.9%氯化钠注射液(USP)重构。
4禁忌症
肉毒杆菌素是禁忌的:
•对肉毒杆菌毒素产品或制剂中的任何成分高度敏感的患者[请参阅警告和注意事项( 5.4 )]。
•在建议的注射部位存在感染。
•对于泌尿系统感染的患者,应使用Intrutrusor注射;或患者的尿潴留或排尿后残余(PVR)尿量> 200毫升谁不经常执行清洁间歇自导尿(CIC)[见警告和注意事项( 5.12 , 5.13 )。
5警告和注意事项
5.1毒素效应的传播
肉毒杆菌毒素和其他批准的肉毒杆菌毒素的上市后安全性数据表明,在某些情况下,可以在局部注射部位以外观察到肉毒杆菌毒素的影响。症状与肉毒杆菌毒素的作用机理一致,可能包括乏力,全身性肌肉无力,复视,上睑下垂,吞咽困难,声音障碍,构音障碍,尿失禁和呼吸困难。注射后数小时至数周已报告了这些症状。吞咽和呼吸困难可能会危及生命,并且有报告称死亡与毒素影响有关。对于接受痉挛治疗的儿童,症状的风险可能最大,但对于接受痉挛和其他疾病治疗的成年人,也可能出现症状,尤其是那些患有潜在疾病的患者。在未经批准的用途和经批准的适应症中,已经报道了与毒素作用扩散相一致的症状,其剂量与用于治疗颈肌张力障碍和痉挛的剂量相当或更低。如果发生吞咽,言语或呼吸系统疾病,应建议患者或护理人员立即就医。
没有明确的严重不良事件报告,表明与肉毒杆菌毒素有关的毒素作用远距离传播 对于推荐剂量(30单位及以下)的睑缘痉挛,已报告了推荐剂量(100单位)的严重原发性腋窝多汗症,斜视或标记剂量的慢性偏头痛。
5.2肉毒杆菌毒素产品之间缺乏互换性
肉毒杆菌毒素的效价单位对所用的制备和测定方法具有特异性。它们不能与肉毒杆菌毒素产品的其他制剂互换,因此,肉毒杆菌的生物活性单位不能与通过任何其他特定测定方法评估的任何其他肉毒杆菌毒素产品的单位进行比较或转化为该单位[参见说明( 11 )] 。
5.3未经批准的严重不良反应
据报道,未经批准使用肉毒杆菌毒素注射的患者中,严重的不良反应包括过度虚弱,吞咽困难和吸入性肺炎,以及与致命后果相关的某些不良反应。在这些情况下,不良反应不一定与毒素的远距离传播有关,而可能是由于向注射部位和/或邻近结构施用肉毒杆菌毒素引起的。在某些情况下,患者患有吞咽困难或其他严重残疾。没有足够的信息来确定与未经批准使用肉毒杆菌素相关的不良反应风险增加的相关因素。尚未确定肉毒杆菌素在未经批准的用途中的安全性和有效性。
5.4过敏反应
已经报道了严重和/或立即的超敏反应。这些反应包括过敏反应,血清病,荨麻疹,软组织水肿和呼吸困难。如果发生这种反应,应停止进一步注射肉毒杆菌素,并立即开始适当的医学治疗。已经报道了一种致命的过敏反应,其中使用利多卡因作为稀释剂,因此不能可靠地确定病因。
5.5既往存在神经肌肉疾病的临床意义重大的风险增加
给予肉毒杆菌毒素时,应监测患有周围运动神经性疾病,肌萎缩性侧索硬化或神经肌肉连接障碍(例如重症肌无力或兰伯特-伊顿综合征)的个体。患有已知或未认识到的神经肌肉疾病或神经肌肉连接障碍的患者,临床上有明显影响的风险可能会增加,包括全身性肌肉无力,复视,上睑下垂,声音障碍,构音障碍,严重吞咽困难和治疗剂量的肉毒杆菌素会损害呼吸功能[参见 警告和注意事项( 5.1 , 5.6 )]。
5.6吞咽困难和呼吸困难
用肉毒杆菌毒素和其他肉毒杆菌毒素产品治疗可能会导致吞咽或呼吸困难。已有吞咽或呼吸困难的患者可能更容易出现这些并发症。在大多数情况下,这是注射或呼吸控制口咽或呼吸的口咽部肌肉中肌肉减弱的结果[请参阅警告和注意事项( 5.1 )]。
据报道,用肉毒杆菌毒素治疗后死亡是严重吞咽困难的并发症。吞咽困难可能会持续数月,并且需要使用喂食管来维持足够的营养和水分。严重吞咽困难可能会导致误吸,在吞咽或呼吸功能已受到损害的患者进行治疗时,这是一个特别的风险。
用肉毒杆菌毒素治疗可能会削弱作为通气辅助肌肉的颈部肌肉。这可能会导致呼吸系统疾病患者严重丧失呼吸能力,而这些患者可能已经变得依赖这些辅助肌肉。上市后有严重呼吸困难的报告,包括呼吸衰竭。
据报道,颈部肌肉较小的患者和需要双侧注射胸锁乳突肌以治疗颈肌张力障碍的患者发生吞咽困难的风险较高。限制注射入胸锁乳突肌的剂量可以减少吞咽困难的发生。注射到肩骨肩may骨可能与上呼吸道感染和吞咽困难的风险增加有关。
如果肉毒杆菌毒素患者出现吞咽,言语或呼吸系统疾病,则可能需要立即就医。这些反应可在注射肉毒杆菌毒素后数小时至数周内发生[见警告和注意事项( 5.1 )] 。
5.7肉毒杆菌素对患有痉挛性或与神经系统疾病相关的逼尿肌过度活动的呼吸状态不佳的患者的肺部影响
肉毒杆菌毒素治疗呼吸状况不佳的患者 对于痉挛应密切监测。在一项双盲,安慰剂对照,平行组研究中,对成年患者进行了上肢痉挛治疗,肺功能稳定下降(定义为FEV 1为预测值的40-80%,FEV 1 / FVC≤0.75),事件发生率肉毒杆菌毒素治疗的患者的强制肺活量(FVC)变化的≥15%或≥20%通常更大 与安慰剂治疗的患者相比(见表7)。
| 肉毒杆菌 360伙 | 肉毒杆菌 240伙 | 安慰剂 | ||||
| > 15% | > 20% | > 15% | > 20% | > 15% | > 20% | |
| 第一周 | 4% | 0% | 3% | 0% | 7% | 3% |
| 第六周 | 7% | 4% | 4% | 2% | 2% | 2% |
| 第十二周 | 10% | 5% | 2% | 1% | 4% | 1% |
与安慰剂的差异无统计学意义
在患有肺功能下降的成人痉挛患者中,与安慰剂相比,肉毒杆菌毒素治疗患者的不良反应也更常见于上呼吸道感染[ e警告和注意事项( 5.10 )] 。
在一项双盲,安慰剂对照,平行组研究中,对成年逼尿肌过度活动与神经系统疾病和限制性肺疾病的神经肌肉病因相关的成年患者[定义为FVC,C5至C5之间的脊髓损伤患者的预测值为50-80%和C8或MS],接受肉毒杆菌毒素治疗的患者中,≥15%或≥20%的强迫肺活量变化的发生率通常比接受安慰剂的患者高(参见表8)。
| 肉毒杆菌 200伙 | 安慰剂 | |||
| > 15% | > 20% | > 15% | > 20% | |
| 第二周 | 0/15(0%) | 0/15(0%) | 1/11(9%) | 0/11(0%) |
| 第六周 | 2/13(15%) | 1/13(8%) | 0/12(0%) | 0/12(0%) |
| 第十二周 | 0/12(0%) | 0/12(0%) | 0/7(0%) | 0/7(0%) |
5.8肉毒杆菌毒素治疗睑缘痉挛患者的角膜暴露和溃疡
减少肉毒杆菌毒素的眨眼 注射眼轮肌可导致角膜暴露,持续的上皮缺损和角膜溃疡,尤其是在患有VII神经疾病的患者中。应对任何上皮缺损进行大力治疗。这可能需要保护性滴剂,软膏,治疗性软性隐形眼镜或通过修补或其他方式闭眼。
5.9肉毒杆菌毒素治疗斜视患者的球后出血
在肉毒杆菌毒素治疗斜视的过程中,发生了足以损害视网膜循环的眼球后出血。建议使用适当的仪器对轨道进行解压缩。
5.10经痉挛治疗的患者的支气管炎和上呼吸道感染
与安慰剂(1%)相比,使用肉毒杆菌毒素治疗上肢痉挛的成年患者发生支气管炎的不良反应更为频繁(在251单位-360单位总剂量下为3%)。在接受上肢痉挛治疗的肺功能下降的成年患者中,与安慰剂相比,用肉毒杆菌毒素治疗的患者的不良反应也更为频繁(总剂量360单位为11%;总剂量240单位为8%)。 (6%)。在接受下肢痉挛治疗的成年患者中,与安慰剂(1%)相比,接受肉毒杆菌毒素治疗的患者中不良反应的发生率更高(总剂量300单位至400单位为2%)。在接受上肢痉挛治疗的小儿患者中,与安慰剂(9%)相比,接受肉毒杆菌毒素治疗的患者发生不良反应的发生率更高(6%/ kg时为17%,3units / kg时为10%)。 。在接受下肢痉挛治疗的小儿患者中,未报告上呼吸道感染的发生率高于安慰剂。
5.11逼尿肌过度活跃症与神经系统疾病相关联的患者的自主神经反射异常
接受肉毒杆菌内毒素注射引起的自主神经反射不良可能发生在因与神经系统疾病有关的逼尿肌过度活动而接受治疗的患者中,可能需要及时的药物治疗。在临床试验中,用Botox 200单位治疗的患者的自主神经反射不良的发生率高于安慰剂(分别为1.5%和0.4%)。
5.12膀胱过度活动症患者的尿路感染
肉毒杆菌素会增加尿路感染的发生率[见不良反应( 6.1 )] 。膀胱过动症的临床试验排除了过去6个月中有2种以上UTI的患者,以及因UTI复发而长期服用抗生素的患者。仅在获益可能超过潜在风险的情况下,才应考虑使用肉毒杆菌毒素治疗此类患者以及治疗期间多次复发性尿路感染的膀胱过度活动症患者。
5.13膀胱功能障碍患者的尿Re留
由于存在尿retention留的风险,如果需要,仅对愿意并能够在治疗后开始进行导管插入术的患者进行尿if留的治疗。
对于不使用导管的患者,应在治疗后2周内评估空后残留(PVR)尿量,并根据医学情况定期评估直至12周,尤其是在多发性硬化症或糖尿病患者中。根据患者症状,如果PVR尿液量超过200 mL,则开始导管插入术,并继续直至PVR降至200 mL以下。如果患者排尿困难,请指导他们与他们的医生联系,因为可能需要导管插入。
以下描述了接受肉毒杆菌毒素或安慰剂注射的膀胱过度活动症和逼尿肌过度活动症与神经系统疾病相关的患者的尿retention留的发生率和持续时间。
膀胱过度活动症
在针对OAB患者的双盲,安慰剂对照试验中,表9显示了在接受Botox或安慰剂治疗后开始进行清洁间歇性导管插入术(CIC)进行尿retention留的受试者的比例。还显示了谁出现了尿留。
| 时间点 | 肉毒杆菌100单位 (N = 552) | 安慰剂 (N = 542) | |||||
| 导尿以留置尿液的患者比例 | |||||||
| 在整个治疗周期中的任何时候 | 6.5%(n = 36) | 0.4%(n = 2) | |||||
| 具有高度临床意义。避免组合;互动的风险大于收益。 | |
| 具有中等临床意义。通常避免组合;仅在特殊情况下使用。 | |
| 临床意义不大。降低风险;评估风险并考虑使用替代药物,采取措施规避相互作用风险和/或制定监测计划。 | |
| 没有可用的互动信息。 |
药物状态
- 可用性 仅处方
- 怀孕和哺乳 现有风险数据
- CSA时间表* 不是管制药物
- 审批历史 FDA 1991年批准
美国日本医生

Suzanne Reitz MD

Bert Hepner DO

Gregory Aaen MD

Gregory Aaen MD

Gregory Aaen MD

渡邊剛

宮崎総一郎 中部大学特聘教授

百村伸一 教授

村上和成 教授

中山秀章 教授
临床试验
- 用于用一线osimertinib(LAT-Flosi)处理的少殖民NSCLC的LAT
- 针对口腔癌患者的个性化幸存者护理计划 - 对身体心理功能和重返工作
- 使用Tritanium®C前颈笼进行一或两层的前颈椎切除术和融合(Stryker)
- 躯干稳定练习对脑瘫生活质量和沟通的影响
- 食管测量和CT扫描测量的比较
- 可口的利多卡因凝胶对接受胃肠道上镜检查的患者的GAG反射作用
- 口咽运动和中风后阻塞性睡眠呼吸暂停
- 幽门螺杆菌幽门螺杆菌消除了不同的二氮四核治疗疗法
- 对青少年和成年人中的lanadelumab的研究,以防止与正常C1抑制剂(C1-INH)对非高 - 抗敏力血管性水肿的急性攻击
- TY-9591在晚期非小细胞肺癌(NSCLC)患者EGFR阳性突变患者中的研究